Кореспонденция на: Мария Емилия Л. Монтейро, доктор по медицина, професор, Катедра по вътрешни болести, Медицински колеж, Федерален университет Флуминенсе, Руа Марио Сардиня, 46, Сао Франциско, Нитерой, RJ 24360-007, Бразилия. rb.moc.arret@sedeugortsachl
Резюме
ЦЕЛ: Да се определи дали диетите с високо съдържание на протеини, мазнини и ниско съдържание на въглехидрати могат да причинят лезии в черния дроб на плъхове.
МЕТОДИ: Разделихме на случаен принцип 20 женски плъхове Wistar в контролна диетична група и експериментална диетична група. Животните от контролната група са получавали диета AIN-93M, а животните от експерименталната група са получавали диета, базирана на Аткинс (59,46% протеин, 31,77% мазнини и 8,77% въглехидрати). След 8 седмици плъховете бяха анестезирани и обезкървени за анализ на трансаминази и черният им дроб беше отстранен за изследвания на поточна цитометрия, имунохистохимия и светлинна микроскопия. Ние изразихме данните като средно ± стандартно отклонение (SD), приемайки несдвоени и параметрични данни; анализирахме разликите, използвайки t-теста на Student. Статистическата значимост е определена при Р Ключови думи: Апоптоза, нараняване на черния дроб, диета с високо съдържание на протеини, диета с високо съдържание на мазнини, диета с ниско съдържание на въглехидрати
Основен съвет: Затлъстяването е сериозен и нарастващ здравословен проблем. Диета с високо съдържание на протеини, мазнини и ниско съдържание на въглехидрати, известна като диетата на Аткинс, е приета от 70-те години на миналия век. Много хора се придържат към тази диета в опит да отслабнат и наскоро тя е въведена за деца с трудно контролируеми припадъци и възрастни хора, страдащи от болестта на Алцхаймер и Паркинсон. Ползите и ефектите от диетата на Аткинс остават неясни, особено при чернодробния метаболизъм. Тъй като първичните метаболитни реакции, включващи макронутриенти, се проявяват в черния дроб, от съществено значение е да се разберат потенциалните чернодробни лезии, които могат да бъдат резултат от диетични модификации.
ВЪВЕДЕНИЕ
Разпространението на затлъстяването нараства в световен мащаб сред възрастни, младежи и деца; този сериозен здравен проблем изисква широко обществено мобилизиране в търсене на решения. Изключително голям брой хора се придържат към специални диети в опит да отслабнат [1]. Диетата с високо съдържание на протеини, мазнини и ниско съдържание на въглехидрати е обявена от американския кардиолог Робърт С. Аткинс в средата на 70-те години на миналия век за най-добрия и здравословен начин да станете слаби [2]. Тази така наречена „диета на Аткинс“ или „протеинова диета“ продължава да се разглежда като „въпрос на любов или омраза“ [3]. Тази диета беше въведена наскоро за деца с трудно контролируеми припадъци и възрастни хора с болестта на Алцхаймер и Паркинсон [4]. Въпреки многобройните медицински публикации, свързани с диетата на Аткинс, резултатите от повечето такива проучвания са неубедителни и не успяват да покажат ползи и ефекти, особено при метаболизма в черния дроб [5].
Няколко проучвания съобщават за връзки между високо протеинова диета и промени в черния дроб [6], чревната лигавица [7], бъбреците [8,9], панкреаса [10], мастната тъкан [11] и костите [9,12 ]. Тъй като първичните метаболитни реакции, включващи макронутриенти, се проявяват в черния дроб, от съществено значение е да се разберат потенциалните чернодробни лезии, които могат да бъдат резултат от диетични модификации. Доказано е, че диетите с високо съдържание на мазнини или с ниско съдържание на въглехидрати могат да причинят чернодробна стеатоза, свързана с прекомерно търсене на мастни киселини от диетата и от мастните тъкани, като последица от глюконеогенезата [5]. В наскоро публикувано проучване беше установено, че диета с високо съдържание на протеини (независимо от количеството и вида на мазнините или въглехидратите) не води до стеатоза и всъщност може да я обърне [13].
Чернодробните клетки са важни цели за лезии при наличие на прекомерни хранителни компоненти, тъй като те се абсорбират през чревната лигавица и бързо достигат до черния дроб през порталната вена [6]. Сред макронутриентите въглехидратите и мазнините са до голяма степен отговорни за наблюдаваните промени, тъй като те насърчават промени в генната транскрипция и гликолитичните и липогенни ензими [стерол реагиращ свързващ протеин 1/2 (SREBP) и целта на рапамицин за бозайници - mTOR), инсулин и адипокини ] [14].
Необходими са допълнителни хистопатологични изследвания на черния дроб на животни, хранени с нисковъглехидратна и високобелтъчна диета, тъй като досегашните резултати са противоречиви [19,20].
Тук предположихме, че диетата с високо съдържание на протеини (59.46%), с мазнини (31.77%) и с много ниско съдържание на въглехидрати (8.77%) може да причини хепатоцитни лезии, както е установено чрез поточна цитометрия и имунохистохимия (IHC). Ние имахме за цел да свържем резултатите от цитометрията с промени в светлинната микроскопия и нивата на плазмените трансаминази.
МАТЕРИАЛИ И МЕТОДИ
Животни
Експерименталното проучване е проведено от март-май 2015 г. в Експерименталната лаборатория по хранене на Nutrition College, Федерален университет Fluminense, Niterói, RJ, Бразилия. Протоколът с животни минимизира болката и дискомфорта за плъховете. Експериментът използва 20 женски плъхове Wistar (Rattus norvegicus) на възраст от 11-13 седмици. Животните тежаха 211-249 g и бяха отгледани в лабораторията за животни на Фондация Oswaldo Cruz, Министерство на здравеопазването, Рио де Жанейро, Бразилия. Животните бяха държани в групови клетки с по четири животни, за адаптация, в продължение на 5 дни, получаване на вода и лабораторна диета ad libitum. След този период плъховете бяха разделени на случаен принцип в две групи от по 10 животни [контролната диетична група (CDG) и експерименталната диетична група (EDG)] и индивидуално настанени в полипропиленови клетки с контролирана температура (24 ± 2 ° C) и влажност (60% ± 10%) и редуващ се цикъл светлина-тъмнина, състоящ се от 12 часа светлина и тъмнина.
Диети
Диетата CDG, състояща се от диетата AIN 93M [21], е формулирана за поддържане на възрастни плъхове от Американския институт по хранене през 1993 г .; основахме разработената EDG диета на диетата на Аткинс. И двете групи са получавали вода и диета ad libitum за 8 седмици. Диетите бяха изготвени от Pragsoluções Biociências Comércio e Serviços, LTD, Jaú, Сао Пауло, Бразилия. Контролната диета имаше следния състав: въглехидрати (76,98%), протеини (13,56%) и мазнини (9,46%). Експерименталната диета е съставена от въглехидрати (8,77%), протеини (59,46%) и мазнини (31,77%). Количеството витамини, минерали, L-цистеин, холин и фибри са еднакви в двете групи, а трет-бутилхидрохинонът е изчислен като 0,002 mg на грам мазнина, всички въз основа на AIN 93M определения (Таблици (Таблици 1 1 и И2 2).
маса 1
Състав на контролната диета (AIN-93M)
| Съставки | g/100 g | CH (g) | PTN (g) | Устни (g) | FI (g) |
| Царевично нишесте | 46.5 | 39,52 | |||
| L-цистеин | 0,18 | 0,18 | |||
| Холин битартрат | 0,25 | 0,25 | |||
| Минерален микс | 3.50 | 0,77 | |||
| Витаминен микс | 1 | 0,97 | |||
| Трет-бутилхидрохинон | 0,008 | ||||
| Фибри | 5 | 5 | |||
| Соево масло | 4 | 4 | |||
| Казеин (> 85% протеин) | 14. | 11.06 | |||
| Захароза | 10 | 10.00 | |||
| Декстринизирано царевично нишесте | 15.5 | 13,95 | |||
| Kcal (%) | 338,8 | 260,84 | 45,96 | 32 | |
| Макронутриенти (%) | 100 | 76,98 | 13.56 | 9.46 |
Контролната диетична група е хранена с тази диета в продължение на 8 седмици, разработена от Американския институт по хранене през 1993 г. за лабораторни гризачи, с адекватни проценти на макроелементи въглехидрати (CH), протеини (PTN) и липиди (LIP), витамини, минерали и фибри (FI).
Таблица 2
Състав на експерименталната диета (въз основа на диетата на Аткинс)
| Съставка | (g/100 g) | CH (g) | PTN (g) | Устни (g) | FI (g) |
| Агар | 2 | 2 | |||
| L-цистеин | 0,18 | 0,18 | |||
| Холин битартрат | 0,25 | 0,25 | |||
| Минерален микс | 3.5 | 0,77 | |||
| Витаминен микс | 1 | 0,97 | |||
| Трет-бутилхидрохинон | 0,028 | ||||
| Фибри | 5 | 5 | |||
| Захароза | 6 | 6 | |||
| Казеин (> 85% протеин) | 20. | 16. | |||
| Пилешки гърди на прах | 60 | 36 | 12 | ||
| Соево масло | 2 | 2 | |||
| Kcal (%) | 352,68 | 30,96 | 209,72 | 112 | |
| Макронутриенти (%) | 100 | 8,77 | 59.46 | 31.77 |
Експерименталната диетична група е хранена с тази диета в продължение на 8 седмици, разработена от авторите въз основа на диетата на Аткинс. Процентът на макронутриентите е 2: 1 въглехидрати (CH) + протеин (PTN)/липиди (LIP) с фибри (FI). Останалите съставки имаха същото количество, както се препоръчва за AIN-93M.
Експериментални процедури и събиране на проби
На сутринта на деня на жертвоприношението всички животни са подложени на вагинални цитонамазки, за да се определи фазата на естросния им цикъл. Животните в еструса бяха разделени и нямаше повече достъп до храна. След 8 часа на гладно животните се упояват чрез интраперитонеално инжектиране на разтвор, съдържащ 11,50 mg/100 g телесна маса кетамин и 0,10 mg/100 g телесна маса ксилазин и са обезкървени чрез сърдечна пункция [22]. След това те бяха жертвани един по един, като се редуваха между експерименталната и контролната група. Кръвта се поставя в хепаринизирана епруветка и се центрофугира в продължение на 20 минути при 314 rad/s и плазмата се отделя и съхранява при -80 ° С до анализ. Черният дроб се отстранява след изтегляне на кръвта и шест чернодробни фрагмента с размери 1 cm 3 се измиват внимателно с NaCl 0,9%, потапят се в реципиент със същия разтвор и се съхраняват във фризера при -4 ° C за 2 часа преди извършване поточна цитометрия.
Аналитични методи
Статистически анализ
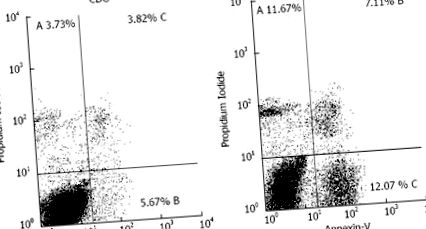
Проточна цитометрия в хепатоцити от експерименталната диетична група и контролна диетична група при 8 седмици. Анексин-V се използва за идентифициране на късна апоптоза и неапоптотична смърт и пропидиев йодид за ранна апоптоза. A-% ранна апоптоза; B-% неапоптотична смърт; C-% късна апоптоза; D-% жизнеспособни клетки. EDG: Експериментална диетична група; CDG: Контролна диетична група.
Когато се сравняват нежизнеспособните клетки в двете групи, само средният процент на ранна апоптоза е статистически значим (Таблица (Таблица 3 3).
Таблица 3
Нежизнеспособни клетки в експериментална диетична група и контролна диетична група
Оцветяване на чернодробни фрагменти при 8 седмици: експериментална диетична група и контролна диетична група. О: Нормална централна вена, функционална синусоидална дилатация и малки хепатоцити в EDG (HE, първоначално увеличение 400 ×); B: Нормална централна вена, синусоидални клетки и хепатоцити в CDG (HE, първоначално увеличение 400 ×); C: Зони без гликоген в EDG (HE, първоначално увеличение 400 ×); D: Хомогенно разпределение на гликогена в CDG (HE, първоначално увеличение 400 ×). EDG: Експериментална диетична група; CDG: Контролна диетична група; ТОЙ: Хематоксилин и еозин.
ДИСКУСИЯ
Както се очакваше, установихме, че диетата с високо съдържание на протеини, мазнини и ниско съдържание на въглехидрати причинява клетъчни и хистопатологични лезии в черния дроб на опитни гризачи. ALT и AST бяха увеличени в EDG в сравнение с CDG. Тъй като тези тестове се считат за точни чернодробни функционални тестове, нашите резултати потвърждават наличието на чернодробно увреждане, включващо разрушаване на хепатоцитите с нарушаване на плазматичната мембрана и къснофазова апоптоза и неапоптотична смърт в EDG [23,24].
В проучване на Jean et al [25] група животни, които са получили диета, състояща се от 50% протеин, показват висок ALT и нормален AST в сравнение с контролите, които са получили модифицирана AIN-93M диета. Резултатите бяха интерпретирани като чернодробни лезии, тъй като ATL е специфичен чернодробен ензим, разположен в хепатоцитната цитоплазма; AST може да се изрази и чрез мускули и бъбреци [23,25]. Oarada et al [6] демонстрират, че когато плъховете се хранят с нарастващи количества протеин (35%, 40%, 45% и 50%), ALT и AST се увеличават в същата степен. Съответно тези автори стигнаха до заключението, че независимият от протеини макронутриенти и консумацията на енергия е рисков фактор за увреждане на черния дроб. В скорошно проучване Kostogrys и сътр. [26] не откриват промени в нивата на плазмените трансаминази с диета от 50,0% протеини, 37,7% мазнини и 12,3% въглехидрати, въпреки че черният дроб е увеличен в сравнение с животните, получаващи диетата AIN93-M. Сравняването на нашите резултати с тези, отбелязани в литературата, може да бъде трудно, тъй като процентите на макроелементите, хранени с плъхове, варират в различните проучвания.
Проточната цитометрия потвърждава чернодробното увреждане, както се демонстрира от повишените нива на плазмените трансаминази; 30,85% от хепатоцитите са нежизнеспособни в EDG в сравнение с 13,22% при контролните животни. Нежизнеспособните клетки в CDG включват 3,73% ранна апоптоза, 5,67% късна апоптоза и 3,82% неапоптотична смърт. Тези открития в контролната група могат да се считат за физиологични, тъй като апоптозата и неапоптотичната смърт представляват непрекъснат процес, който е отговорен за поддържането на баланса между пролиферацията и клетъчната смърт. Неапоптотичната смърт е част от същия процес, тъй като това е крайната съдба на клетките, претърпели апоптоза [24].
Апоптозата беше значително увеличена в EDG, с 11,67% ранна апоптоза, 12,07% късна апоптоза и 7,11% неапоптотични клетки, показващи нефизиологично състояние. Всяко нарушаване на регулацията на апоптозата е вредно и води до увреждане на тъканите [15]. Подобни резултати са открити от Chiang et al [27], които демонстрират, че мишките, получаващи 8-седмична диета с 60% протеин, показват промени в телесното тегло, хистологията на черния дроб и експресията на апоптоза и фиброза.
Друго важно откритие на настоящото проучване е, че процентът на ранна апоптоза, дегенерация на иРНК, е значително по-висок в EDG (37,34%) в сравнение с този в CDG (28,43%) (P Huang TT, Cawley JH, Ashe M, Costa SA, Frerichs LM, Zwicker L, Rivera JA, Levy D, Hammond RA, Lambert EV, et al. Мобилизиране на публична подкрепа за политически действия за предотвратяване на затлъстяването. Lancet. 2015; 385: 2422–2431. Doi: 10.1016/S0140 -6736 (14) 61743-8. [PubMed] [CrossRef] [Google Scholar]
- Активирането на AMPK предпазва от затлъстяване, предизвикано от диета, чрез независима от Ucp1 термогенеза в
- Прекъсващото гладуване, високопротеинова диета ми помогна да отслабна 105 Lbs
- Благоприятни ефекти на какао, кафе, зелен чай и гарциния комплекс добавка върху диета индуцирани
- Диетата с високо съдържание на протеини може да ви запек
- Може ли нисковъглехидратната диета да помогне на страдащите от мигрена