Когато увеличите храната си, какво ще видите? Първото нещо, което ще забележите, е детайлът във всички сложни структури на храната. Увеличавайки по-близо, вероятно ще се сблъскате с някои клетки. Когато погледнете още по-отблизо, ще видите, че тези клетки отново са изградени от много различни молекули. И тези молекули отново са изградени от атоми.
Тези молекули и атоми образуват нашата храна, те определят структурата на вашата храна, хранителната стойност и какъв тип реакции могат да възникнат по време на готвене или обработка. Разбирането на тези атоми и молекули до известна степен със сигурност ще ви помогне да разберете храната си и по-задълбочените публикации в нашия блог, където понякога сме склонни да приемаме определени знания.
Ако думите, молекулите и атомите ви карат да се страхувате, продължете да четете, ние ще ви обясним какви са и как работят и ще въведем три много важни групи молекули: въглехидрати, протеини и мазнини. В края на тази публикация химията вече не трябва да звучи толкова страшно:-).
Интересувате ли се да научите повече за тези основни концепции на науката за храните? Разгледайте нашия курс „Основи на хранителната химия“, ние сме събрали всички основи заедно с викторини и слайдшоута, за да ви помогнем да разберете още по-добре основите!
Представяме ви: Атомите в храната
Хранителната химия често започва с атоми, атомите образуват молекули и именно тези молекули изучаваме в хранителната химия. И така, ще започнем тази поредица от основи на химията на храните с атоми.
Атомите са градивните елементи на молекулите, всеки и всичко в този свят е изградено от атоми. Атомите не могат да се видят в светлинен микроскоп, те са много много малки, обикновено 1 милиардна част от метър!
Има различни типове атоми (ще се върнем към това по-късно), но всеки тип атом се изгражда по подобен начин. Основните градивни елементи на всички атоми са три основни „парчета“: протони, неутрони и електрони. Различните типове атоми ще имат различен брой на тези строителни блокове, но те ще съдържат един и същи тип строителни блокове.
Протони, неутрони и електрони
Важна концепция на тези три градивни блока е, че всеки от тях има електрически заряд. Протоните имат положителен заряд, електроните са отрицателно заредени, а неутроните нямат заряд, както казва името им, те са неутрални.
Протоните и неутронът на атома образуват центъра (ядрото) на атома, отрицателно зарядните електрони се носят около този център на малко по-голямо разстояние. Електроните са малки в сравнение с протоните и неутроните. Тъй като те се отдалечават от ядрото, те могат да бъдат по-лесни за обмен между атоми. Те играят важна роля в химичните реакции и при производството на молекули.
Роля на протоните: определяне на елемента
Броят на протоните в атома определя кой тип атом разглеждаме. Този тип атоми се наричат още „елементи“. В света има ограничен брой елементи (или типове атоми), само 118. Всички те са групирани в така наречената таблица с периоди на елементи, за които може би сте чували в уроците по химия. Най-простият елемент има само един протон, всеки следващ елемент има един допълнителен протон, до този 118.
Докато електроните могат да се обменят доста лесно, това не е така за протоните и неутроните. Има реакции, при които те се разменят, но в повечето хранителни химикали това няма да се случи (помислете: ядрена химия).
Ще разгледаме елементите, които най-често се срещат в храната (за щастие това не са всичките 118) в тази публикация, но като въведение е добре да разберете кои елементи изобщо съществуват. Какъв по-добър начин да направите това, отколкото чрез песен?
Неутроните определят изотопа
Така че електроните се „вихрят“ около ядрото на протоните и неутроните и играят важна роля в химичните реакции. Броят на протоните определя елемента, така че какво правят неутроните? Броят на неутроните определя изотопа на даден елемент. За храната това не е много уместно, но за ядрената химия това е много важна концепция. Поради тази причина няма да го обсъждаме повече тук.
Най-често срещаните елементи (видове атоми) в храната
Тъй като има 118 елемента, химиците трябваше да намерят удобен начин да ги назоват. Използването на пълните им имена през цялото време би било объркващо, особено когато започнем да описваме молекули, които отново са изградени от атоми. Следователно, всеки елемент има собствено съкращение от една, две или три букви (както можете да видите в периодичния системен филм).
В храната има относително малък брой общи атоми. Четири от тях са особено често срещани, въглерод, кислород, азот и водород. Нека обсъдим най-важните:
- Въглерод (С): това е градивният елемент на повечето молекули, които ще срещнем в храната. Важно е за мазнините, въглехидратите и протеините. Без въглерод повечето молекули в храната не могат да се образуват.
- Кислород (O): кислородът е особено добър за участие във всякакви химически реакции. Кислородът има доста налични електрони, които често се използват за свързване на две молекули една към друга или разделяне на молекули на парчета.
- Азот (N): този атом е от съществено значение за производството на протеини. Без азотни протеини не може да се образува. Азотната група също е често срещано място за протичане на реакции.
- Водородът (H): вероятно е най-разпространеният атом, но не е толкова интересен в повечето системи. Водородът често „запълва“ празни пространства в молекулите. Ще видите, че щом обсъдим киселини и основи, това наистина е много важен атом!
След 4-те „големи“ атома има няколко други, достойни за обсъждане:
- Фосфор (P) и сяра (S): често играят интересна роля в протеиновата химия.
- Натрий (Na) и хлорид (Cl): чували сте за сол, която по същество е комбинация от тези две, по този начин натрий и хлорид!
- Калций (Ca): важен минерал за вашите кости.
Молекули
Молекулите са по-големи структури от атоми, които са реагирали помежду си, за да образуват стабилен компонент. Повечето атоми не са стабилни сами по себе си, няма да намерите чист кислороден атом във въздуха, вместо това два кислородни атома ще са реагирали, за да образуват една кислородна молекула (O2). Същото важи и за водорода (H2).
Използваме съкращенията на току-що научените атоми, за да посочим кои от тези атоми присъстват в молекулата. Всяка молекула ще бъде различна комбинация от тези атоми. Атомите ще бъдат прикрепени един към друг по различни начини и подредби.
Молекулите са представени чрез показване на буквите на атомите, от които са изградени, и използване на малък индексен номер, за да се посочи колко от този атом присъства в молекулата (както направих за молекулите кислород и водород). За химиците тези молекулни формули са от съществено значение за описване на процесите, които изучават.
В отделен пост обсъждаме тези формули по-подробно.
Структура на молекулите
Много е полезно да знаете кои атоми присъстват в молекулата. Това обаче не казва на химиците цялата история. Вместо това трябва да знаете и как тези атоми са прикрепени един към друг. Начинът, по който атомите са прикрепени един към друг, силно влияе върху начина, по който ще реагират.
Има молекули, които могат да имат една и съща химическа формула (така че са съставени от един и същи вид и брой атоми), но имат напълно различна структура и следователно структурна формула! Те всъщност могат да реагират и да се държат доста различно, въпреки че в началото може да изглеждат подобни.
Пример за храна са глюкозата и фруктозата. И двете са изградени от едни и същи атоми: C6H12O6. Химичната им структура и поведение обаче са доста различни (прочетете повече за подсладителите тук).
Засега няма да се впускаме в начина, по който тези молекули се изграждат, рисуват и показват. Вместо това, нека започнем да прилагаме наученото досега, като разгледаме най-често срещаните групи молекули в храната: въглехидрати, протеини и мазнини. Тези молекули се наричат още „макронутриенти“ и са от съществено значение за нас от хранителна гледна точка. Трите групи молекули имат много различни характеристики, които ще повлияят на това как ще се получи храната ви. Те играят важна роля в реакциите на покафеняване, както и развитието на вкуса и вкуса.
Въглехидрати
Въглехидратите са изградени от въглерод (С), кислород (О) и водород (Н) атоми. Повечето въглехидрати могат да бъдат описани чрез следната химическа формула: CxH2yOy. С други думи, броят на водородните атоми е два пъти по-голям от този на кислорода. Броят на въглеродните атоми не трябва да е свързан с броя на кислородните и водородните атоми. (Забележете, има няколко изключения от това правило!)
Въглехидратите също могат да се нарекат захариди. Когато се говори за захариди, се прави общо разделение на четири групи: монозахариди, дизахариди, олигозахариди и полизахариди. Разделянето се извършва въз основа на размера на молекулите.
Монозахаридите са най-малките въглехидрати, те не могат да се разделят, за да образуват още по-малки захариди. Глюкозата и фруктозата са може би най-известните монозахариди. И двете имат една и съща химична формула: C6H12O6. Независимо от това, те са изградени по малко по-различен начин, което ги кара да реагират напълно различно в тялото ви.
Дисахаридите са следващите най-малки захариди. Винаги са изградени от 2 монозахархида. Например, лактозата се произвежда от глюкоза и галактоза. Захарозата (обикновена трапезна захар) се произвежда от фруктоза и глюкоза.
Следващата стъпка са олигозахаридите, те са направени от повече от 2 монозахариди, обикновено от 3 до 10. Тези молекули често могат да бъдат намерени в растенията, придавайки им структура. Олигозахаридите често образуват влакнестата част на растението.
Не на последно място идват и полизахаридите. Това са огромни молекули, съставени от повече от 10 монозахариди. Те могат да образуват сложни структури, монозахаридът не е задължително да образува една дълга верига, вместо това те могат да образуват сложни мрежи. Въпреки че всички полизахариди са направени от монозахариди, те могат да се държат доста различно. Чест пример за полизахарид в храната е нишестето (отново състоящо се от два различни полизахарида: амилоза и амилопектин).
Протеини
Протеините са друго основно хранително вещество за нас, хората с различна молекулярна структура. Протеините са по същество много дълги вериги от молекули, с някои странични вериги, които се сгъват в много сложна. Протеините са много по-големи от въглехидратите. От повечето протеини няма да можете да запишете молекулната формула, те са сложни, с твърде много различни атоми.
Това каза, че тази дълга верига има непрекъснато повтарящ се модел. Това е дълга верига от така наречените аминокиселини, които са реагирали, образувайки тази дълга верига. Понастоящем има 23 известни различни аминокиселини (всяка с различна R-група на чертежа по-долу), които, когато се комбинират, могат да създадат всички протеини. Аминокиселините образуват протеини, образувайки една дълга верига. OH-групата ще реагира с NH2 групата (освобождавайки водна молекула), за да образува връзка между двете аминокиселини.
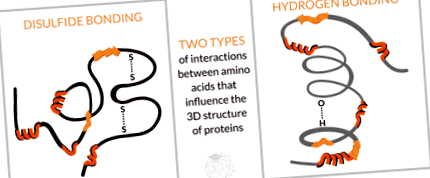
За разлика от въглехидратите, няма разграничение въз основа на размера на протеините. Има много различни протеини и всички те са склонни да бъдат огромни и много сложни. Тъй като това е толкова дълга верига от аминокиселини, много взаимодействия могат да възникнат във веригата. Различни странични групи (R- на чертежа по-горе) могат да си взаимодействат. Те няма да се „свързват“ както молекулите във веригите, но могат да се отблъснат или привличат една друга. Има много различни взаимодействия, които могат да възникнат. Тези взаимодействия могат да накарат дългите нишки да се сгънат или да се завъртят във всякакви триизмерни структури и те отново ще се организират по специфичен начин.
Цялостната форма на протеиновите молекули е много важна за неговата активност. Тази форма се определя от това как тази дълга верига от аминокиселини се сгъва и превръща. След като 3D структурата бъде разрушена, протеините ще се държат много различно, виждаме това при готвене на яйца, нагряване на ензими (които са специфичен вид протеини), готвене на месо или приготвяне на сирене!
Не на последно място: мазнини. Въпреки че продуктите с ниско съдържание на мазнини могат да се видят наоколо, не можете да приемате без консумация на мазнини. Мазнините са също толкова важни за нас, колкото протеините и въглехидратите.
Мазнините принадлежат към по-голяма група молекули, които се наричат липиди, мазнините са специфична подгрупа на липидите. Всички липиди са хидрофобни молекули (те не обичат водата). Пример за липид, който не е мазнина, е холестеролът.
Химично правилното описание на мазнините е: триглицериди. Когато мазнините са течни при стайна температура, те обикновено се наричат масла. Името триглицерид описва основната структура на мазнините: една молекула глицерол, с три мастни киселини, прикрепени към нея (виж по-долу).
Както беше при протеините и въглехидратите, има много различни мазнини. Има много различни мастни киселини и те отново могат да се комбинират по много различни начини, за да образуват различни триглицериди!
На структурния чертеж на мастна киселина по-горе можете да видите А. Това А означава факта, че може да има много различни вериги, започвайки от този момент. A винаги ще се състои от дълга верига от въглеродни атоми. Броят на въглеродните атоми в тази верига може да варира от само 4 до над 20 въглеродни атома.
Друга много важна характеристика е дали има така наречените двойни връзки между въглеродните атоми. Както можете да видите на изображението по-долу, тези двойни връзки могат да накарат молекулите да променят посоката си, вместо да образуват права линия. Мастните киселини без двойна връзка се наричат наситени, тези с двойна връзка са ненаситени.
Видовете мастни киселини, присъстващи в триглицеридите, ще определят свойствата на действителната мазнина или масло. Един от тях е точката на топене.
Колкото по-дълга е веригата на мастните киселини, толкова по-висока ще бъде точката на топене на мазнината. По-малките молекули могат да се движат по-лесно, така че се нуждаят от по-ниска температура, за да станат течни. Същото важи и за молекулите, които имат двойни връзки, ако двойната връзка е от типа, който кара мастната киселина да има извивка в структурата си, тя ще понижи точката на топене. Причината е, че тези изкривявания затрудняват мазнините да се структурират една до друга.
Прилагане на нашите знания
Всичко това е доста теоретично, за съжаление, ако сте нов в темата, това е, което ще ви трябва, за да разберете явленията, които виждате в храната си. Но сега е време да видим как някои знания оживяват!
Хареса ли ви наученото и искате да научите повече основи на науката за храните? Помислете за записване в нашия курс по основи на хранителната химия, където се гмуркаме малко по-дълбоко и ви даваме шанса да тествате знанията си в нашите тестове!
- Вижте как протеините оживяват в:
- Глутен
- Сирене
- Риба
- Вижте как мазнините оживяват в:
- Зехтин (внимавайте за окисляване)
- Пържене
- Свинска мас
- Сладолед
- Вижте как захарите оживяват в:
- Медена пита
- Бисквитки
- Торта от моркови
- Ръководство за печат за представяне на нови храни на вашето бебе; Food Insight
- Август - Национални празници на храната
- 7 зърна без глутен, за които трябва да знаете - NDTV Food
- 1-годишна диаграма за бебешка храна
- Предимство на накисването на леща, истината за фибрите и други вегетариански митове, Food News & Top