Резюме
Заден план
Азотът на уреята в кръвта (BUN) е едно от веществата, което влияе върху изчислената серумна осмолалност (cSosm). Предишно проучване показа, че BUN и cSosm са независимо свързани с развитието на хронично бъбречно заболяване (ХБН) при пациенти със запазена бъбречна функция. В напредналите стадии на ХБН има едновременно повишаване на нивата на cSosm и BUN. Въпреки това остава неясно дали нивата на BUN или cSosm са свързани с бъбречните резултати при пациенти с умерена до тежка бъбречна дисфункция. Целта на това проучване е да изясни дали нивото на BUN или cSosm е свързано с прогресия на бъбречните заболявания при пациенти с напреднала ХБН.
Методи
В това проспективно проучване включихме 459 пациенти с ХБН (стадии 3–5). Комбинираната бъбречна крайна точка е краен стадий на бъбречно заболяване (ESRD) или смърт и ESRD самостоятелно е добавен като алтернативен резултат. За определяне на рисковите фактори за лош бъбречен изход е използван модел на Кокс с пропорционални рискове. Ние коригирахме за ковариати, включително изчислената скорост на гломерулна филтрация (eGFR). CSosm (mOsm/kg) се изчислява, като се използва следната формула: (2 × натрий) + (BUN/2.8) + (глюкоза/18).
Резултати
По време на средно проследяване от 25,8 месеца, бъбречната крайна точка се наблюдава при 210 пациенти. Мултивариативният анализ на Cox определя коефициента на риск (HR) [95% доверителен интервал (CI)] за съставния бъбречен изход във втория, третия и четвъртия BUN квартил е 1,36 (0,72–2,58), 1,87 (0,95–3,66) и 2,66 (1,23–5,76) (P за тенденция
Заден план
Уреята е основният метаболит, получен от диетичния протеин и от обмяната на протеини в тъканите. Той се филтрира свободно в гломерула, но не се секретира и се реабсорбира от бъбречните каналчета. В допълнение, с намаляването на скоростта на потока на урината се реабсорбира повече урея [1]. Азот в уреята в кръвта (BUN) измерва азотния компонент на серумната урея. Нивата на BUN корелират обратно с намаляването на бъбречната функция [2] и се влияят също от извънбъбречни фактори като прием на протеини, стомашно-чревно кървене, катаболни състояния, недохранване, сърдечна недостатъчност, дехидратация, използване на глюкокортикоиди и синтез на чернодробна урея [3].
При физиологични условия карбамидът бавно се дисоциира в цианат, който бързо се превръща в изоцианат. Изоцианатът е реактивен електрофил с висок афинитет към нуклеофилни групи като първични амини [4]. Признато е, че карбамилирането е спонтанна модификация на аминокиселини и протеини, медиирани от цианата, след транслация, което води до биохимични промени. Доказано е също така, че уреята може да упражнява директна токсичност върху различни тъкани като чревния епител, съдовите стени, панкреасните β-клетки и адипоцитите и индиректната токсичност чрез карбамилиране [5, 6]. По-специално, нивата на BUN са свързани със смъртността сред пациентите със сърдечна недостатъчност [7, 8].
Методи
Пациенти и дизайн на проучването
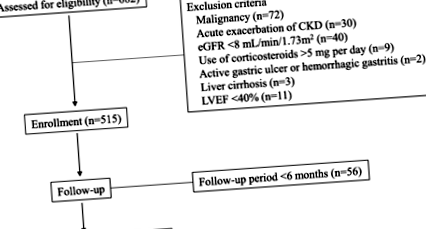
Шестстотин осемдесет и два последователни японски пациенти с ХБН етап 3–5 бяха приети в нашата болница, Националната болнична организация Кюшу Медицински център, за оценка и обучение относно ХБН между юни 2009 г. и декември 2017 г. Фигура 1 показва блок-схема на пациента процес на записване. За да се намалят ефектите на извънбъбречните фактори върху нивата на BUN, пациенти, които са използвали кортикостероиди в доза> 5 mg/ден или които са имали активна стомашна язва или хеморагичен гастрит, чернодробна цироза или фракция на изтласкване на лявата камера Фиг. 1
Блок-схема на процеса на записване. ХБН, хронично бъбречно заболяване; eGFR, изчислена скорост на гломерулна филтрация; LVEF, фракция на изтласкване на лявата камера
Клинични и биохимични оценки
Кръвни проби бяха получени от всеки пациент рано сутринта след пост през нощта. Измервана е и дневна протеинурия. EGFR (ml/min/1,73 m 2) е изчислен, като се използва следното ново уравнение за японски пациенти: 194 × серумен креатинин - 1,094 × възраст - 0,287 × 0,739 (ако е жена) [14]. CSosm (mOsm/kg) се изчислява, като се използва следната формула: (2 × натрий) + (BUN/2.8) + (глюкоза/18) [15].
Клиничните оценки при постъпване и определенията за хипертония, захарен диабет, тютюнопушене и дислипидемия са описани в предишния ни доклад [13]. Направена е ехокардиограма за оценка на диаметъра на лявото предсърдие и фракцията на изтласкване на лявата камера.
Статистически анализ
Непрекъснатите данни се изразяват като средна стойност ± SD или медиана (интерквартилен диапазон) в зависимост от тяхното разпределение. Нивата на участниците BUN бяха разделени на квартили. Категоричните данни бяха сравнени за BUN квартили, използвайки хи-квадрат теста с точния тест на Fisher, използван за групи, съдържащи по-малко от пет индивида във всяка дадена клетка. Използван е дисперсионен анализ (ANOVA) за сравняване на непрекъснати променливи, които са приблизително нормално разпределени, а тестът на Kruskal – Wallis е използван за сравняване на изкривени непрекъснати променливи. Участниците cSosm нива също бяха разделени на квартили. Коефициентите на корелация на ранга на Спиърман бяха използвани за идентифициране на връзката между две непрекъснати променливи.
Резултати
Средният период на проследяване е 25,8 месеца (диапазон, 1,2–95,8 месеца). В края на проследяването 210 пациенти са достигнали съставната бъбречна крайна точка. Тридесет и седем пациенти са починали преди да достигнат ESRD. Причините за смъртта са инфекциозни заболявания при девет пациенти, внезапна смърт при седем, уремия при пет, злокачествено заболяване при четири, сърдечни заболявания при пет, други определени причини при пет и неизвестни при двама.
Анализът на Каплан-Майер показва значително по-високи нива на бъбречни събития в по-високите BUN квартили (фиг. 2). Таблица 2 показва HRs за съставен бъбречен изход според квартилите на BUN или cSosm. При многопроменлив анализ (Модел 3), по-високите BUN квартили имат значително по-висок риск от неблагоприятни бъбречни резултати в сравнение с най-ниския квартил. За разлика от това, в сравнение с най-ниския квартил на cSosm, не е установено значително увеличение на риска от лоши бъбречни резултати при по-високите квартили на cSosm в Модел 3. Сплайн анализът на връзката между BUN и риска от неблагоприятни бъбречни резултати показва, че рискът от лоши бъбречни резултати беше прогресивно по-висок с увеличаване на нивото на BUN (фиг. 3).
Криви на Каплан-Майер за свобода от съставен бъбречен изход при пациенти, стратифицирани по квартили на BUN и сравнени с използване на лог-рангови тестове. BUN, азот в урея в кръвта
Коригирано съотношение на риск за съставен бъбречен изход според нивата на BUN. Плътната линия показва съотношението на опасност, а пунктираните линии - 95% доверителен интервал. BUN, азот в урея в кръвта
Фигура 4 обобщава коригирани HRs според подгрупи, стратифицирани по демографски и клинични характеристики. При всички субекти всяко повишаване на нивото на BUN с 10 mg/dL е свързано с повишен риск от неблагоприятни бъбречни композитни резултати (HR, 1,23; 95% CI, 1,04–1,45). При мъжете по-високите нива на BUN са свързани със значително увеличаване на риска от неблагоприятни бъбречни композитни резултати. При пациенти с по-висок eGFR, по-нисък серумен албумин и по-високо ниво на протеинурия, рискът от лоши бъбречни резултати значително се увеличава с увеличаване на нивото на BUN. В допълнение, при пациенти, приемащи диуретици, тъй като нивото на BUN се е увеличило, е установено значително увеличение на риска от лош бъбречен изход. Няма значителни взаимодействия за бъбречните резултати, с изключение на употребата на диуретици (P = 0,02), наблюдавани между нивата на BUN и други изходни клинични характеристики (P за взаимодействие, 0,06–0,88).
Коригирани съотношения на риск и 95% доверителни интервали за съставния бъбречен изход за всеки 10 mg/dL увеличение на BUN в подгрупи, стратифицирани според изходните характеристики. Коригирано за същите ковариати като Модел 3 в Таблица 2. ESRD, краен стадий на бъбречно заболяване; BUN, азот в урея в кръвта; eGFR, изчислена скорост на гломерулна филтрация
Ние също така изследвахме връзката на нивата на BUN и cSosm с прогресията към ESRD (бъбречни събития, н = 173) (Таблица 3). В напълно коригирания модел (Модел 3), в сравнение с първия квартил на BUN, четвъртият квартил на BUN има значително повишен риск от съставния резултат, докато по-високите квартили на cSosm не показват значително увеличение на риска за лоши резултати.
Оценена е колинеарността между променливите, използвани в Модел 3, както е показано в Допълнителен файл 1: Таблица S1 (за съставни резултати) и Допълнителен файл 2: Таблица S2 (само за ERSD). Всички променливи имаха ниски VIF стойности. Освен това, Допълнителен файл 3: Таблица S3 (за съставни резултати) и Допълнителен файл 4: Таблица S4 (само за ESRD) показват коригираните HRs за резултатите след премахването на една променлива наведнъж. И в двата анализа отстраняването на три променливи (дневна протеинурия, серумен албумин и хемоглобин) не доведе до значителна връзка между по-високите нива на cSosm и резултатите. Значителна асоциация беше показана за първи път чрез премахването на четвъртата променлива (eGFR).
Анализ на чувствителността
За да оценим стабилността на констатациите, показани в Таблица 2, направихме анализ на чувствителността и тези резултати са показани в Таблица 4. В многопроменлив анализ ние включихме серумен креатинин като ковариат, вместо eGFR. По-високите BUN квартили, но не cSosm квартилите, са независимо свързани с неблагоприятни бъбречни композитни резултати. Тези констатации са подобни на тези, показани в таблица 2.
Дискусия
Настоящото проучване демонстрира, че по-високите нива на BUN са свързани с неблагоприятни бъбречни резултати, независимо от eGFR при пациенти с умерена до тежка ХБН. Неотдавнашно проучване съобщи, че както BUN, така и cSosm са независими рискови фактори за ХБН при пациенти със запазена бъбречна функция [11]. В настоящото проучване обаче, мултипроменлив анализ на Cox (Модел 3) не показва значителна връзка между cSosm и лоши бъбречни резултати. Тези открития предполагат, че абсолютната BUN, а не серумната осмолалност, може да има предсказваща стойност за прогресията на бъбречното заболяване. Обратно, в нашата кохорта, по-високите нива на BUN са били значително свързани с лоши резултати в по-високата, но не и по-ниската група на eGFR, въпреки че не е имало значимо взаимодействие за бъбречните резултати между нивата на BUN и eGFR, както е показано на фиг. че въздействието на нивото на BUN върху прогресията на бъбречните заболявания е по-силно в по-ранните етапи на ХБН.
Освен това беше извършен анализ на чувствителността, както е показано в таблица 4. Резултатите от този анализ бяха подобни на тези, наблюдавани в таблица 2. Тези открития потвърдиха стабилността на нашите резултати. По този начин нивата на BUN могат да бъдат свързани с бъбречни резултати, независимо от бъбречната функция.
Ограничения на проучването
Заключения
По-високите нива на BUN са идентифицирани като рисков фактор за прогресия на бъбречното заболяване при пациенти с умерена до тежка ХБН, независимо от eGFR. Въпреки че нивата на cSosm се увеличават заедно с нивата на BUN, те не са свързани независимо с лош резултат. Освен това, въз основа на анализа на чувствителността, също се предполага, че нивата на BUN са свързани с неблагоприятни бъбречни резултати, независимо от бъбречната функция. Нашите открития предполагат, че измерването на нивата на BUN може да бъде полезно за прогнозиране на бъбречни резултати.
- BUN - клиничен азот на урея в кръвта (BUN), серум
- Азот в кръвта - общ преглед на ScienceDirect теми
- Остра бъбречна дисфункция без отхвърляне ”се свързва с лоши бъбречни резултати след 2 години след
- BUN Нива - Тестове за азот в кръвта на д-р
- Резултати от теста за азот в кръвта (BUN) и проследяване на клиниката в Кливланд