Субекти
Резюме
Ключови точки
Интересът към диетите за изключване за лечение на синдром на раздразнените черва (IBS) се възражда.
Рандомизирани контролирани проучвания (RCT) показват, че някои диети - като диета с ниско съдържание на ферментируеми олигозахариди, дизахариди, монозахариди и полиоли или диета без глутен - могат да намалят симптомите на IBS.
Диетата може да има ефект върху симптомите на IBS чрез различни механизми, като директен ефект на храната, промяна на чревната микробиота и имунно активиране.
RCT, оценяващи диети за изключване, имат уникални проблеми, свързани с избора на контроли, което прави тълкуването на резултатите предизвикателно.
Бъдещите РКИ трябва да събират данни, които дават механистична представа за това как диетата може да окаже въздействие върху симптомите.
Въведение
Ancel Keys направи своите наблюдения върху наситените мазнини и исхемичната болест на сърцето в епоха преди медицина, основана на доказателства. Неговите наблюдения се основават на убедителни механистични данни, подкрепени от наблюдателни проучвания 9. Тъй като бяха проведени строги проучвания, които се придържат към стандартите за медицина, основани на доказателства, ние осъзнахме, че ролята на мазнините като рисков фактор за сърдечни заболявания е по-сложна от първоначално предложеното 10 и че простото премахване на наситените мазнини от вашата диета няма да доведе до предотвратяват исхемична болест на сърцето; освен това, заместването на въглехидрати с мазнини може дори да бъде вредно 10. Следователно, принципите на медицината, основани на доказателства, трябва да се прилагат, когато се изучава ролята на диетите за изключване като лечение на IBS. В този преглед ние обсъждаме механизмите, които могат да доведат до симптоми при IBS и обсъждаме различни подходи за това как диетите за изключване могат да бъдат оценени в рандомизирани контролирани проучвания (RCT).
Механизми за диета, причиняващи симптоми на IBS
Директен ефект на храната в лумена на червата
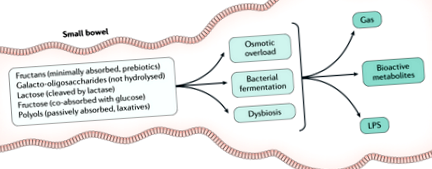
Съществуват множество механизми, чрез които храната може да предизвика симптоми на IBS (Фиг. 1).
Ферментиращите олигозахариди, дизахариди, монозахариди и полиоли (FODMAP) могат да причинят симптоми на синдром на раздразненото черво (IBS) чрез осмотично претоварване, бактериална ферментация или дисбиоза. LPS, липополизахарид.
Интересът към това как храните могат да имат пряко въздействие в лумена на червата, за да предизвикат симптоми, се стимулира от описанието на предимствата на диетата с ниско съдържание на FODMAP. Тази изключваща диета включва ограничаване на много често срещани хранителни продукти, като някои от тях са добре известни, че предизвикват стомашно-чревни симптоми, като лактоза, фруктоза и полиоли.
Обичайните олигозахариди включват фруктани (като инулин, фрукто-олигозахариди и олигофруктоза), които са въглехидрати с къса верига, присъстващи в зърнени култури и зеленчуци, които се абсорбират минимално в човешките черва 11. Освен това галакто-олигозахаридите - късоверижни въглехидрати, присъстващи в бобовите растения, фасула и лещата - не се хидролизират в човешкото черво поради липсата на ензим α-галактозидаза 12. Тези молекули имат осмотичен ефект, увеличавайки натоварването на течността към стомашно-чревния тракт (въпреки че степента, до която се проявява този ефект, зависи от дължината на веригата) 13 и увеличавайки разтягането на червата. Тези продукти също водят до бактериална ферментация с повишено образуване на газове в чревния тракт, особено в дебелото черво 14 .
Като цяло тези резултати предполагат, че осмотичните ефекти и бактериалната ферментация се появяват след поглъщане на определени въглехидрати при всички индивиди, но степента и възприемането на тези ефекти се увеличават при пациенти с IBS, вероятно поради висцералната свръхчувствителност - един от най-широко приеманите патофизиологични фактори при IBS и други функционални стомашно-чревни нарушения 26 .
Някои пациенти обаче действително могат да се възползват от ферментируема пребиотична диета, тъй като рандомизираното проучване на 27 пациенти с функционални стомашно-чревни разстройства показва, че стомашно-чревните симптоми се подобряват в подобна степен при диета с ниско съдържание на FODMAP или при лечение с пребиотични фибри 27 Освен това растителните храни могат да предизвикат стомашно-чревни симптоми по механизми, различни от осмотично натоварване или бактериална ферментация. Тези механизми могат да включват стимулиране на чревната секреция чрез химикали (като лактуцини в маруля и реин в ревен), предназначени да възпират тревопасните животни 28. В това отношение предизвикателството с маруля и ревен увеличава съдържанието на вода в тънките черва (както се оценява чрез ЯМР) и предизвиква симптоми на червата при здрави доброволци 28 .
Ефект върху чревната микробиота
Систематичен преглед на проучванията за контрол на случаите предполага, че съществуват разлики между чревната микробиота на пациенти с IBS и здрави индивиди като контроли 29. Най-последователната констатация е намаляване на изобилието на Bifidobacterium и увеличаване на Бактероиди и видове Enterobacteriaceae при пациенти с IBS в сравнение със здрави контроли. Ефектът от разнообразието на чревната микробиота при IBS е неясен, като повечето проучвания не предоставят тази информация; тези проучвания, които докладват за разнообразието, са приблизително еднакво разделени между липса на разлика и намаляване на разнообразието при пациенти с IBS в сравнение със здрави индивиди като контроли 29 .
Диета и възпаление
Храната е ясно отговорна за възпалението като част от IgE-медиирана хранителна алергия 38; в единия край на спектъра на имунологичния отговор е анафилаксия, но по-заглушен отговор може да доведе до стомашно-чревни симптоми, включително IBS. Както беше посочено по-рано, RCT на елиминиране на храни въз основа на IgG и IgE-медиирано алергично тестване даде разочароващи резултати 5, но тези констатации може отчасти да се отнасят до неточността на тестовете, използвани за хранителна алергия 39 .
Основната нарушаваща група храни, довела до това, че пациентите с IBS са CLE-положителни, е пшеницата, като 46 от 76 (61%) от тези пациенти реагират на пшеница 40. Това откритие е в съответствие с наблюдението, че значителна част от пациентите с IBS възприемат, че техните симптоми се предизвикват от ястия, съдържащи пшеница или глутен 41. Въпреки че е ясно доказано, че глутенът е ключовият хранителен фактор при цьолиакия, неговата роля в генерирането на симптоми и основните механизми при пациенти с IBS без цьолиакия е слабо разбрана. Чревната пропускливост е променена при подгрупа пациенти с IBS, които са се подобрили след безглутенова диета 42,43, а друго проучване предполага, че пациентите с IBS, които имат имунна реактивност към глутен или HLA-DQ2, са по-склонни да се възползват от глутен -безплатна диета 44. Предклинични проучвания показват, че глутеновите и неглутеновите протеини, присъстващи в пшеницата, като инхибитори на α-амилаза трипсин (ATI), индуцират вродени имунни отговори и повишават чревната пропускливост, холинергичното активиране и разстройството на червата 45,46,47 .
Две проучвания от 2019 г. предполагат, че чревната микробиота може да участва в процесите, свързани с чувствителността към глутен или пшеница. По-конкретно, някои тънки чревни бактерии, като Псевдомонада, произвеждат еластази, които имат протеолитична активност срещу глутен, което допринася за цялостното разграждане на глутена. Тази активност на еластазата обаче е свързана и с независима от глутен, активирана с протеаза рецептор 2 (PAR2) -урегулиране на възпалителните пътища 48. При мишки, експресиращи гени, свързани с цьолиакия (HLA-DQ8), бактериалната еластаза се синергизира с глутен, за да предизвика тежко възпаление 48. По подобен начин ATIs индуцират вроден имунен отговор чрез активиране на Toll-like receptor 4 (TLR4) път, причинявайки бариерна дисфункция при липса на увреждане на лигавицата 49. Едновременното приложение на ATI с глутен, синергизира и усилва неговите имуностимулиращи ефекти, променяйки стомашно-чревния транзит и чревната пропускливост. Интересното е, че ATI са влошени от Лактобацилус, което намалява неговите възпалителни ефекти 49. Тези ефекти са обобщени на фиг. 2. Уместността на тези интригуващи открития за симптоматиката на IBS и чувствителността към глутен сега трябва да бъде демонстрирана в последващи проучвания при хора.
Някои тънки чревни бактерии, като Псевдомонада, произвеждат еластази, които имат протеолитична активност срещу глутен, което допринася за цялостното разграждане на глутена. Тази активност на еластазата обаче се свързва и с независима от глутен, активирана с протеаза рецептор 2 (PAR2), медиирана регулиране на възпалителните пътища. По подобен начин инхибиторите на амилаза триптаза (ATI; протеини, открити в пшеницата) индуцират вроден имунен отговор чрез активиране на пътя, подобен на Toll-подобен рецептор 4 (TLR4). Интересното е, че ATI се влошават от Лактобацилус. IBS, синдром на раздразненото черво.
- Диети, след които теглото не се връща преглед, хранителни характеристики, отзиви 🙎🏻 ☝🏾 🤞
- Прекратяване на пристрастията към теглото и стигмата на затлъстяването Природни отзиви Ендокринология
- FSH антитяло предотвратява затлъстяването и загубата на кост Ендокринология
- Контрацептивите, упражненията и диетата - и трите са необходими в PCOS Nature Reviews Endocrinology
- Оценка и управление на свързаните със затлъстяването безалкохолни мастни чернодробни заболявания Nature Reviews