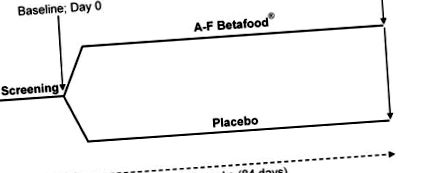
Схематично представяне на дизайна на клиничното изпитване. Петдесет участници бяха включени в 12-седмично двойно-сляпо, рандомизирано, плацебо-контролирано, двураменно паралелно проучване. Всички участници, включени в проучването, са завършили всички оценки, свързани с проучването, на изходно ниво (Ден 0) и 12 седмици след добавянето.
Разположение на участниците. От 121-те проверени участници, 50 допустими участници бяха записани и бяха рандомизирани да получават или A-F Betafood ®, или плацебо при 25 участника на група. Осем участници, всички ранни прекратявания, не бяха включени в популацията PP. „Оттеглено от QI“ се отнася до участник, който е отстранен от проучването от квалифициран изследовател за нарушение на протокола от изследването. „Оттеглено съгласие“ се отнася до участник, който се оттегля (или прекратява) от проучването по лични причини. ITT, намерение за лечение; PP, на протокол.
Чернодробна функция и възпалителни маркери в популацията на протокол на изходно ниво и седмица 12 след добавяне с A-F Betafood ® или плацебо (n = 42). (a) AST, (b) ALT, (c) GGT и (d) hs-CRP. Средно ± SD. AST, аспартат аминотрансфераза; ALT, аланин аминотрансфераза; GGT, гама-глутамилтрансфераза; hs-CRP, високочувствителен С-реактивен протеин.
Липиден профил в популацията на протокола на изходно ниво и седмица 12 след добавяне с A-F Betafood ® или плацебо (n = 42). (a) Общ холестерол, (b) LDL-холестерол (c) HDL-холестерол и (d) нива на триглицериди. Средно ± SD. LDL, липопротеин с ниска плътност; HDL, липопротеин с висока плътност.
Резюме
Схематично представяне на дизайна на клиничното изпитване. Петдесет участници бяха включени в 12-седмично двойно-сляпо, рандомизирано, плацебо-контролирано, двураменно паралелно проучване. Всички участници, включени в проучването, са завършили всички оценки, свързани с проучването, на изходно ниво (Ден 0) и 12 седмици след добавянето.
Разположение на участниците. От 121-те проверени участници, 50 допустими участници бяха записани и бяха рандомизирани да получават или A-F Betafood ®, или плацебо при 25 участника на група. Осем участници, всички ранни прекратявания, не бяха включени в популацията PP. „Оттеглено от QI“ се отнася до участник, който е отстранен от проучването от квалифицирания следовател за нарушение на протокола от изследването. „Оттеглено съгласие“ се отнася до участник, който се оттегля (или прекратява) от проучването по лични причини. ITT, намерение за лечение; PP, на протокол.
Чернодробна функция и възпалителни маркери в популацията на протокол на изходно ниво и седмица 12 след добавяне с A-F Betafood ® или плацебо (n = 42). (a) AST, (b) ALT, (c) GGT и (d) hs-CRP. Средно ± SD. AST, аспартат аминотрансфераза; ALT, аланин аминотрансфераза; GGT, гама-глутамилтрансфераза; hs-CRP, високочувствителен С-реактивен протеин.
Липиден профил в популацията на протокола на изходно ниво и седмица 12 след добавяне с A-F Betafood ® или плацебо (n = 42). (a) Общ холестерол, (b) LDL-холестерол (c) HDL-холестерол и (d) нива на триглицериди. Средно ± SD. LDL, липопротеин с ниска плътност; HDL, липопротеин с висока плътност.
- Пълнотекстовият екстракт от зелено кафе с хранителни вещества подобрява кардиометаболитните параметри и модулира червата
- Безплатни пълноценни хранителни натоварвания с диетични киселини и резултати от психичното здраве при деца и юноши
- Безплатни пълноценни отклонения на хранителните вещества в диетата на китайски възрастни от китайската пагода за храна 2016 и
- Без хранителни вещества, стареене в цял текст и ограничаване на калориите модулират профила на метилиране на ДНК на
- Безплатни пълноценни диети и хранителен статус на монголски възрастни