Субекти
Резюме
Предистория/цели
Понастоящем метформинът извън етикета се използва често за лечение на затлъстяване при юноши. Въпреки това, проучванията за дългосрочно лечение с метформин при юноши със затлъстяване са оскъдни. Следователно е проведено 18-месечно отворено удължено проучване след 18-месечно рандомизирано плацебо-контролирано проучване (RCT) за ефикасността, безопасността и поносимостта на метформин при юноши със затлъстяване и инсулинова резистентност.
Субекти/методи
След приключване на RCT, метформин беше предложен на всички участници със стандартно отклонение за индекс на телесна маса (BMI-sds)> 2,3 и оценка на модела на хомеостазата за инсулинова резистентност (HOMA-IR) ≥ 3,4. Крайните точки са промяна в ИТМ и HOMA-IR.
Резултати
Като цяло 31/42 участници са завършили разширеното проучване (74% момичета, средна възраст 14,8 (11,6 - 17,9), ИТМ 31,2 (22,3 - 45,1), HOMA-IR 3,4 (0,2 - 8,8)). В началото 22/42 (52,4%) участници са имали право на метформин, от които 13 (59,0%) са се съгласили с лечението. При участниците, продължили лечението с метформин, се наблюдава повишение на ИТМ (+2,2 (+0,2 до +9,0)) и HOMA-IR (+13,7 (+1,6 до +48,3)). При наивни участници с метформин BMI се стабилизира след първоначално намаляване (+0,5 (-2,1 до +5,1)). За HOMA-IR се наблюдава намаление (-1,1 (-4,6 до +1,4)).
Заключение
Докато лечението с метформин при участници, които не са получавали метформин, изглежда води до първоначално намаляване на ИТМ и HOMA-IR, няма доказателства за устойчив ефект след продължителна употреба при юноши. Ограниченото съответствие и/или недостатъчната доза могат да обяснят разликите в дългосрочните ефекти между юноши и възрастни.
Въведение
Затлъстяването е основен здравословен проблем в световен мащаб 1, с приблизително разпространение при деца и юноши до 5,4% през 2025 г. 2. Затлъстяването е свързано с усложнения като метаболитен синдром, захарен диабет тип 2 (T2DM), сърдечно-съдови заболявания и чернодробна стеатоза 2,3. Инсулиновата резистентност (IR) има важна роля за развитието на усложнения, тъй като е предшественик на нарушен глюкозен толеранс 4,5, признат като независим рисков фактор за сърдечно-съдови заболявания 4 и част от метаболитния синдром 5,6. Тъй като затлъстяването преминава към по-млада възраст, свързаните с това усложнения ще се проявят по време на детството 3. Мултидисциплинарната интервенция за начина на живот е крайъгълният камък на лечението (за детското) затлъстяване 7. Въпреки това, той е свързан само с незначителен дългосрочен ефект поради висок процент на отпадане и ограничена мотивация, наблюдавана в почти всички проучвания 7,8 .
През последните години проучванията се фокусират върху допълнителни терапии на върха на интервенция в начина на живот, като фармакотерапия и бариатрична хирургия 7. Бариатричната хирургия, въпреки че все още не се счита за стандартна терапия, се препоръчва да бъде ефективна при постпубертални юноши с устойчиво на терапия затлъстяване 9,10,11. Що се отнася до фармакотерапията, орлистат и метформин са двете най-изследвани лекарства 7,12. Орлистат, инхибитор на липазата, е единственото одобрено лекарство за лечение на детско затлъстяване. Полезността в ежедневната клинична практика обаче е ограничена поради често съобщаваните нежелани ефекти върху стомашно-чревния тракт и само умерено намаляване на теглото без благоприятни ефекти върху кардиометаболитно усложнение 7,12,13,14 .
Метформин, перорален антихипергликемичен агент, одобрен за лечение на T2DM от 10-годишна възраст нататък, е във фокуса на многобройни проучвания като допълнителна терапия при лечението на детско затлъстяване 15,16,17,18,19,20,21, 22,23,24. Той е свързан с малки, но значителни намаления в теглото и като цяло се понася добре 15,16,17,18,19,20,21,22,23,24. Въпреки че литературата е непоследователна, благоприятните ефекти на метформин върху кардиометаболитни усложнения са описани 15,16,17,18,21. Поради това се предполага, че метформин може да има потенциал за забавяне и/или предотвратяване на усложнения от (педиатрично) затлъстяване 25. Проучванията за ефикасността на метформин при юноши обаче са предимно ограничени до период на проследяване от 6 месеца 15,16,17,18,19,20. Проведени са само няколко проучвания с по-дълъг период на проследяване с максимум до 24 месеца 21,22,23,24. Следователно не е ясно дали продължителното лечение с метформин при юноши ще доведе до дълготрайни положителни ефекти върху теглото.
Следователно целта на това проучване е да докладва за резултатите от 18-месечно отворено удължено проучване след рандомизирано плацебо-контролирано проучване (RCT) за 18-месечно лечение с метформин или плацебо по отношение на ефикасността, безопасността и поносимостта на метформин лечение при юноши със затлъстяване и IR 22. Освен това се оценява развитието на свързаните със затлъстяването метаболитни и сърдечно-съдови усложнения.
Материали и методи
Тъй като протоколът за изпитване и резултатите от 18-месечния RCT са докладвани другаде 22,26, тук е представено само кратко описание на дизайна на изследването.
Дизайн на проучването и участници
Следователно, в това отворено разширено проучване имаше четири проучвания в зависимост от употребата на метформин или плацебо по време на RCT и лечението с метформин в това проучване. Участниците с метформин по време на отвореното разширено проучване са били означени с MM или PM, а участниците без метформин - с MP или PP. Първата буква представлява лечението по време на RCT (M за метформин, P за плацебо), втората буква лечението по време на отвореното проучване за разширение.
Измерванията бяха извършени в детските амбулатории или дневните отделения на участващите болници. Всички участници имаха три планирани посещения в болница и три телефонни разговора, с изключение на потребителите на метформин, които имаха допълнителни посещения вместо телефонни разговори, за да наблюдават безопасността и поносимостта. Тестовете за фитнес бяха проведени в амбулаторията по физикална терапия на болница „Свети Антоний“ и в Спортния медицински център на болница „Йерун Бош“. За разлика от RCT не се предлага специална контролирана програма за физическо обучение. Подобно на RCT, участниците в терапията с метформин получават таблетки с метформин 500 mg с незабавно освобождаване при нарастващ режим на дозиране, с максимум две таблетки два пъти дневно през четвъртата седмица. В случай на стомашно-чревни оплаквания дозата е намалена до последната добре поносима доза. След изчезване на симптомите дозата се увеличава до максимално допустимата доза 26. За разлика от RCT, не са извършени преброявания на хапчета.
Резултати
Крайните точки са промяна в BMI (ΔBMI) и промяна в HOMA-IR (ΔHOMA-IR). Освен това бяха оценени безопасността и поносимостта на метформин. В допълнение бяха оценени промените в HbA1c, процентът на телесните мазнини, качеството на живот и физическата годност. И накрая, беше оценен процентът на свързаните със затлъстяването метаболитни и сърдечно-съдови усложнения.
ИТМ се изчислява като тегло (kg)/(височина (m)) 2. Съответният ИТМ, адаптиран към възрастта и пола, BMI-sds е изчислен с помощта на калкулатора за растеж на TNO за професионалисти 28. IR се изчислява, като се използва HOMA-IR (плазмена глюкоза на гладно (mmol/l) × плазмен инсулин на гладно (mU/l))/22,5)) 29 и се определя като HOMA-IR ≥ 3,4 30 .
Безопасността е отчетена като брой случаи с чернодробни и/или бъбречни функционални тестове, надвишаващи границите на безопасност (ALAT> 69U/l (момичета) или> 78 U/l (момчета), скорост на гломерулна филтрация (GFR) 26 .
Дефиниции на метаболитни усложнения: нарушен глюкозен толеранс се определя като нарушена глюкоза на гладно (IFG) ≥ 5.6–31. Високият триглицерид се определя като ≥ 1,7 mmol/l, а ниският липопротеин с висока плътност (HDL) като 31. Високото систолично кръвно налягане се определя като систолично и/или диастолично кръвно налягане ≥ 95-и процентил за възрастовия пол и височина 32. Метаболитният синдром се дефинира като наличие на поне 3 от следните критерии: обиколка на талията ≥ 95-ия процентил за възрастта, систолично и/или диастолично кръвно налягане ≥ 95-ия процентил за възрастта, високи триглицериди, нисък HDL и нарушен глюкозен толеранс 6. Микроваскуларните усложнения се определят като урина албумин 30-300 mg/l в проба рано утринна урина 31. Сърдечно-съдовите усложнения се оценяват по артериалната скованост. Артериалната скованост беше оценена неинвазивно чрез измерване на скоростта на пулсовата вълна (PWV) и индекса за увеличаване (AIX), използвайки SphygmoCor (Модел SCOR-Px, Версия на софтуера, 7.01; AtCor Medical Pvt. Ltd, Сидни, Австралия).
Антропометричните и лабораторните параметри се оценяват на всеки 6 месеца. Процентът на телесните мазнини, IWQOL-деца, тест за физическа годност и артериална скованост бяха оценени едва в края на разширеното проучване, поради което за сравнение бяха използвани данни, получени в края на RCT.
Статистически анализ
Статистическият анализ беше извършен с помощта на IBM SPSS Statistics, версия 24 (IBM SPSS Statistics, Чикаго, IL, САЩ). Тъй като броят на участниците в едно изследвано рамо е малък, резултатите обаче са представени описателно стр-стойностите са изобразени в таблиците. Поради малкия размер на извадката се приема, че параметрите не са нормално разпределени и поради това непрекъснатите данни се отчитат като медиана с обхват, а категоричните данни като честоти с процент. Тестът на Крускал – Уолис е използван за сравняване на изходните характеристики на изследваните групи от непрекъснати данни и χ 2 тест или точен тест на Fisher за категорични променливи. Параметрите на резултата във времеви моменти т = 0 и т = 18 от откритото удължено проучване са сравнени за изследваните групи, използвайки теста на Kruskal – Wallis. An α-ниво от 5% се счита за значимо за всички статистически тестове.
Резултати
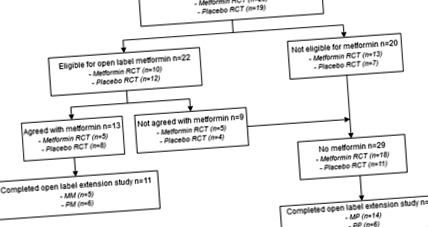
Фигура 1 показва блок-схемата на изследваната популация. Всички 42 участници, завършили RCT, бяха включени в откритото разширено проучване. В началото на проучването 22/42 (52%) участници са имали право на метформин, от които 13 (59%) са съгласни с лечението. Останалите участници 29 (69%) не са използвали метформин 5 (17,2%) без затлъстяване, 15 (51,7%) без IR и 9 (31,0%) без съгласие за лечение). Единадесет участници бяха загубени за проследяване по време на проучването (т.е. 4MP, 5PP, 2PM); следователно бяха анализирани общо 31 участници.
ММ метформин по време на RCT и разширено проучване, PM плацебо по време на RCT и метформин по време на разширено проучване, MP метформин по време на RCT и плацебо по време на разширено проучване, PP плацебо по време на RCT и разширено проучване
Базови характеристики
Базовите характеристики на участниците, завършили откритото разширено проучване, са представени в Таблица 1. Наблюдава се широк диапазон в демографските и лабораторни данни между всички участници и участниците в обхвата на изследването. От участниците 84% са били със затлъстяване, а 45% са имали IR в началото на откритото разширено проучване. Проучванията се различават значително за HOMA-IR, но не и за BMI или BMI-sds. Участниците са били предимно жени и са в пубертетен (Tanner 2-4) или постпубертален (Tanner 5) етапи. Наблюдаваните етапи на Tanner се различават значително между изследваните групи.
Ефект върху ИТМ и HOMA-IR
Фигура 2 показва прогресията на ИТМ и HOMA-IR по време на откритото разширено проучване, стратифицирано от изследваната група. В подгрупата MM се наблюдава общо увеличение на ИТМ от началото на отвореното проучване за разширение. В подгрупата PM се наблюдава първоначално намаляване на ИТМ и след това увеличение. В подгрупата MP се забелязва стабилизиране на ИТМ през първите 6 месеца и след това увеличение. В подгрупата РР се наблюдава първоначално увеличение през първите 6 месеца и след това стабилизиране на ИТМ. За HOMA-IR се наблюдава рязко увеличение в подгрупата MM. В останалите подгрупи се наблюдава вълнообразен модел. Преглед на абсолютните стойности, както и промените в BMI, HOMA-IR и BMI-sds по време на проучването за разширено отворено етикетиране, RCT и RCT и отвореното проучване за разширение заедно са представени в допълнителна таблица 1 и допълнителна фигура. 1.
Среден ИТМ (а); медиана HOMA-IR (б). ММ метформин по време на RCT и разширено проучване, PM плацебо по време на RCT и метформин по време на разширено проучване, PP плацебо по време на RCT и разширено проучване, MP метформин по време на RCT и плацебо по време на разширеното проучване
Безопасност и поносимост
Няма съобщения за сериозни нежелани реакции. Що се отнася до измерванията на безопасността, чернодробна дисфункция, определена като ALAT над границите на безопасност, се наблюдава при 2 участници (1 MM и 1 MP). Нисък витамин В12 е наблюдаван при 2 участници (1 MM и 1 MP). Не се наблюдава бъбречно увреждане. Метформин обикновено се понася добре. Двама участници съобщават за гадене и четири диарии. Двама участници (и двамата PM) прекратиха проучването поради странични ефекти (стомашно-чревни симптоми).
Други резултати
Фигура 3 показва средните промени на HbA1c, процент на телесни мазнини, маса на мазнини и маса без мазнини. Увеличение на HbA1c се наблюдава в подгрупата MM, докато намалява в останалите подгрупи. За процента телесни мазнини се наблюдава стабилизация в подгрупата PM и PP, докато подгрупата MM и MP показва увеличение. Мастната маса се увеличава в подгрупата ММ и РР, където в подгрупата МР и ПМ се наблюдава средно намаление в широк диапазон. За маса без мазнини се наблюдава увеличение във всички подгрупи. Преглед на абсолютните стойности, както и промените в HbA1c, процента на телесните мазнини, масата на мазнините и обезмаслената маса по време на отвореното проучване за удължаване и RCT и проучването за разширено отворено етикетиране заедно са представени в допълнителна таблица 1.
ММ метформин по време на RCT и разширено проучване, PM плацебо по време на RCT и метформин по време на разширено проучване, PP плацебо по време на RCT и разширено проучване, MP метформин по време на RCT и плацебо по време на разширеното проучване. Пунктираната линия не представлява промяна
Надежден анализ по отношение на промяната във физическата форма и качеството на живот не може да бъде извършен, тъй като само няколко участници са провели фитнес теста (н = 11) и/или предадени в оценката на IWQOL (н = 19) в края на RCT и в края на отвореното проучване за разширение.
Усложнения, свързани със затлъстяването
В края на откритото разширено проучване се наблюдава нарушен глюкозен толеранс при 8/31 (26%) участници. Един участник разви T2DM (потвърден с допълнителен орален тест за глюкозен толеранс), 3 IFG и 4 IGT. Високи триглицериди са наблюдавани при 7/31 (23%) участници, а ниски HDL при 11/31 (36%). Освен това 2 участници развиха високо систолично и/или диастолично кръвно налягане. Микроалбуминурия се наблюдава при 1/31 (3%) участници. В допълнение, в цялата популация нарастване на съдовата скованост, измерено с AIx (-3,1 срещу 2,3; стр = 0,04), не се наблюдава значителна разлика за PWV (4,2 срещу 4,6; стр = 0,10). Преглед на прогресията на свързаните със затлъстяването метаболитни и сърдечно-съдови усложнения по време на RCT и открито удължено проучване е показан в Таблица 2.
Дискусия
В това проучване подрастващите участваха в 18-месечно отворено удължено проучване след 18-месечно двойно заслепено RCT относно дългосрочната ефикасност, безопасност и поносимост на метформин при юноши със затлъстяване и IR 22. В началото на отвореното разширено проучване на участниците беше предложен метформин в зависимост от ИТМ и HOMA-IR; следователно са създадени 4 групи от проучвания, в които участниците са използвали съответно 18 месеца, 36 месеца или изобщо не са имали метформин.
Високият отпадане е в съответствие с други проучвания за затлъстяване, независимо от продължителността на проучването 15,19,21,23,24, и също се наблюдава по време на рутинни клинични грижи в детски (затлъстяване) амбулаторни клиники. Тъй като проучванията при популации със затлъстяване са ограничени от броя на включванията и високото отпадане, се препоръчва за по-малко рестриктивните критерии за включване/изключване на RCT да се използват в комбинация с формирането на изследователски мрежи за постигане на адекватни номера на включване 42. Когато се обмислят проучвания при педиатрични популации със затлъстяване, е под въпрос дали те трябва да се извършват в RCT или е по-практично да се извършват проучвания в ежедневна клинична обстановка, използвайки стандартизиран протокол.
Заключение
Докато лечението с метформин при немедицински участници с метформин изглежда води до първоначално намаляване на ИТМ и HOMA-IR, няма доказателства за устойчив ефект след продължителна употреба при юноши. Ограниченото съответствие и/или недостатъчната доза могат да обяснят разликите в дългосрочните ефекти между юноши и възрастни.
- Дългосрочна безопасност, поносимост и загуба на тегло, свързани с метформин при диабет
- Лечение на метформин (глюкофаж) - лечение на диабет тип 2
- Индуцирана от инфузия на липиди и инсулин скелетна мускулатура инсулинова резистентност се дължи на метаболизма
- Lorcaserin за лечение на затлъстяване По-отблизо неговите странични ефекти Отворено сърце
- Инсулинова резистентност, дислипидемия и сърдечно-съдови заболявания при диабет