Резюме
Заден план
Синдромът на поликистозните яйчници (PCOS) е най-често срещаното ендокринно разстройство при жените по време на репродуктивна възраст. Характеризира се клинично с олиго-овулация или ановулация, хипер-андрогенизъм и наличие на поликистозни яйчници. Той е свързан с повишено разпространение на метаболитен синдром, сърдечно-съдови заболявания и диабет тип 2. Появата на СПКЯ е свързана с няколко наследствени и екологични фактора, но инсулиновата резистентност играе ключова патогенетична роля. Ние се опитахме да проучим ефектите на кетогенната диета (KD) върху жени в детеродна възраст с диагноза PCOS.
Методи
Четиринадесет жени с наднормено тегло с диагноза PCOS са били подложени на кетогенна средиземноморска диета с фьоекстракти (KEMEPHY) в продължение на 12 седмици. Промени в телесното тегло, индекса на телесна маса (BMI), мастната телесна маса (FBM), чистата телесна маса (LBM), висцералната мастна тъкан (ДДС), инсулин, глюкоза, HOMA-IR, общ холестерол, липопротеин с ниска плътност (LDL), липопротеин с висока плътност (HDL), триглицериди (TG), общ и свободен тестостерон, лутеинизиращ хормон (LH), фоликулостимулиращ хормон (FSH); дехидроепиандростерон сулфат (DHEA), естрадиол, прогестерон, глобулин, свързващ половите хормони (SHBG) и оценка на Ferriman Gallwey.
Резултати
След 12 седмици антропометричните измервания и състава на тялото разкриха значително намаляване на телесното тегло (- 9,43 kg), BMI (- 3,35), FBM (8,29 kg) и ДДС. Налице е значително, леко намаление на LBM. Наблюдавано е значително намаляване на нивата на глюкоза и инсулин в кръвта, заедно със значително подобрение на HOMA-IR. Наблюдава се значително намаляване на триглицеридите, общия холестерол и LDL заедно с повишаване на нивата на HDL. Съотношението LH/FSH, LH общ и свободен тестостерон и нивата на DHEAS в кръвта също бяха значително намалени. Естрадиолът, прогестеронът и SHBG се повишават. Резултатът на Ferriman Gallwey беше леко, макар и не значително, намален.
Заключения
Нашите резултати показват, че KD може да се разглежда като ценно нефармакологично лечение за СПКЯ. Трябва да се тестват по-дълги периоди на лечение, за да се провери ефектът на KD върху дерматологичните аспекти на СПКЯ.
Пробна регистрация Clinicaltrial.gov, NCT04163120, регистриран на 10 ноември 2019 г., регистриран със задна дата, https://clinicaltrials.gov.
Заден план
Синдромът на поликистозните яйчници (СПКЯ) се счита за най-често срещаното ендокринно разстройство при жените в репродуктивна възраст, като прогнозното разпространение варира от 6 до 15%, в зависимост от използваните диагностични критерии. PCOS всъщност е хетерогенно състояние с променлива фенотипна експресия, което води до значителни противоречия относно диагностичните критерии [1].
Жените с СПКЯ често търсят грижи за менструални смущения (олигоменорея, аменорея, продължително нередовно менструално кървене), клинични прояви на хиперандрогения и безплодие. Хирзутизмът е често срещано клинично представяне на хиперандрогения, срещаща се при до 70% от жените с СПКЯ и се оценява с помощта на системата за оценяване на Ferriman-Gallwey [2].
Интересното е, че излишният прием на въглехидрати и нискостепенното възпаление взаимодействат взаимно с инсулиновата резистентност и хиперандрогенизма, за да подсилят метаболитния фенотип на СПКЯ [9]. Всъщност е известно, че острата хипергликемия увеличава възпалението и оксидативния стрес чрез генериране на реактивни кислородни видове (ROS) [10]. PCOS жените имат особен диетичен модел, характеризиращ се с намалена употреба на екстра върджин зехтин, бобови растения, морски дарове и ядки, по-малко количество сложни въглехидрати, фибри, мононенаситени мастни киселини и по-високи прости въглехидрати, обща мазнина и наситени мастни киселини, в сравнение с нормалните жени. Тези хранителни навици са свързани с неблагоприятен състав на тялото, характеризиращ се с намалена маса без мазнини [11].
Еднозначна терапия за СПКЯ не съществува; особената хетерогенност на тази патология изисква лечението да бъде персонализирано в зависимост от клиничното представяне и нуждите на пациента.
Настоящите насоки като лечение от първа линия за менструални нарушения, акне и хирзутизъм препоръчват хормонални контрацептиви, на всяка възраст. Антиандрогените се препоръчват в случай, че естропрогестините са противопоказани или при наличие на тежък хирзутизъм.
По този начин, целта на настоящото проучване е да се определят ефектите от кетогенна диета (KD) при жени в детеродна възраст с диагноза PCOS. Ние предположихме, че модифицираната KD (диета KEMEPHY) ще доведе до подобряване на телесното тегло, холестерола в плазмата, триглицеридите, хиперинсулинемията и хормоналните резултати.
Материали и методи
Уча дизайн
Това беше 12-седмично проучване с една ръка. Резултатните мерки бяха телесно тегло, ИТМ, FBM, LBM, процент на FBM, процент на LBM, глюкоза, инсулин, HOMA-IR, общ холестерол, HDL, LDL, триглицериди, общ тестостерон, свободен тестостерон, прогестерон, естрадиол, LH, FSH, DHEAS, LH/FSH съотношение, SHBG и Ferriman Gallwey Score. Протоколът за изследване отговаря на всички принципи на декларацията от Хелзинки. Всички пациенти са предоставили писмено информирано съгласие преди началото на проучването. Изследването е одобрено от етичната комисия към Департамента по биомедицински науки (HEC-DSB13/16). Това изпитание е регистрирано със задна дата на Clinicaltrial.gov, NCT04163120, регистрирано на 10 ноември 2019 г., https://clinicaltrials.gov.
Участници
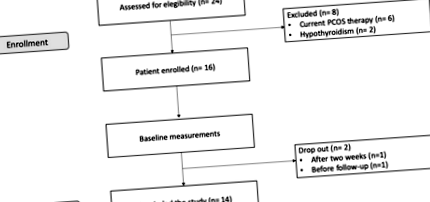
Двадесет и четири жени с наднормено тегло бяха записани чрез публично оповестяване в медицински центрове в територията на Падова и Виченца. Критериите за включване бяха: диагноза на СПКЯ съгласно Ротердамските критерии (поне 2 от 3 между олиго/аменорея или аменорея, клинични признаци на хиперандрогения и поликистозни яйчници, потвърдени с ултразвук [33]), фертилна възраст (18–45 години); ИТМ ≥ 25 kg/m 2, желание за отслабване; приемане да не се използват контрацептиви по време на експерименталния период. Критериите за изключване бяха бременност и кърмене, хормонална терапия и/или инсулинови сенсибилизатори през последните 2 месеца, чернодробни, бъбречни и сърдечни заболявания, локално лечение на хирзутизъм, освен това, според критериите от Ротердам, други етиологии (вродена надбъбречна хиперплазия, андроген секретиращи тумори, Синдром на Кушинг) са изключени. Шест жени бяха изключени за текуща фармакологична терапия на СПКЯ и 2 за диагностициран клиничен хипотиреоидизъм. Един напусна проучването след 2 седмици, а един се оттегли преди проследяването; по този начин 14 субекта (възраст 27,5 ± 8,3 години; височина 168 ± 4,3 см; тегло 81,19 ± 8,44 кг) завършиха проучването (фиг. 1).
Блок-схема на експериментален дизайн. Набиране на пациенти. Допълнителни подробности са докладвани в текста
Преди да започнат диетичния протокол, участниците дойдоха в лабораторията по физиология на храненето и физическите упражнения към Департамента по биомедицински науки на Университета в Падуа за базови измервания. Пациентите са подложени на подробна анамнеза и физически преглед и е извършен плазмен анализ за глюкоза, инсулин, общ холестерол, HDL, LDL, триглицериди (TG), общ тестостерон, свободен тестостерон, прогестерон, естрадиол, LH, FSH, DHEAS и SHBG.
Антропометрични измервания
Телесното тегло беше измерено с точност до 0,1 kg с помощта на електронна везна (Tanita BWB-800 Medical Scales, САЩ), а височината с точност до 1 cm с помощта на монтиран на стената преносим стадиометър Harpenden (Holtain Ltd, UK). Индексът на телесна маса (ИТМ) се изчислява в kg/m 2. Обиколката на талията е измерена като най-малката обиколка между най-ниското ребро и илиачния гребен [34, 35].
Анализ на телесния състав
Съставът на тялото (телесна маса на мазнините FBM, чиста телесна маса LBM и висцерална мастна тъкан) е анализиран чрез Dual X Ray Absorptiometry (DEXA) Hologic Horizon TM QDR RSeries Bedford, Massachusetts, USA. Ежедневните сканирания за контрол на качеството бяха придобити по време на периода на изследване. По време на изпитанието не бяха направени промени в хардуера или софтуера. Субектите бяха сканирани с помощта на стандартни протоколи за позициониране, докато бяха облечени само в леки дрехи. Регионалният анализ на ДДС на багажника и висцералната мастна тъкан беше оценен според анатомични ориентири от същия техник с помощта на компютърни алгоритми (Apex System).
Кръвни изследвания
Взети са кръвни проби от антекубиталната вена и са събрани в BD Vacutainers Tubes (SST TM II Advance, REF 367953). След вземане на кръвни проби пробите се центрофугират (4000 оборота в минута при 4 ° С, като се използва центрофуга J6-MC от Beckman). Така полученият серум се разпределя в аликвотни части и се съхранява при - 80 ° C. Всички проби бяха анализирани в една и съща аналитична сесия за всеки тест, използвайки една и съща партида реактив и с CV интрасайни ® Кръвни β-кетонни тест ленти и Precision Xtra ® [36] (Abbott Laboratories, Illinois 60064-3500, USA), който измерва BHB в кръвта ниво в прясна капилярна цяла кръв от върха на пръста между 0,0 и 8,0 mmol/L. Пункцията е извършена с ланцет Accu-Chek Softclix (Roche, Monza MB, Италия) върху чисти, сухи и топли пръсти. Хирзутизмът се счита за положителен, когато оценката на Ferriman Gallwey е> 8.
Използван е модифициран протокол KD. Диетата KEMEPHY [37,38,39,40,41,42] е средиземноморски евкалорен кетогенен протокол (около 1600/1700 kcal/ден) с използването на някои фитоекстракти. По време на този протокол субектите имат право да ядат без ограничения зелени листни зеленчуци, кръстоцветни, тиквички, краставици и патладжани. Количеството месо, яйца и риба беше ограничено (120 g месо или 20 g риба или 2 яйца) (вж. Таблица 1). Освен това субектите ежедневно консумирали четири хранителни добавки и течни билкови екстракти. Хранителните добавки са формули с високо съдържание на протеини (19 g/порция) и много ниско съдържание на въглехидрати (3,5 g/порция), симулиращи аспекта и вкуса на обикновените храни, богати на въглехидрати, добавени със сухи фитоекстракти [43]. Течните билкови екстракти бяха използвани за тяхната дренираща/тонизираща активност, полезна за намаляване на някои често съобщавани леки странични ефекти на кетогенните диети като запек, главоболие и халитоза. Билковите екстракти са докладвани по-подробно в нашата предишна публикация (Таблица 2) [37].
Статистически анализ
Тестът на Student’s t беше използван за сравняване на параметрите преди и след 12 седмици от KD, използвайки софтуерния пакет GraphPad Prism версия 8.00 за Mac, GraphPad Software, Сан Диего, Калифорния, САЩ. Всички данни са изразени като средно ± стандартно отклонение. Нормалността на данните беше оценена чрез теста на D’Agostino Pearson. Значимостта се отчита при стойност p
Резултати
Антропометричните измервания и състава на тялото разкриват средна загуба на тегло от 9,43 kg (преди 81,19 ± 8,44 kg срещу след 71,76 ± 6,66 kg; p Фиг. 2
Метаболитни биомаркери
Кетонните тела се измерват през ден през първите 6 дни, след това на всеки 6 дни. Средната стойност на BHB е 0,31 ± 0,18 mmol/L през първите 6 дни и 1,77 ± 0,55 от ден 7 до ден 84. Пациентите в началото на проучването са имали HOMA-IR по-висок от 2,5, потвърждавайки инсулиновата резистентност. В края на проучването се наблюдава значително намаляване на глюкозата (преди 5,10 ± 0,25 mmol/L срещу 4,64 ± 0,24 mmol/L; p Таблица 3 Метаболитни биомаркери преди и след 12 седмици KD
Ендокринни биомаркери
Характерното обръщане на съотношението LH/FSH се наблюдава в началото на проучването и изчезва след 12 седмици (преди 2.00 ± 0.30 срещу след 1.15 ± 0.20; p Фиг. 3
Резултатът на Ferriman Gallwey е леко намален, макар и не значително (преди 11,36 ± 1,98 срещу 10,57 ± 1,6).
Дискусия
Дванадесет седмици LCKD подобриха почти всички антропометрични, биохимични и хормонални променливи в група от 14 жени с диагностициран СПКЯ. PCOS, най-често срещаната женска ендокринопатия в репродуктивна възраст, се характеризира със забележителна фенотипна хетерогенност и не само трябва да се разглежда като плодовитост или естетическо разстройство, но състояние, свързано с широк спектър от дългосрочни метаболитни и сърдечно-съдови усложнения. Причините не са известни, но инсулиновата резистентност се счита за важен фактор етиопатогенетичен, който обхваща 70% от пациентите и в повечето случаи е свързан с наднорменото тегло и затлъстяването. Коремното затлъстяване може да бъде свързано с СПКЯ чрез връзка, при която то изпълнява двойната роля на причина и следствие: от една страна, всъщност увеличаването на висцералната мастна тъкан се благоприятства от хиперандрогенията, от друга изглежда, че представлява важен патогенетичен фактор за развитието и прогресирането на СПКЯ при чувствителни жени [44].
Третата група за консенсус на PCOS, спонсорирана от Амстердам ESHRE/ASRM [45], посочва, че по-високият ИТМ е свързан с по-голямо разпространение на менструални нередности, хиперандрогенемия и хирзутизъм. Мастната тъкан всъщност е извънжлезист източник на андрогени и нейното прекомерно количество може да влоши хиперандрогенията. Коремните адипоцити са по-активни като ендокринни клетки, отколкото адипоцитите в долната част на тялото, които определят гиноидното затлъстяване: те са по-чувствителни към катехоламини и по-малко към инсулин, с крайния резултат от хиперинсулинемия, компенсираща с нискостепенно възпаление, променен липид профил, повишено производство на андрогени и ниски нива на SHBG, които като цяло благоприятстват ановулацията. Хиперинсулинемията също влияе върху метаболитната гъвкавост, способността на скелетните мускули да използват алтернативно въглехидрати или липиди в зависимост от наличието на енергийни субстрати [46]. Жените с СПКЯ имат по-намалена метаболитна гъвкавост (оценена чрез промени в дихателния коефициент след инсулинова стимулация), когато имат хиперандрогения, висок ИТМ и инсулинова резистентност [47, 48].
Управлението на СПКЯ е по същество симптоматично: когато плодовитостта не е основният проблем, естропрогестините представляват предпочитаното лечение и често се използват за дълги периоди от време. Пациентите със СПКЯ обаче имат повишен сърдечно-съдов риск и продължителната употреба на орални контрацептиви може да има отрицателни ефекти, така че изборът на естропрогестинов продукт трябва да се направи след индивидуална оценка на сърдечно-съдовия риск при всички пациенти. Не е същото да се използва естропрогестинов продукт при пациент със СПКЯ, който има нормално тегло и има нормален глюкозен толеранс и липиден профил, или при пациент със СПК, който е със затлъстяване и има метаболитен синдром [49]. Освен това пациентите не „лекуват“ с използването на орални контрацептиви и след суспендирането често имат нередности в цикъла, така че повечето от тях са принудени да предприемат терапии за предизвикване на овулация, обикновено с кломифен, както се препоръчва насоки [12]. Следователно контрацепцията е приемлива стратегия, когато в същото време се страхува от нежелана бременност, но за много жени различното лечение би било много по-изгодно и желателно.
Насоките [12] предлагат хормонални контрацептиви като първа линия за лечение на менструални аномалии и хирзутизъм/акне при СПКЯ, докато метформин се препоръчва като лечение при жени с СПКЯ и диабет тип 2 или нарушен глюкозен толеранс, когато модификацията на начина на живот не успее. За жени с менструални нарушения, които имат противопоказания или непоносимост към естропрогестините, метформин се счита за терапия от втора линия. Според някои експерти [50] вместо това трябва да се направи опит с метформин, преди да се приложат орални контрацептиви, независимо от противопоказанията, като се препоръчва контрацепция, когато има висок риск от нежелана бременност. Изглежда, че метформин подобрява и последващия отговор на яйчниците към кломифен при нарушения на безплодието, като има сравними резултати както при пациенти с много висок, така и при пациенти без ИТМ. Въпреки това, метформин не е без странични ефекти, които често компрометират спазването.
Следователно дебатът за терапията продължава и често има объркване, както сред здравните специалисти, така и сред пациентите, относно това кой е отговорен за избора на лечение: жените обикновено се обръщат към гинеколога на първо място, тъй като имат проблеми с менструалния цикъл нередовност и плодовитост, с разочарование от ендокринолога. Освен това много жени неволно приемат идеята за непрекъсната медикализация и търсят различни решения.
В този контекст може да се предвиди централна роля на диетолог, в светлината на указанията на същите насоки, които сега смятат, че решаващ елемент в управлението на СПКЯ е модификацията на начина на живот и храненето.
Инсулиновата резистентност беше значително намалена, като падна под прага на HOMA-IR от 2,5; също така холестеролът и триглицеридите бяха значително намалени. Андрогените намаляват значително, както и LH и LH/FSH, което предполага регресия на хормоналните аномалии на PCOS. Подобрението в оценката на Ferriman Gallwey не достига статистическа значимост, но можем да предположим, че 12 седмици не са били достатъчни, за да се наблюдава намаляване на резултатите от хирзутизма: всъщност цикълът на косата в зависимост от телесната площ може да продължи няколко месеца и е известно, че фармакологичната терапия, базирана на антиандрогени, отнема от 6 до 12 месеца, за да се получи добро намаляване на резултата.
Заключения
Резултатите от нашето проучване предполагат използването на KD като възможна терапевтична помощ при СПКЯ, което да бъде последвано от по-балансиран хранителен режим, но винаги с особено внимание към количеството въглехидрати. Продължителността на KD все още е въпрос: няма данни за странични ефекти в краткосрочен план, те се считат за безопасни за кратки цикли. Налице е по-малко информация за диетите в дългосрочен план, но опитът, придобит в областта на епилепсията и синдрома на дефицит на GLUT-1 [73,74,75,76,77,78,79], подкрепя възможна употреба и за продължителни периоди. Вероятно е да се предположи настройката на протоколи, които да се повтарят в цикли с течение на времето, разпръснати с периоди на балансиран режим.
Трябва да се имат предвид някои ограничения на изследването. Първият е, че не са оценени ефектите на KD върху други резултати като олигоменорея и безплодие. Второ, OGTT за глюкоза и инсулин би добавил повече информация за метаболитните ефекти на KD, за съжаление експерименталната обстановка не ни позволи да извършим този анализ; накрая, малкият размер на извадката и дизайнът на единичната ръка са необходими допълнителни потвърждения, евентуално увеличаване на броя на участниците, удължаване на периода на лечение и съчетаване на нискокалорична кетогенна диета с нискокалорична средиземноморска диета.
Наличност на данни и материали
Наборите от данни, използвани и/или анализирани по време на настоящото проучване, са достъпни от съответния автор при разумна заявка.
- Диета, метформин и инозитол при жени с наднормено тегло и затлъстяване с ефекти на синдрома на поликистозните яйчници
- Ефекти от бездействието и състава на диетата върху енергийния баланс на човека International Journal of Obesity
- Развитие на затлъстяването и синдрома на поликистозните яйчници при юноши - FullText - Хормонални изследвания
- Диета за бременни жени с наднормено тегло и затлъстяване; Новини-Медицински
- Експертно мнение; Луд за кетони; - Кетогенната диета при спортистите с различен ефект върху атлетиката