Маджид Карандиш
Център за изследване на храненето и метаболитните болести, Университет по медицински науки Ahvaz Jundishapur, Ahvaz, Иран
Махтаб Тамими
1 Катедра по хранителни науки, Международен отдел Arvand, Университет по медицински науки Ahvaz Jundishapur, Ahvaz, Иран
Али Акбар Шайестех
2 Катедра по гастроентерология, Медицински факултет, Университет по медицински науки Ahvaz Jundishapur, Ahvaz, Иран
Мохамад Хосеин Хагигизаде
3 Катедра по биостатика и епидемиология, Факултет по обществено здраве, Университет по медицински науки Ahvaz Jundishapur, Ahvaz, Иран
Мохамад Таха Джалали
4 Изследователски център за хиперлипидемия, Университет по медицински науки Ahvaz Jundishapur, Ahvaz, Иран
Резюме
Заден план:
Има малко проучвания за изследване на ефекта от добавянето на магнезий (Mg) върху чернодробните ензими. Целта на това проучване е да се оцени ефектът от добавянето на Mg и загубата на тегло върху чернодробните ензими, липидния профил и кръвната захар на гладно при пациенти с неалкохолна мастна чернодробна болест (NAFLD).
Материали и методи:
Това проучване е двойно-сляпо, плацебо-контролирано, рандомизирано клинично изпитване. Ултрасонографията се използва за диагностициране на затлъстяване на черния дроб при пациенти с аланин аминотрансфераза (ALT) ≥ 40 U/L и без други чернодробни заболявания. Общо 68 участници (18-59 години) с NAFLD бяха разделени на случаен принцип в две групи, за да получат или Mg добавка (350 mg елементарен Mg на ден), или плацебо в продължение на 90 дни. В началото и в края на интервенцията серумен ALT, аспартат аминотрансфераза (AST), алкална фосфатаза (ALP), общ холестерол (TCHO), липопротеинов холестерол с висока плътност (HDL-C), триглицериди (TG), кръвна захар и серум инсулин и нивата на Mg са измервани на гладно. Липопротеиновият холестерол с ниска плътност (LDL-C) и инсулиновата резистентност (IR) са изчислени, като се използват формулата на Friedewald и моделът на хомеостаза за оценка на инсулиновата резистентност (HOMA-IR), съответно. Всички участници получиха препоръки за начина на живот, включително нискокалорична диета и физическа активност.
Резултати:
Значително намаление в рамките на интервенционната и плацебо групата се наблюдава при ALT (57,00 (25) до 41,82 ± 19,40 U/L, P = 0,000; 68,50 ± 26,96 до 40,17 ± 19,40 U/L, P = 0,000 в Mg и плацебо групите, съответно ). Подобни значителни намаления се наблюдават при AST и серумния инсулин на гладно в рамките на изследваните групи. Намаляването на теглото също е значимо и в двете групи (съответно 91,05 ± 13,77 до 87,60 ± 14,37 kg и 94,59 ± 16,85 до 91,45 ± 16,39 kg при Mg и плацебо). LDL-C и TCHO са намалени значително в плацебо групата, но не и в интервенционната група. Серумният Mg се е увеличил значително в интервенционната група. Не са наблюдавани статистически значими разлики между двете проучвани групи на изходно ниво и след интервенция.
Заключение:
Според резултатите от това проучване, добавката Mg не влияе върху чернодробните ензими, но загубата на тегло може да има важна роля за подобряване на мастната чернодробна болест.
ВЪВЕДЕНИЕ
Безалкохолната мастна чернодробна болест (NAFLD) се определя като спектър от нарушения, характеризиращи се предимно с макровезикуларна чернодробна стеатоза. Клиничното значение на NAFLD произтича от факта, че значителна част от тези пациенти (20-30%) развиват неалкохолен стеатохепатит (NASH) и това състояние, за разлика от обикновения мастен черен дроб, е потенциално прогресиращо чернодробно разстройство, което може да доведе до краен стадий на чернодробно заболяване и хепатоцелуларен карцином. [1] Въпреки че точният механизъм за развитие на NASH не е известен, скорошни проучвания показват, че пациентите с NASH имат по-високо разпространение на инсулинова резистентност. [2,3] Затлъстяването също е силно свързано с чернодробна стеатоза. [3] В допълнение, някои проучвания съобщават за връзка между намалените серумни нива на магнезий (Mg) и NASH. [4]
Mg е кофактор за повече от 300 метаболитни реакции в тялото. [5] Mg играе важна роля в цялостните клетъчни функции, включително синтеза на ДНК и протеини, метаболизма на глюкозата и мазнините и окислителното фосфорилиране. [6] Недостигът на Mg е свързан с предизвикване на възпалителен отговор, митохондриална дисфункция, профиброгенен отговор и намаляване на активността на антиоксидантната система; който стимулира пероксидацията на липидите и индуцирането на цитокини и добре известни пътища за развитие на стеатохепатит и чернодробна фиброза. [7]
В няколко проучвания се съобщава, че добавките на Mg са свързани с подобрени възпалителни фактори, [7] метаболизъм на глюкозата и инсулинова резистентност. Такава връзка не е била показана в други проучвания. [8,9,10,11] Ползите от добавките на Mg при пациенти с NAFLD не са установени. Следователно, ефектът от добавките на Mg и загубата на тегло върху серумните чернодробни ензими, липидния профил и инсулиновата резистентност са изследвани в това двойно-сляпо, плацебо-контролирано, рандомизирано проучване.
МАТЕРИАЛИ И МЕТОДИ
Участници
Това проучване е двойно-сляпо, плацебо-контролирано, рандомизирано клинично изпитване. Участниците бяха вербувани от Ахваз, разположен в югозападната част на Иран. Писмено информирано съгласие е получено от всички пациенти. Критериите за включване бяха: Възраст между 18-59 години, анормална чернодробна функция с аланин аминотрансфераза (ALT) ≥40 U/L и затлъстяване на черния дроб, диагностицирана с ултразвук. Критериите за изключване бяха: хронична диария, прием на алкохол (равен на или повече от 30 g/ден), консумация на диуретици или предишна перорална добавка Mg, чернодробно заболяване, хемохроматоза, болест на Уилсън, цироза, анамнеза за други чернодробни, бъбречни или белодробни нарушения.
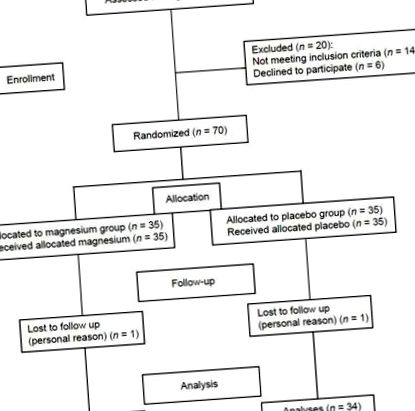
Блок-схема на набиране за двойно-сляпо, плацебо-контролирано, рандомизирано контролирано проучване на Mg добавки при NAFLD
Седемдесет пациенти с NAFLD са разделени на случаен принцип в две групи: Интервенционната група (n = 35) е получавала 350 mg елементарен Mg на ден под формата на магнезиев оксид в продължение на 90 дни, а контролната група (n = 35) е получавала плацебо (лактоза ). Капсулите добавки и плацебо изглеждаха идентични и бяха специално подготвени за това проучване от Darou-Pakhsh Company (Техеран, Иран) и съхранявани при 20-25 ° C. Тази доза Mg е избрана според допустимите горни нива на прием (UL) на Mg и доклада на Heriberto Rodriguez-Hernandez относно ефекта от добавките на Mg върху ALT. [7]
Диетичните навици, демографските и антропометричните данни са получени чрез лично интервю или измерване.
Дневният прием на хранителни вещества, включително енергия и Mg, се изчислява чрез три 24-часови диетични припомняния през първия месец от изследването от обучен диетолог. Диетичните данни са анализирани от софтуера Nutritionist IV. Физическата активност беше оценена с помощта на общия практически въпросник за физическа активност (GPPAQ) на изходно ниво. [12]
Беше изчислена нискокалорична диета и участниците бяха помолени да се подложат на тази диета. Потребността от енергия се изчислява по формулата на Световната здравна организация (СЗО) и след това се намалява до 500 kcal/ден (≥ 55% въглехидрати, 15-20% протеини и ≤30% мазнини). Всички участници бяха посъветвани да извършват поне 30 минути физическа активност на ден. Съответствието и намесата в начина на живот се оценяват на всеки 2 седмици чрез телефонен контакт. Останалите капсули са получени в края на проучването за изчисляване на степента на съответствие.
Измервания
Биохимичните променливи бяха измерени на изходно ниво и в края на проучването.
Височината и теглото бяха измерени чрез използване на стандартни протоколи с участници в леки дрехи и без обувки. Индексът на телесна маса (ИТМ) се изчислява като тегло (kg), разделено на квадрат на височина (m 2), а процентът на телесните мазнини се изчислява с монитора на телесни мазнини Omron (HBF-306) в началото и в края на проучването. Взети са кръвни проби след 12-14 часа на гладно през нощта на изходно ниво и след интервенционния период. Серумните проби се прехвърлят в микроепруветки и се съхраняват при -70 ° C до анализ. ALT и аспартат аминотрансферазата (AST) се определят по метода, разработен от Международната федерация по клинична химия (IFCC). [13,14] Алкалната фосфатаза (ALP) се определя от Deutschen Gesellschaft für Klinische Chemie (DGKC); [15] общ холестерол (TCHO), липопротеинов холестерол с висока плътност (HDL-C), триглицерид (TG) и серум Mg се измерват по ензимен колориметричен метод. Кръвната захар на гладно (FBS) се измерва с колориметричен метод. Липопротеиновият холестерол с ниска плътност (LDL-C) се изчислява по формулата на Friedewald. [16] Концентрацията на инсулин се определя чрез имуноензимометричен метод, а инсулиновата чувствителност се оценява чрез хомеостазен модел на оценка на инсулиновата резистентност (HOMA-IR) по следната формула: Инсулин на гладно (μIU/ml) × гликемия на гладно (mg/dl)/405. [17]
Статистически анализ
РЕЗУЛТАТИ
Общо 68 участници завършиха процеса. Двама участници бяха загубени за проследяване (по 1 пациент от всяка група). Поради лична причина те не обичаха да продължават участията си. Равен брой загубени за проследяване в изследваните групи направиха групите сравними по отношение на тази променлива. Не са докладвани нежелани или странични ефекти от участниците. Степента на съответствие е съответно 85,2 и 84% в Mg добавките и плацебо групите. В началото не е имало значителни разлики в демографските характеристики и хранителния статус между интервенционните и плацебо групите [Таблица 1]. Средната възраст на участниците е 36 ± 7 години. Шестима участници от добавките и двама участници от плацебо групи са били предписани една таблетка метформин (500 mg) на ден по време на проучването. Няма обаче статистически значима разлика между групите по отношение на приема на това лекарство (P = 0,25). Средните ± SD от общия прием на Mg, включително добавката, са съответно 553,83 ± 54,38 и 188,25 ± 70,16 в групите с добавки и плацебо.
маса 1
Изходни демографски и хранителни данни на 68 пациенти с NAFLD
Антропометричните и биохимичните характеристики на 68-те пациенти на изходно ниво и в края на проучването са показани в Таблица Таблица 2 2 и 3, 3, съответно. В началото няма значителни разлики във всички измерени променливи между двете групи. След интервенция теглото и ИТМ (P = 0,004 и P = 0,000 в Mg и съответно плацебо групите), процентът на телесните мазнини, инсулин и инсулинова резистентност (IR), ALT (P = 0,000 и в двете групи) и AST намаляват значително интервенция и плацебо групи. В края на интервенционния период серумните нива на АЛАТ са съответно под 40 U/L в Mg (n = 19) и плацебо групите (n = 22). FBS и TG намаляват и в двете групи, но не значително (P> 0,05). Незначително увеличение се наблюдава при HDL-C и в двете групи. От друга страна, TCHO и LDL-C намаляват значително в плацебо групата, но не и в интервенционната група. ALP намалява в плацебо групата и се увеличава в интервенционната група, но не значително. В края на проучването не са наблюдавани статистически значими разлики между интервенционните и плацебо групите.
Таблица 2
Сравнение на антропометричните характеристики на изходно ниво и 90 дни след интервенцията при 68 пациенти с NAFLD (средно ± SD)
Таблица 3
Сравнение на биохимичните характеристики на изходно ниво и 90 дни след интервенцията при 68 пациенти с NAFLD
ДИСКУСИЯ
Това проучване показа, че добавките с Mg не засягат чернодробните ензими при NAFLD. Ползите от Mg добавки при пациенти с NAFLD все още не са установени.
Доколкото ни е известно, до момента е публикувано само едно контролно проучване за ефекта на добавката Mg върху нивата на ALT. [7] Значителният ефект на добавката Mg върху нивата на ALT в това проучване е в противоречие с констатацията от нашето проучване. Има голяма разлика между две изследвания. Те класифицираха участниците според хипомагнезиемията и използваха доза Mg по-висока от допустимата UL (450 mg/ден елементарен Mg). Продължителността на това проучване беше 4 месеца, което е малко по-дълго от това проучване. Въпреки че добавките с Mg могат да бъдат най-полезни за лица с Mg дефицит, [7,8,9,21], но в нашето проучване участниците са били нормамагнезиемични.
В това проучване се наблюдава значително намаляване на ALT, AST, инсулин и IR в интервенционната и плацебо групата и се смята, че е резултат от значително намаляване на теглото и ИТМ и в двете групи. Намаляването на нивата на ALT, AST, TCHO и TG при жени със затлъстяване, които са получавали диета с ниско съдържание на въглехидрати (LCD) или диета с ниско съдържание на мазнини (LFD) в продължение на 6 месеца, кара Heriberto Rodriguez-Hernandez et al., [23] да предположи, че независимо на диетата, метаболитните промени зависят от намаляването на теглото. Wang et al., [24] показаха, че простите интервенции в начина на живот, включително диетични промени и увеличаване на физическата активност при затлъстели деца с NAFLD, могат да доведат до значително подобрение на чернодробната функция и инсулиновата резистентност. Wong et al., [25] предполагат, че намаляването на теглото е свързано с намален риск при прогресия на NAFLD и тези пациенти трябва да претърпят промени в начина на живот.
В нашето проучване пациентите на интервенция и плацебо групи намаляват съответно 3,78 и 3,31% от първоначалното телесно тегло. Тези намаления са резултат от модификации на начина на живот. Публикуваната литература показва, че различните степени на загуба на тегло, вариращи от 1 до 10%, са свързани с подобряване на IR и чернодробните ензими. [26,27,28,29,30]
В нашето проучване се наблюдава значително намаляване на TCHO и LDL-C в групата на плацебо. Тези резултати бяха неочаквани и няма ясно обяснение за това. Тъй като средната стойност на промените не е голяма, изглежда, че е имало статистическа значимост без никакво клинично значение и средните нива на LDL-C и TCHO са били под 130 mg/dl и 200 mg/dl, съответно в двете групи.
В две предишни проучвания беше показан ефектът от добавките на Mg върху чернодробните ензими, но тези проучвания бяха проведени върху алкохолни участници [31,32] и не е подобно на това проучване, тъй като според нашите познания патогенезата на нарушените чернодробни ензими при алкохолиците се различава от NAFLD. Това проучване е първото рандомизирано клинично проучване, което изследва ефекта от добавките на Mg върху NAFLD.
В това проучване съществуват няколко ограничения: Ултрасонографията се използва за определяне на затлъстяване на черния дроб, но не го повторихме в края на проучването. Промените в степента на NAFLD обаче не са дефинираният основен резултат от това проучване. Кратката продължителност на това проучване е друго ограничение, така че не е ясно, че промените в телесното тегло, както и в чернодробните ензими и нивата на инсулин се поддържат дълго време. Други ограничения на това проучване са липсата на директно измерване на инсулиновата хомеостаза, калий и калций. Установено е обаче, че HOMA-IR е полезен метод за определяне на инсулиновата чувствителност при участници с диабет и недиабет и може да бъде надеждно използван в проучвания, при които се измерват само кръвни проби на гладно от глюкоза и инсулин. [17,33] Mg хомеостазата е свързана със състоянието на калций и калий и трябва да се оценява в комбинация с тези два минерала. [5]
Важен момент е, че резултатите от това проучване са свързани с участници с нормални серумни нива на Mg и тези находки не могат да бъдат екстраполирани на пациенти с хипомагнезиемия.
В заключение, резултатите от това рандомизирано клинично изпитване показват, че добавките с Mg не влияят на нивата на серумните чернодробни ензими, липидния профил и гликемичния контрол при нормамомагнезиеми пациенти с NAFLD. Модификациите на начина на живот, особено намаляването на теглото, могат да подобрят състоянието на това заболяване.
ПРИЗНАНИЕ
Източникът на данни, използвани в тази статия, е от магистърската теза на Махтаб Тамими, студент от Университета по медицински науки на Ахваз Юндишапур; и финансова подкрепа беше предоставена от Университета по медицински науки Ahvaz Jundishapur.
Бележки под линия
Източник на подкрепа: Arvand International Division, Ahvaz Jundishapur University of Medical Sciences, Abadan, Iran, No. NRC-9011 Това проучване е одобрено от Комитета по етика на Университета по медицински науки Ahvaz Jundishapur, Ahvaz, Иран и регистрирано в Иранския регистър на клиничните изпитвания (IRCT номер IRCT201203128753N1)
Конфликт на интереси: Никой не е деклариран.
- Влиянието на хранителните добавки с протеини за пациенти с голямо отслабване, подложени на
- Степента и ефектът от загубата на тегло при пациенти с остра миелоидна левкемия, получаващи индукция и
- Загуба на тегло и подобряване на чернодробната фиброза при египетски пациенти с хроничен хепатит С
- Превърнете Hula Hoop за отслабване, отслабнете движение, тренирайте, ефект на отслабване, фитнес PNG и вектор с
- The; Ефект на Сталоун; Скалист път към отслабване; Джо Де Джорджо