Хишам Берруги
1 Катедра по медицина, Гериатрична служба, Факултет по медицина и биологични науки, Университет на Шербрук, 3001 12e Avenue Nord, Шербрук, QC, Канада J1H 5N4
2 Катедра по биология, Полидисциплинарен факултет, Университет Султан Мулай Слиман, BP 592, 23000 Бени Мелал, Мароко
Суад Ихлеф
1 Катедра по медицина, Гериатрична служба, Факултет по медицина и биологични науки, Университет на Шербрук, 3001 12e Avenue Nord, Шербрук, QC, Канада J1H 5N4
Абделуахед Халил
1 Катедра по медицина, Гериатрична служба, Факултет по медицина и биологични науки, Университет на Шербрук, 3001 12e Avenue Nord, Шербрук, QC, Канада J1H 5N4
Резюме
Резултатите от настоящата работа свидетелстват за благотворната роля на консумацията на зехтин от екстра върджин (EVOO) за оксидативен стрес и сърдечно-съдови заболявания. Полифенолите, съдържащи се в EVOO, са отговорни за инхибиране на оксидативните увреждания на липопротеините и насърчаване на обратния процес на транспорт на холестерола по ABCA1 път.
1. Въведение
Ишемичната болест на сърцето (ИБС) е основната причина за смъртността в Западния свят. Окисляването на липопротеините с ниска плътност (LDL) е ранно събитие в развитието на атеросклероза, основната причина за ИБС [1]. Окислените LDL не се разпознават от LDL-рецептора Apo (B/E), но се поглъщат от макрофаги по нерегулиран начин по пътя на рецептора за почистване, което води до образуването на пенообразни клетки, отличителен белег на артериосклеротичните лезии [1].
Смята се, че специфичният за макрофаги обратен транспорт на холестерола (RCT) е един от най-важните HDL-медиирани кардиопротективни механизми. RCT е процесът, при който холестеролът в периферните клетки се оттича към циркулиращия HDL и се транспортира обратно в черния дроб за отделяне с жлъчката и изпражненията [2, 3]. Популяризирането на RCT се счита за основна антиатерогенна функция на HDL [4, 5]. Изтичането на холестерол от клетки към HDL е първата и ограничаваща скоростта стъпка на RCT [6]. Описани са два основни пътя на изтичане на холестерол от макрофаги: медииран от рецептора на SR-BI холестерол и медииран от ABCA1/ABCG1 холестерол. ABCA1 насърчава изтичането на фосфолипиди и холестерол към беден на липиди apo-AI чрез процес, който включва директно свързване на apo-AI с транспортера ABCA1, докато ABCG1 и SR-BI са ключови медиатори на изтичането на холестерол от макрофаги към зрял HDL [7 ]. Данните от скорошно проучване показват, че възпалителният процес предизвиква промени в състава и метаболизма на HDL, които нарушават RCT [8]. Интересното е, че наскоро показахме, че RCT се нарушава и със стареенето, особено чрез промени в ABCA1-медиирания път на изтичане на холестерол [9, 10].
Благоприятните ефекти на полифенолите изглежда се медиират чрез множество биохимични пътища и сигнални механизми, които действат независимо или синергично. В настоящото изследване ние изследвахме атеропротективния ефект на фенолните съединения в EVOO върху изтичането на холестерол и върху уврежданията от оксидативен стрес при здрави индивиди.
2. Методи
2.1. Субекти
Двадесет и четири здрави доброволци (30,92 ± 2,55 години) с нормални серумни липидни профили и кръвно налягане бяха наети. Всички те са били непушачи и не са приемали никакви лекарства, включително лечение за понижаване на липидите или орални антиоксиданти. Нито една от субектите не е била подложена на естроген-заместителна терапия за менопауза. Никой от участниците не показва клинични признаци на възпаление, затлъстяване или диабет. Физическите и биохимичните параметри на участниците са представени в таблица 1. Комитетът по етика на Гериатричния университетски институт Шербрук одобри проучването и всички субекти предоставиха писмено информирано съгласие преди да бъдат записани.
маса 1
Клинични и биохимични параметри на участниците.
| n = 24 (w/m) | 14/10 |
| Възраст (средно ± SD години) | 30,92 ± 2,55 |
| Индекс на телесна маса (kg/m 2) | 23,7 ± 1,65 |
| Кръвно налягане в системата (mmHg) | 127 ± 4,65 |
| Диас. кръвно налягане (mmHg) | 78,23 ± 2,09 |
| Общ холестерол (mmol/L) | 5,06 ± 0,2 |
| Триглицериди (mmol/L) | 1,32 ± 0,15 |
| HDL-c (mmol/L) | 1,42 ± 0,09 |
| LDL-c (mmol/L) | 3,05 ± 0,15 |
| Apo A1 (g/L) | 1,56 ± 0,05 |
| Апо B (g/L) | 0,90 ± 0,04 |
| Apo B/Apo A1 | 0,8 ± 0,04 |
| TC/HDL-c | 3,81 ± 0,23 |
| LDL-c/HDL-c | 2,5 ± 0,2 |
| TG/HDL-c | 1,08 ± 0,17 |
| Глюкоза (mmol/L) | 4.43 ± 0.10 |
| Инсулин (pmol/L) | 38,32 ± 5,26 |
| CRP (mg/L) | 3,16 ± 0,13 |
TC (общ холестерол); HDL-C (HDL-холестерол); LDL-C (LDL-холестерол); CRP (С-реактивен протеин).
2.2. Фитохимия
Фенолните съединения бяха извлечени от EVOO, използвайки метода на Pirisi et al. [20]. Накратко, EVOO се смесва с н-хексан и метанол/вода и се разбърква във вихров апарат в продължение на една нощ при 4 ° С. След това сместа се центрофугира и хидроалкохолният разтвор се промива с n-хексан и след това се лиофилизира за една нощ.
2.3. Изолиране на липопротеини
Човешката плазма на гладно се събира в хепаринови епруветки и HDL незабавно се изолира, използвайки метода на Sattler et al. [21]. Изолираните липопротеини се диализират през нощта при 4 ° С срещу 10 -2 М натриев фосфатен буфер (рН 7.0). Концентрациите на протеини бяха измерени с помощта на търговски комплекти за анализ (Bio-Rad, Канада), използвайки производствения протокол.
2.4. Обогатяване на липопротеини с EVOO и EVOO-PC
Човешката плазма се инкубира през нощта с леко разбъркване при 4 ° С в присъствието на EVOO (0,2 mg/ml плазма) или EVOO-PC (1,76 mg/ml плазма). След това LDL и HDL се изолират, както е описано по-горе.
2.5. Медно медиирано окисляване на липопротеини
Липопротеините се пероксидират, както е описано по-рано, като се използват йони на преходни метали като окислители [22]. Накратко, обогатените с EVOO и EVOO-PC липопротеини [(LDL 100 μg/mL) или (HDL 200 μg/mL)] бяха суспендирани в 10 mM натриев фосфатен буфер (pH 7) и бяха инкубирани за 0 до 4 h при 37 ° C в присъствието на 10 μM меден сулфат. Реакцията на окисление се спира чрез добавяне на EDTA. Образуването на липиден пероксид се оценява чрез проследяване на образуването на конюгиран диен при 234 nm.
2.6. Клетъчни култури
Човешки THP-1 моноцити и J774 макрофаги се култивират в RPMI 1640 и DMEM среда, съответно. Средата беше допълнена с 10% инактивиран с топлина FBS, 50 mM 2-β-меркаптоетанол (само за THP-1), 2 mM L-глутамин, 5 mg/mL глюкоза и 100 U/mL пеницилин. Диференциацията на THP-1 моноцитите в макрофаги се индуцира чрез култивиране на моноцитите в присъствието на 100 μM PMA за 96 h.
2.7. Измервания на изтичане на холестерол
Макрофагите, получени от THP-1 и макрофагите J774 се инкубират в прясна среда за растеж, съдържаща 0,2 μCi/mL [3 H] -холестерол за 48 часа или 1 μCi/mL [3 H] -холестерол, съответно за 24 часа. Заредените клетки се измиват, уравновесяват в безсерумна среда, съдържаща 1% BSA за 12 h, измиват се отново и се подлагат на различни обработки. Получените от THP-1 макрофаги се инкубират в продължение на 24 часа с (1) среда без HDL, (2) HDL (50 μg/mL), (3) обогатен с EVOO HDL (OO-HDL) или (4) EVOO -Обогатен с HDL HDL (PC-HDL).
[3 H] -Натоварени с холестерол THP-1 макрофаги са били подложени на оксидативен стрес, като са били инкубирани с 0,2 тМ желязо/аскорбат (Fe/Asc) в отсъствие или присъствие на EVOO-PC (320 μg/ml) за 6 h . След това те бяха инкубирани с HDL в продължение на 24 часа, за да се оцени изтичането на холестерол при различни условия.
Ефектът на EVOO-PC върху ABCA1-медиирания холестеролов излив беше оценен с помощта на макрофаги J774. [3 H] -Натоварени с холестерол макрофаги J774 бяха инкубирани в продължение на 12 часа с 0 до 320 μg/mL EVOO-PC за генериране на обогатени с ABCA1 клетки или с 300 μM 8-Br-cAMP (положителен контрол) за стимулиране на ABCA1 генна транскрипция и експресия на повърхностен протеин. След това макрофагите J7774 бяха инкубирани с 25 μg/mL апо-AI в продължение на 4 часа.
За да разберем по-добре механизма на EVOO-PC-медиирания холестеролов излив, ние изучихме ефекта на двете основни фенолни съединения в EVOO (тирозол и хидрокситирозол) върху ABCA1-медиирания холестеролов излив. [3 H] -Натоварени с холестерол макрофаги J774 се инкубират в продължение на 12 часа с 0 до 25 μM тирозол или хидрокситирозол, за да се генерират обогатени с ABCA1 клетки и след това се инкубират с 25 μg/mL апо-AI в продължение на 4 часа. 8-Br-cAMP се използва като положителна контрола.
Изтичането на холестерол се определя чрез течно сцинтилационно броене и процентът на радиоактивно маркиран холестерол (процент на изтичане на холестерол) се изчислява по следната формула: (cpm в средата/[cpm в клетките + среда]) × 100.
2.8. Анализи на Western Blot
Експресията на ABCA1 протеин в макрофаги J774 беше изследвана чрез инкубиране за 12 h с 0 до 320 mg/ml EVOO-PC или 5 или 10 μM хидрокситирозол или тирозол. Протеините (20 μg) се разделят чрез електрофореза върху 10% акриламидни гелове и се прехвърлят в мембрани от поливинилиден дифлуорид (PVDF). Мембраните бяха блокирани с 5% мляко в PBS/Tween 20 и бяха инкубирани с първични антитела (анти-ABCA1) и след това със специфични IgG-HRP-конюгирани вторични антитела. като контрол се използва β-актин. Протеиновите ленти бяха открити с помощта на подобрен реактив за хемилуминесценция (ECL) [10].
2.9. Статистически анализ
Стойностите се изразяват като средни стойности ± SEM. За многократни сравнения е използван еднопосочен дисперсионен анализ (ANOVA). Използван е линеен регресионен анализ за оценка на връзката между две непрекъснати променливи. Всички статистически анализи бяха извършени с помощта на софтуера GraphPad Prism-5.
3. Резултати
3.1. Ефект на екстра върджин зехтин и екстракти от фенолни съединения EVOO върху окисляването на липопротеините
Концентрацията на общите фенолни съединения (41,9 mM; еквивалент на галова киселина) беше изчислена с помощта на метода Folin-Ciocalteu.
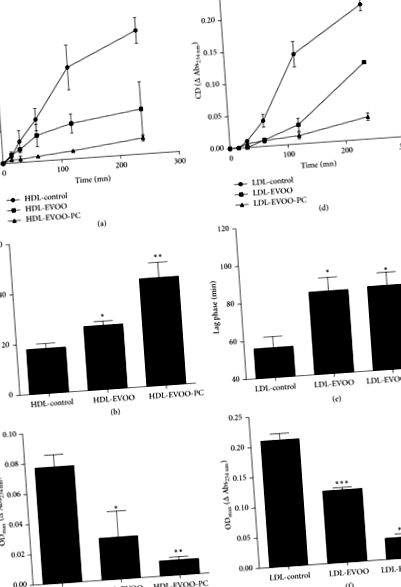
Пероксидацията с CuSO4 на полиненаситените мастни киселини (PUFA) в HDL и LDL се оценява чрез образуването на конюгирани диени. Кинетиката на пероксидация показа, че фазата на изоставане на LDL е по-дълга от тази на HDL. Фазата на изоставане беше последвана от фази на разпространение и прекратяване.
В светлината на тези резултати след това изследвахме ефекта на две основни фенолни съединения в EVOO-PC (пречистен тирозол и хидрокситирозол) върху изтичането на холестерол от и експресията на ABCA1 протеин в макрофагите J774. Нашите резултати показаха, че тирозолът и хидрокситирозолът се повишават в зависимост от концентрацията на ABCA1-зависимия изтичане на холестерол (Фигури 4 (a) и 4 (b), респ.).
Тирозолът и хидрокситирозолът увеличават експресията на ABCA1 протеин и усилват апоА-I-медиирания холестеролов излив. [3 H] -Холестерол-заредени макрофаги J774 бяха инкубирани в продължение на 12 часа с различни концентрации (0 до 25 μM) тирозол (а) или хидрокситирозол (b), за да се получат обогатени с ABCA1 клетки, които след това бяха инкубирани с 25 μg/mL на апо-AI за 4 часа. Резултатите се изразяват като средно ± SEM на поне три независими експеримента.
4. Дискусия
Зехтинът е основният източник на мазнини в средиземноморската диета. Голяма част от знания предостави доказателства за ползите от средиземноморската диета и консумацията на зехтин за превенция на атеросклероза и ИБС [24–27]. Няколко проучвания съобщават, че антиатерогенният ефект на зехтина е свързан с антиоксидантните и противовъзпалителни ефекти, оказвани от различни компоненти, особено мононенаситени мастни киселини (MUFA) и полифеноли [11, 17, 28–30]. Фенолните съединения, особено хидрокситирозол и олевропеин, дозозависими инхибират LDL и HDL окисляването in vitro и in vivo, потискат реакциите, задвижвани от супероксид, и прекъсват верижното разпространение на липидни пероксиди [31–34]. Интересното е, че проучване на Covas et al. [17] показа, че консумацията на EVOO увеличава постпрандиалната концентрация на фенолни съединения в плазмата и в LDL и HDL, което може да обясни защитния ефект на фенолните съединения.
Плазмените нива на HDL-холестерол са силно и обратно корелирани с риска от атеросклеротични сърдечно-съдови заболявания [35]. Предполага се, че HDL улеснява изтичането на холестерол от периферните тъкани и го транспортира обратно до черния дроб в процес, наречен RCT [36]. ABCA1 улеснява изтичането на холестерол от клетки към беден на липиди апо-AI, но не и към HDL [7, 37], докато друг ABC транспортер, ABCG1, както и SR-BI рецепторът, участва в изтичането на холестерол от макрофаги към HDL [38, 39]. Някои изследвания предполагат, че хранителните хранителни вещества и диетата могат да играят ключова роля в регулирането на RCT [25, 40–42]. По-рано показахме, че консумацията на EVOO подобрява RCT процеса, като повишава капацитета на HDL да медиира изтичането на холестерол и на макрофагите, получени от човешки моноцити (HMDM), за да отделят свободен холестерол [43]. В настоящото проучване изследвахме как консумацията на EVOO може да стимулира изтичането на холестерол. Ние се фокусирахме върху ефекта на EVOO-PC, особено есенциални феноли като тирозол и хидрокситирозол.
Въпреки това, малко се знае за молекулярния механизъм, чрез който фенолните съединения стимулират изтичането на холестерол. За да разберем по-добре механизма, чрез който EVOO-PC усилва медиирания от HDL холестеролов излив, ние изследвахме ефекта на EVOO-PC върху клетъчните сигнални пътища. Нашите резултати ясно показаха, че EVOO-PC, включително тирозол и хидрокситирозол, стимулира експресията на ABCA1 протеин в макрофагите J774, което може да обясни как тези феноли насърчават изтичането на холестерол до апоА-1. Uto-Kondo et al. [40] съобщават, че консумацията на кафе от здрави хора засилва изтичането на холестерол, медиирано от HDL, като увеличава експресията на ABCG1 и SR-BI, но не и ABCA1 и че това може да се дължи на фенолните киселини в кафето. Това изглежда малко вероятно, като се има предвид, че фенолните киселини активират експресията на чернодробен X рецептор-α (LXRα), което от своя страна трансактивира както ABCA1, така и ABCG1. Други проучвания, включително нашето, показват, че ресвератролът стимулира LXRα, ABCA1 и ABCG1 [52, 53]. По този начин изглежда, че различните фенолни съединения могат да стимулират изтичането на холестерол чрез различни механизми.
В заключение, нашите резултати показаха, че EVOO-PC засилва антиатерогенните свойства на HDL чрез намаляване на окислителните модификации на HDL и чрез поддържане на физикохимичните свойства на HDL, което от своя страна подобрява функционалността на HDL, особено способността да стимулира изтичането на холестерол. EVOO-PC също така защитава клетките от окислително увреждане и стимулира експресията на ABCA1 протеин, ключов фактор за изтичането на холестерол и генезиса на HDL. Нашите резултати са в съгласие с предишните ни открития, показващи, че консумацията на полифеноли от зехтин помага за намаляване на сърдечно-съдовия риск.
Признание
Настоящото проучване беше подкрепено с безвъзмездни средства от Канадските институти за здравни изследвания (MOP-89912 и IAO-134212).
- ДЪЛБОКА ФРЮ С ЕКСТРА ДЕВИНСКО МАСЛИНО - Giuliana Premium зехтин - Giuliana зехтин
- Холестеролът Източникът на зехтин
- Храни, които подобряват отношението ви от
- Коронавирусна диета 9 Храни, които насърчават релаксацията, за да ви помогнат да останете спокойни; CBS Детройт
- Храни, които естествено понижават холестерола - Здравеопазване на лекарите от Новия Запад