Евгений Н. Суспицин
a N.N. Институт по онкология на Петров, Санкт Петербург, Русия
b Педиатричен медицински университет в Санкт Петербург, Санкт Петербург, Русия
Анна П. Соколенко
a N.N. Институт по онкология на Петров, Санкт Петербург, Русия
b Педиатричен медицински университет в Санкт Петербург, Санкт Петербург, Русия
Лидия В. Лязина
b Педиатричен медицински университет в Санкт Петербург, Санкт Петербург, Русия
c Градски медицински генетичен център, Санкт Петербург, Русия
Елена В. Преображенская
a N.N. Институт по онкология на Петров, Санкт Петербург, Русия
Алла Й. Лепенчук
b Педиатричен медицински университет в Санкт Петербург, Санкт Петербург, Русия
Евгений Н. Имянитов
a N.N. Институт по онкология на Петров, Санкт Петербург, Русия
b Педиатричен медицински университет в Санкт Петербург, Санкт Петербург, Русия
d I.I. Мечников Северозападен медицински университет, Санкт Петербург, Русия
Свързани данни
Резюме
Синдромът на Bardet-Biedl (BBS) е рядка автозомно-рецесивна цилиопатия, характеризираща се със затлъстяване, постаксиална полидактилия, пигментозен ретинит, умствена изостаналост и бъбречни аномалии. Доказано е, че поне 19 гена са свързани с BBS и следователно генетичните тестове са много сложни. Използвахме платформа Illumina MiSeq за анализ на секвениране на цели екзоми на семейство със силни клинични характеристики на BBS. Хомозиготна мутация c.1967_1968delTAinsC (p.Leu656fsX673; RefSeq> NM_176824.2) в BBS7 е идентифицирана и при двете засегнати деца, докато здравите им братя и сестри и родителите, които не са роднини, са хетерозиготни за този алел. Генотипирането на 2832 ДНК проби, получени от руски кръводарители, разкрива 2 допълнителни хетерозиготни субекта (0,07%) с мутация c.1967_1968delTAinsC. Тези открития могат да улеснят генетичната диагноза за славянски пациенти с BBS.
Синдромът на Bardet-Biedl (BBS; OMIM 209900) е рядка генетична цилиопатия, проявяваща се с причиняваща слепота дистрофия на ретината, постаксиална полидактилия, затлъстяване, бъбречна дисфункция, хипогонадизъм, когнитивни аномалии и някои други тежки дефекти. Молекулярната диагноза на това разстройство е силно сложна, тъй като мутациите в поне 19 гена (BBS1-BBS19) могат да причинят фенотипа на BBS [Marion et al., 2012; Форсайт и Бийлс, 2013; Aldahmesh et al., 2014; Scheidecker et al., 2014]. Последователността на кандидат-гените е свързана с високи разходи за настройка на подходящи анализи, изисква значителни разходи и труд, за да се анализира множеството релевантни локуси и има риск от липсващи причинителни мутации в все още неизвестни гени на BBS [Marion et al., 2012; Редин и др., 2012; Scheidecker et al., 2014]. Неотдавнашното изобретение на секвениране на цели екзоми (WES) предостави жизнеспособна алтернатива за генетична диагноза на BBS [Ajmal et al., 2013]. Доколкото ни е известно, пациентите с BBS все още не са системно описвани в Русия или други славянски страни. Тук представяме руско семейство с BBS, което е идентифицирано чрез WES.
Доклад за случая
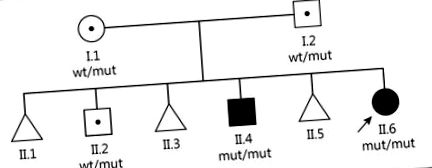
Семейство с 2 случая на предполагаема BBS поиска генетично консултиране в градския медицински генетичен център в Санкт Петербург, Русия (фиг. (Фиг. 1). 1). Родителите, които очевидно не са роднини, са родени в различни региони на Русия (Брянск и Волгоград). 35-годишната майка (I.1) съобщава за хронична анемия и лека стомашно-чревна дисфункция, докато 41-годишният баща (I.2) е здрав. И двамата родители не са имали предишни бракове. Към момента на сезиране в това семейство са настъпили 6 бременности. Първата (II.1), третата (II.3) и петата (II.5) бременност са прекъснати спонтанно на 6-8 седмици по неизвестни причини. Втората бременност (II.2) доведе до раждането на видимо здраво момче, което сега е на 16 години. За съжаление децата от четвъртата (II.4, 7-годишно момче) и шестата (II.6, 1.5-годишно момиче) бременност демонстрират характерни клинични характеристики на BBS.
Руско семейство с BBS. wt/mut = Хетерозиготен носител на BBS7 c.1967_1968delTAinsC мутация; mut/mut = хомозиготен носител на тази мутация. Родословието е съставено с помощта на дизайнер на родословни диаграми (CeGaT, Германия).
Признаците на BBS при засегнатото момче включват макрозомия (височина: 145 см; тегло: 52 кг; обиколка на главата: 54 см; обиколка на гърдите: 85 см), коремно затлъстяване, пигментозен ретинит, анамнеза за хирургично коригирана постаксиална полидактилия, изпъкнало чело, плосък нос мост, микропенис, лека умствена изостаналост и намалена емоционална отзивчивост. Засегнатото момиче е имало подобен фенотип, включително макрозомия (височина: 93 см; тегло: 20 кг; обиколка на главата: 50 см; обиколка на гърдите: 66 см), коремно затлъстяване, анамнеза за хирургично коригирана постаксиална полидактилия, изпъкнало чело, плосък носен мост, забавяне на говора и упорито отношение. Не е извършен офталмологичен преглед поради съпротива на детето.
Материали и методи
ДНК проби от засегнатото момиче и нейния здрав баща бяха подложени на WES. Обогатяването на Exome е извършено с помощта на Nextera Exome Enrichment Kit (Illumina, САЩ), който трябва да покрие 37 Mb кодиращи последователности (214 405 екзона; 98,3% от последователностите, анотирани в базата данни RefSeq) и включва всички 19 известни BBS гени. Масивното паралелно секвениране беше проведено с помощта на Illumina MiSeq и включваше множество 150-bp четения с приблизително 50 × покритие. Дълбочината на секвениране в кодиращите региони на BBS1-BBS19 не се различава значително от средната стойност (онлайн допълваща таблица 1; www.karger.com/doi/10.1159/000371408). Преобразуването на специфични за нуклеотиди флуоресцентни сигнали се извършва с помощта на софтуера MiSeq Reporter. Четенията бяха приведени в съответствие с човешкия референтен геном (версия hg19) от Burrows-Wheeller Aligner. Получените файлове бяха анализирани с помощта на софтуера GATK (Genome Analysis Tool Kit). Идентифицираните разлики от референтната последователност бяха коментирани с помощта на ресурса на Annovar (www.openbioinformatics.org/annovar/).
Резултати и дискусия
WES доведе до идентифициране на хомозиготна c.1967_ 1968delTAinsC (p. Leu656fsX673; RefSeq> NM_176824.2) мутация на зародишна линия в гена BBS7 при анализираното момиче. Засегнатият й брат носеше и този хомозиготен дефект BBS7, докато здравият брат и двамата родители бяха хетерозиготни носители на алела c.1967_1968 delTAinsC. Тази мутация вече е описана от Muller et al. [2010], който открива хетерозиготност на съединение BBS7 (c.1967_1968delTAinsC и c.528 + 1G> A) при пациент с BBS. BBS7 кодира субединица от комплекса BBSome и е от съществено значение за правилното функциониране на ресничките. Мутации в BBS7 са разкрити само при 2% от анализираните пациенти с BBS [Forsythe and Beales, 2013].
Наличието на идентична мутация при несвързани родители на пациенти с BBS не е неочаквано. Изненадващо, славянското население на Русия и съседните страни се характеризира с изразени основополагащи ефекти, така че редица генетични заболявания в тази част на света се приписват на повтарящи се алели [Dörk et al., 2000; Соколенко и др., 2010; Jurecka et al., 2012]. Чрез специфична за алела PCR, ние допълнително анализирахме колекция от 2832 ДНК проби, получени от руски здрави кръводарители и разкрихме 2 допълнителни субекта (0,07%), хетерозиготни за алела c.1967_1968delTAinsC в BBS7.
Това изследване илюстрира силата на WES за диагностика на генетично хетерогенни заболявания. Важно е, че ДНК анализът е извършен с помощта на сравнително достъпно лабораторно устройство от следващо поколение за секвениране. Повтарящият се характер на идентифицираната мутация, c.1967_1968delTAinsC в BBS7, сега трябва да бъде взет предвид при обмисляне на диагноза BBS при пациенти със славянски произход.
- Секвенирането на Exome идентифицира гени и генни набори, допринасящи за тежко детско затлъстяване, свързване
- Чести езикови състояния в първичната помощ - американски семеен лекар
- Определяне на често срещаните симптоми на синдрома на пропускащ червата и трудността на диагностиката
- Средства за отравяне с храна и съвети за предотвратяване на здравия разум - BadFoodRecall
- Диетичен лек при често срещани заболявания - конюнктивит