Еозинофилният езофагит (EoE) е хронично, медиирано от имунитет, възпалително състояние, характеризиращо се със симптоми на дисфункция на хранопровода и преобладаващо възпаление на еозинофилите (≥15 еозинофили на поле с висока мощност) на лигавицата на хранопровода, диагностицирано след изключване на други причини за езофагеална еозинофилия ( Маса 1). В това съобщение ние засягаме текущото състояние на различни аспекти на EoE и подчертаваме възможностите за бъдеща работа.
Епидемиология
Допреди няколко десетилетия EoE се смяташе за необичайно същество, но сега се очертава като честа причина за заболеваемост на горните стомашно-чревни (GI) пътища както при деца, така и при възрастни. Голям мета-анализ прогнозира честотата и честотата на разпространение при деца съответно на 5,1 случая/100 000 лица/година и 19,1 случая/100 000 души. 1 EoE се диагностицира при 2–6,5% от пациентите, подложени на езофагогастродуоденоскопия (EGD) за всяка индикация и това се увеличава до 12–22%, ако дисфагията е индикация. 2 Въпреки че EoE може да засегне пациенти от всички възрастови групи, той има бимодален пик с повечето случаи в педиатричната възрастова група или в третото десетилетие от живота. 3 EoE е по-често при мъжете от Кавказка и има силна връзка със съпътстващи атопични състояния като астма, екзема, ринит и хранителни алергии. 4
Бъдещи указания/неудовлетворени нужди
Точните причини за нарастващата честота и разпространение са до голяма степен неизвестни и не могат да бъдат обяснени единствено с повишено разпознаване на заболяването. Съществува значителен интерес към разгадаването на тези промени, включително епидемиологични фактори като ранни събития в живота, инфекциозни процеси, агенти на околната среда и хранителни навици.
Клинично представяне
Клиничното представяне на EoE варира в зависимост от възрастта на пациента. Малките деца обикновено се проявяват с неспецифични симптоми като затруднено хранене, повръщане, коремна болка, неспособност да се развият нормални хранителни режими, като например прогресиране на минали течности/меки твърди вещества и понякога неуспех за процъфтяване. Юноши и възрастни имат класически симптоми, които включват дисфагия и въздействие върху храната; EoE сега е една от най-честите причини за дисфагия и въздействие върху храната в Съединените щати. 2 Някои пациенти също могат да имат симптоми, имитиращи гастро-езофагеален рефлукс, като киселини, епигастрална болка, диспепсия и болка в гърдите. Пациентите с EoE често развиват механизми за справяне, за да компенсират симптомите си, като бавно хранене, прекалено дъвчене, малки хапки, нарязване на храни на по-малки парчета, смазване на храна с различни сосове, пиене на течност след повечето ухапвания и избягване на текстурирана храна като месо и хляб. 4
Бъдещи указания/неудовлетворени нужди
Отчетените от пациентите резултати (PRO) при EoE се нуждаят от по-нататъшно проучване, включително идентифициране и валидиране на инструменти освен съществуващите резултати от педиатричен еозинофилен езофагит (PEESS v2.0) и PedsQL. 5,6 пациенти с EoE имат хронични симптоми и могат да развият механизми за справяне с недооценяване на истинските симптоми. В бъдеще прецизната медицина може да бъде в състояние да насочи конкретно различни терапевтични режими въз основа на различни клинични, ендоскопски и хистологични характеристики на EoE; част от тази работа може да бъде информирана от наскоро описаните ендотипове на EoE. 7
Диагноза
Диагнозата EoE се прави въз основа на симптоми, ендоскопски характеристики, а хистологичните находки и EGD с биопсии се считат за диагностичен тест по избор. Общите ендоскопски характеристики включват лигавичен оток, загуба на съдов модел, линейни бразди, бели петна и концентрични пръстени. Тъй като лигавицата на хранопровода може да изглежда нормална при някои пациенти, наложително е при всички случаи да се вземат биопсии на лигавицата на хранопровода, тъй като в противен случай диагнозата може да бъде пропусната. Поради неравномерния характер на EoE се препоръчва да се вземат множество биопсии от проксимален и дистален хранопровод. Биопсиите от пациенти с EoE показват ≥15 интраепителни еозинофили на поле с висока мощност; други находки включват базалноклетъчна хиперплазия, удължаване на съдови папили, микроабсцеси на еозинофили и фиброза на собствената пластина. Важно е да се вземат предвид други състояния, като гастроезофагеален рефлукс, които могат да доведат до езофагеална еозинофилия. 8
Лабораторните и рентгенологичните тестове обикновено са с малка полза при оценката на пациентите с EoE. Контрастните изследвания на горната част на стомашно-чревния тракт не са достатъчно чувствителни, за да се открият фини промени в EoE, но могат да помогнат за идентифициране на алтернативна патология или усложнения на EoE като стриктура на хранопровода и хранопровод с малък калибър. Ролята на ендолуминалната функционална луминална образна диагностика (EndoFLIP®), ендоскопско средство, се изследва, за да се оцени разтегливостта на хранопровода за идентифициране на ранна фибростенотична болест. 9
Бъдещи указания/неудовлетворени нужди
Поради инвазивния характер на EGD, необходим за диагностика и мониторинг на заболяването, има търсене за намиране на неинвазивни биомаркери и базирани на офис минимално инвазивни тестове. Докато са изследвани няколко биомаркери като еозинофилни гранули протеини и еозинофилни повърхностни и вътреклетъчни маркери, данните са ограничени и трябва да бъдат отчетени различни променливи, включително съпътстваща атопия. В доказателство за концепция за изследване, урината 3-бромотирозин (3-BT) се различава между EoE и атопичните и неатопичните контроли. 10,11 Други тестове, които се изучават за диагностика и дългосрочно наблюдение на EoE, включват тест за нишка на хранопровода и тест за погълната цитоспонж, които потенциално могат да служат като минимално инвазивни инструменти за оценка на активността на заболяването; първоначалните данни показват добра корелация с езофагеалната еозинофилия. Неседираната трансназална ендоскопия в офиса може да осигури друг по-малко инвазивен метод за проследяване на заболяването. 12
Лечение
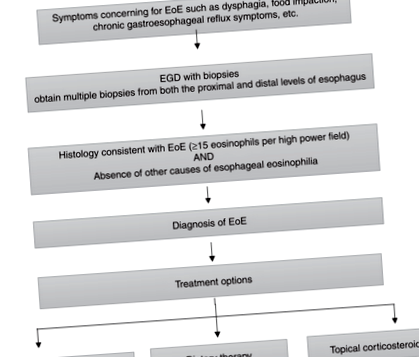
Лечението на EoE се състои от диетични, фармакологични и ендоскопски интервенции (фиг. 1). 8
Лечение на еозинофилен езофагит.
Диетична терапия
Диетичната модификация е ефективно лечение при значителен брой пациенти с EoE. Три диетични метода получиха широко признание: (1) емпирична елиминираща диета: тя се основава на емпирично елиминиране на най-често срещаните алергени. Елиминирането на четири храни е често използван подход, при който млечните продукти, соята, пшеницата и яйцата са емпирично елиминирани. Изследват се и по-нови подходи с „засилена” емпирична диета; (2) елементарна диета: при този режим всички храни се заменят с елементарна формула на основата на аминокиселина; (3) целенасочена елиминационна диета: това включва елиминиране на храни въз основа на тестване за алергия, въпреки че диагностичната точност може да бъде проблем поради фалшиво положителни и фалшиво отрицателни резултати от теста.
Съответствието и хранителните дефицити, свързани с тези диетични подходи, могат да бъдат предизвикателство и е важно внимателното проследяване с опитен диетолог.
Фармакологична терапия
Инхибиторите на протонната помпа (PPI) са важен вариант за фармакологично лечение на EoE. В допълнение към свойствата на потискане на киселината, PPI имат противовъзпалителни свойства, които оказват влияние върху патобиологията на EoE. Доскоро се препоръчваше 8-седмично изпитване на високи дози PPI с последващо EGD за пациенти с езофагеална еозинофилия и отговорилите бяха наричани езофагеална еозинофилия, отговаряща на PPI (PPI-REE). Наскоро преработените насоки вече не налагат такова проучване преди установяването на диагнозата EoE, а по-скоро позиционират PPI като начин на лечение за EoE. 13
Локалните глюкокортикоиди (TCS), включително будезонид и флутиказон, са други фармакологични възможности и двете са ефективни за подобряване на симптомите и хистологията при пациенти с EoE. За доставяне на тези лекарства са използвани различни методи за приложение, включително като вискозна суспензия, инхалатор с дозирана доза и ефервесцентна таблетка. Възможните неблагоприятни ефекти на локалните кортикостероидни препарати включват локален кандидозен свръхрастеж, потискане на надбъбречната ос и потискане на височината на скоростта. Нито една от фармакологичните терапии не е одобрена от Администрацията по храните и лекарствата (FDA); Европейската агенция по лекарствата (EMA) одобри перорален препарат на будезонид, Jorveza®, за възрастни с EoE.
Ендоскопска терапия
Ролята на ендоскопията при лечението на EoE обикновено се ограничава до управление на усложнения като премахване на въздействието на храната или разширяване на езофагеалните стриктури, които не реагират на медицинската терапия. Рецидивът е сравнително чест след дилатация, особено ако дилатацията се използва като единствен начин за лечение. Проучване при възрастни с резултати от разширяване на хранопровода съобщава, че 58% от пациентите се нуждаят от втора дилатация, като повечето (75%) изискват в рамките на 1 година. 14.
Бъдещи указания/неудовлетворени нужди
Множество локални кортикостероидни препарати, включително вискозна суспензия на будезонид и разтварящи се таблетки флутиказон, се изследват в EoE, за да помогнат за по-лесното приложение на лекарства. Няколко биологични лекарства, насочени към интерлевкин (IL) -5 (меполизумаб и реслизумаб), IL-13 (лебрикизумаб), IL-4 и IL-13 (дупилумаб) се изследват като потенциално лечение за EoE. 15 Омализумаб, IgE моноклонално антитяло, не подобрява ендоскопските или хистологичните характеристики при пациенти с EoE. 16 По-нататъшни изследвания могат също да оценят тяхната роля при лечението на огнеупорен EoE.
Поддържаща терапия, естествена история и дългосрочни усложнения
Няма ясен консенсус относно подходящия режим на поддържане на EoE, хронично състояние, което често се повтаря при пациент, който прекратява лечението. По принцип е необходимо да се поддържа поддържащо лечение, независимо дали се избягват хранителни причини или фармакологично, за да се поддържа ремисия.
Познанията за естествената история на EoE са ограничени и много аспекти, включително стратификация на усложненията, са непълно дефинирани. Има обаче данни в подкрепа на това, че хроничното, неразрешено възпаление води до структурно увреждане на хранопровода, което води до фиброза, стриктури и нарушена функция на хранопровода с течение на времето. Това подчертава значението на ранната диагностика и необходимостта от поддържаща терапия.
Бъдещи указания/неудовлетворени нужди
EoE е субект, който до голяма степен е бил непознат до преди около 2-3 десетилетия; следователно нашето разбиране за различни аспекти от естествената му история е все още в зародиш. За да се разберат тези аспекти са необходими по-перспективни, дългосрочни изследователски изследвания, основани на резултатите. По-доброто разбиране на естествената история, патогенезата и въздействието на сегашните лечения върху прогресията на болестта ще помогне за оформянето на бъдещата клинична практика.
Препратки
Arias, A. et al. Систематичен преглед с мета-анализ: честотата и разпространението на еозинофилен езофагит при деца и възрастни в популационни проучвания. Aliment Pharm. Тер. 43, 3–15 (2016).
Dellon, E. S. & Hirano, I. Епидемиология и естествена история на еозинофилен езофагит. Гастроентерология 154, 319–332.e3 (2018).
Benninger, M. S. et al. Разпространение на атопичната болест при пациенти с еозинофилен езофагит. Международна Форум Алергия Ринол. 7, 757–762 (2017).
Кумар, С., Чой, С. и Гупта, С. К. Еозинофилен езофагит - грунд за отоларинголози. ДЖАМА Отоларингол. Head Neck Surg. 145, 373–380 (2019).
Martin, L. J. et al. Резултатите от симптомите на педиатричния еозинофилен езофагит (PEESS v2.0) идентифицират хистологични и молекулярни корелати на основните клинични характеристики на заболяването. J. Allergy Clin. Имунол. 135, 1519–28.e8 (2015).
Franciosi, J. P. et al. Модул за еозинофилен езофагит на PedsQL: осъществимост, надеждност и валидност. J. Педиатър. Гастроентерол. Nutr. 57, 57–66 (2013).
Shoda, T. et al. Класификация на ендотип на еозинофилен езофагит чрез молекулярни, клинични и хистопатологични анализи: проучване в напречно сечение. Lancet Gastroenterol. Хепатол. 3, 477–488 (2018).
Dellon, E. S. et al. Клинични насоки за ACG: доказан подход, основан на диагностика и лечение на езофагеална еозинофилия и еозинофилен езофагит (EoE). Am. J. Gastroenterol. 108, 679–692 (2013). 693.
Menard-Katcher, C. et al. Влияние на възрастта и еозинофилния езофагит върху разтегливостта на хранопровода в педиатрична кохорта. Am. J. Gastroenterol. 112, 1466–1473 (2017).
Cunnion, K. M. et al. Количествена количествена кинетика на еозинофилите: нов анализ за оценка на еозинофилен езофагит. Ан. Алергия Астма Имунол. 116, 435–439 (2016).
Hines, B. T. et al. Минимално инвазивни изследвания на биомаркери при еозинофилен езофагит: систематичен преглед. Ан. Алергия Астма Имунол. 121, 218–228 (2018).
Hiremath, G. & Gupta, S. K. Обещаващи условия за идентифициране и наблюдение на еозинофилен езофагит. Clin. Гастроентерол. Хепатол. 15, 1655–1664 (2017).
Dellon, E. S. et al. Актуализирани международни консенсусни диагностични критерии за еозинофилен езофагит: Сборник от конференцията AGREE. Гастроентерология 155, 1022–1033.e10 (2018).
Runge, T. M. et al. Резултати от езофагеална дилатация при еозинофилен езофагит: безопасност, ефикасност и персистиране на фибростенотичния фенотип. Am. J. Gastroenterol. 111, 206–213 (2016).
Pesek, R. D. & Gupta, S. K. Нови лекарства за еозинофилен езофагит. Становище на експерта. Emerg. Наркотици 23., 173–183 (2018).
Rocha, R. et al. Омализумаб при лечението на еозинофилен езофагит и хранителна алергия. Евро. J. Педиатър. 170, 1471–1474 (2011).
Благодарности
S.K.G. се подкрепя отчасти от CEGIR (U54 AI117804), който е част от мрежата за клинични изследвания за редки болести (RDCRN), инициатива на Службата за изследвания на редки болести (ORDR), NCATS, и се финансира чрез сътрудничество между NIAID, NIDDK и NCATS. CEGIR се подкрепя и от групи за застъпничество на пациенти, включително Американско партньорство за еозинофилни разстройства (APFED), Кампания за насърчаване на изследванията за еозинофилни болести (CURED) и Коалиция за еозинофилни семейства (EFC).
Информация за автора
Принадлежности
Детска болница "Възнесение Сейнт Джон Провидънс", Детройт, Мичиган, САЩ
Катедра по отоларингология и подобряване на комуникацията, Медицинско училище в Харвард, Бостън, Масачузетс, САЩ
Секция по детска гастроентерология, хепатология и хранене, Университет на Илинойс Медицински колеж в Пеория/Детска болница в Илинойс, 530 NE Glen Oak Avenue North Building, стая 6646, Пеория, Илинойс, САЩ
Сандип К. Гупта
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Вноски
Всеки автор се е запознал с Педиатрични изследвания изисквания за авторство.
Автора за кореспонденция
Етични декларации
Конкуриращи се интереси
S.K.G. служи като консултант на Adare Pharmaceuticals Inc, Allakos, Abbott Laboratories, Gossamer Bio, QOL Medical LLC и Receptos, Inc. Той също така получава изследователска подкрепа от Shire Pharmaceuticals.
Допълнителна информация
Бележка на издателя Springer Nature остава неутрален по отношение на юрисдикционните претенции в публикувани карти и институционални принадлежности.
- Зъбна ерозия и диета Управление на денталната ерозия Настоящо разбиране и бъдещи насоки
- Текущо състояние на затлъстяването в детска и юношеска възраст Разпространение, етиология, съпътстващи заболявания и
- Прогресия на заболяването и резултати от бременността при жени с еозинофилен езофагит -
- Клинично представяне и подход към диетичното управление на еозинофилен езофагит
- Еозинофилен езофагит Член