Константин Петрухин
Катедра по офталмология, Колумбийски университет, Ню Йорк, Ню Йорк 10032
Резюме
Свързаната с възрастта макулна дегенерация (AMD) е водещата причина за слепота в западния свят. Няма одобрено от FDA лечение за най-разпространената суха (атрофична) форма на AMD. Дегенерацията на фоторецепторите при сухо AMD се предизвиква от аномалии в пигментния епител на ретината (RPE). Предполага се, че прекомерното натрупване на флуоресцентен липофусцинов пигмент в RPE представлява важен патогенен фактор в етиологията и прогресията на сухото AMD. Цитотоксичните липофусцин бисретиноиди, като А2Е, се образуват в ретината по неензимен начин от ретиноиди на зрителния цикъл. Инхибирането на производството на токсичен бисретиноид в ретината изглежда е добра стратегия за лечение на сухо AMD. В този преглед обсъждаме следните класове фармакологични лечения, инхибиращи образуването на липофусцин бисретиноиди в ретината: директни инхибитори на ключови ензими на зрителния цикъл, RBP4 антагонисти, първични амин-съдържащи алдехидни капани и деутерирани аналози на витамин А.
Въведение
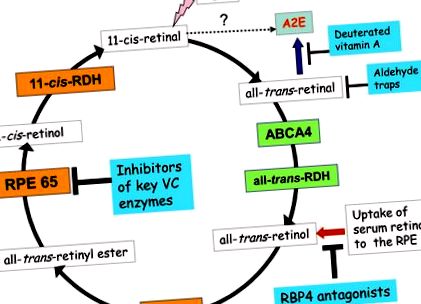
Ензимите и транспортерите, улесняващи реакциите на зрителния цикъл във външните сегменти на фоторецептора, са маркирани в зелено. Ензимите, катализиращи реакциите на зрителния цикъл, проведени в RPE, са показани в оранжево. Биосинтезата на липофусцин бисретиноид започва, когато изцяло транс-ретината напусне зрителния цикъл и не ензимно реагира с фосфатидилетаноламин, образувайки предшественика А2Е, А2-РЕ (синя стрелка); Също така се съобщава, че 11-цис-ретината е предшественик на образуването на А2Е [30] (пунктирана стрелка). Приемането на серумен ретинол до RPE (червена стрелка) подхранва зрителния цикъл. В ярко синьо са подчертани четири точки за потискане на образуването на бипоретиноид на липофусцин: инхибиране на ключови ензими на зрителния цикъл като RPE65, неутрализиране на свободните алдехиди, потискане на образуването на бисретиноиди с деутерирани аналози на витамин А и намаляване на поемането на ретинол към ретината с RBP4 антагонисти. Съкращения: ABCA4, специфичен за ретината ABC транспортер; изцяло транс-RDH, изцяло транс-ретинол дехидрогеназа; LRAT, лецитин-ретинол ацилтрансфераза; 11-цис-RDH, 11-цис-ретинол-дехидрогеназа.
A, Структура на инхибитора RPE65 ACU-4429, както може да се заключи от заявката за патент на САЩ 2011/0003895-A1. A1120 (B) и фенретинид (C) илюстрират класа на RBP4 антагонисти. Рацемичната смес от два първични амин-съдържащи пегабалинови стереоизомери (D) действа като алдехиден капан. Е, деутериран C20-D3 аналог на витамин А под формата на ретинилацетат.
Въпреки че съществуват допълнителни лечебни подходи за инхибиране на натрупването на липофусцин в ретината [44–46], този преглед ще се съсредоточи върху четири класа съединения, които демонстрират предклинична ефикасност за инхибиране на образуването на бисретиноиди при животински модели на засилена липофусциногенеза на ретината.
Инхибитори на ключови ензими на зрителния цикъл
Теоретично, частично инхибиране на зрителния цикъл с последващо намаляване на образуването на бисретиноиди може да се постигне чрез понижаване на активността на други членове на зрителния цикъл, като 11-цис-ретинол дехидрогеназа (RDH5), лецитин-ретинол ацилтрансфераза (LRAT) ) или клетъчен ретиналдехид-свързващ протеин (CRALBP). Специфични антагонисти на RDH5, LRAT и CRALBP тепърва ще бъдат разработени.
Антагонисти на ретинол-зависимото взаимодействие RBP4-TTR
Алдехидни капани
Индуцираната от светлина изомеризация на 11-цис ретината до atRAL и освобождаването на изцяло транс-ретината от опсин е критична стъпка в визуалната трансдукция на сигнала. Ако приемем, че atRAL представлява основен източник за не-ензимно образуване на A2E и други бисретиноиди в ретината, се предполага, че неутрализацията на atRAL чрез образуването на адукти на Schiff base с използване на първични амин-съдържащи лекарства може да намали биосинтеза на липофусцин бисретиноиди и да подобри други аспекти на алдехидната токсичност в ретината [41]. Няколко одобрени от FDA лекарства, съдържащи първични амини, показват ефикасност на фоторецепторна защита при острия индуциран от светлина Abca4 -/- Rdh8 -/- модел на мишка [41], при който фоторецепторната дегенерация се медиира от масивното индуцирано от светлина освобождаване на atRAL. Едно от тестваните съединения, A20 (Фигура 2, D), представлява агонист на рецептора на у-аминомаслена киселина прегабалин (Lyrica). A20 предоставя значителна защита на ретината в парадигмата за остро увреждане на светлината при мишки Abca4 -/- Rdh8 -/- при две тествани дози, 0,5 mg/мишка (
16 mg/kg) и 2 mg/мишка (
Деутерирани форми на витамин А
Заключения
ПРИЗНАВАНИЯ
Това проучване беше подкрепено от NIH Grants R21 NS067594, U01 NS074476, R24 EY019861, P30 EY019007 (Основна подкрепа за изследване на зрението) и неограничени средства от Research to Prevent Blindness (Ню Йорк, Ню Йорк) към Катедрата по офталмология, Колумбийския университет. Авторът благодари на Фондация "Семейство Бърч", Фонда за стипендии "Мери Джахарис-Джон Катсиматидис", Фондация "Каплен" и Фонда за очна хирургия за подаръци в подкрепа на това проучване.
Бележки под линия
Отказ от отговорност на издателя: Това е PDF файл на нередактиран ръкопис, който е приет за публикуване. Като услуга за нашите клиенти ние предоставяме тази ранна версия на ръкописа. Ръкописът ще бъде подложен на редактиране, набиране и преглед на полученото доказателство, преди да бъде публикуван в окончателния си вид. Моля, обърнете внимание, че по време на производствения процес могат да бъдат открити грешки, които биха могли да повлияят на съдържанието, и всички правни откази от отговорност, които се отнасят до списанието, се отнасят до.
Изявление за конфликт на интереси
Колумбийският университет притежава права на интелектуална собственост за офталмологична употреба на A1120 и неговите производни
- PTX Лична програма Физическо терапевтично упражнение
- Псориазис и метаболитен синдром Съпътстващи заболявания и екологични и терапевтични последици
- Фармакологично управление на въздействието на болуса върху хранопровода
- Ravenmark бич на Естелион; Преглед; Всичко, което един фен на стратегията може да иска; TouchArcade
- Стерол 14α-деметилаза като потенциална цел за инхибиране на ензима на антитрипанозомната терапия и