Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Ключова лаборатория по човешка функционална геномика, Дзянсу, Медицински университет в Нанкин, Нанкин, Дзянсу, Китай
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Училище за науки за живота, Китайски фармацевтичен университет, Нанкин, Китай
Училище за науки за живота, Китайски фармацевтичен университет, Нанкин, Китай
Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Кореспонденция: Китайски фармацевтичен университет, ул. Tongjiaxiang 24, Нанкин, Дзянсу 210009, Китай. Имейл: [email protected]
Кореспонденция: Китайски фармацевтичен университет, 639 Longmian Ave., Нанкин, Дзянсу 211198, Китай. Имейл: [email protected]
Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Училище за науки за живота, Китайски фармацевтичен университет, Нанкин, Китай
Ключова лаборатория за молекулярни и медицински биотехнологии Джиангсу, Колеж по науки за живота, Нормален университет в Нанкин, Нанкин, Китай
Кореспонденция: Китайски фармацевтичен университет, ул. Tongjiaxiang 24, Нанкин, Дзянсу 210009, Китай. Имейл: [email protected]
Кореспонденция: Китайски фармацевтичен университет, 639 Longmian Ave., Нанкин, Дзянсу 211198, Китай. Имейл: [email protected]
Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Ключова лаборатория по човешка функционална геномика, Дзянсу, Медицински университет в Нанкин, Нанкин, Дзянсу, Китай
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Училище за науки за живота, Китайски фармацевтичен университет, Нанкин, Китай
Училище за науки за живота, Китайски фармацевтичен университет, Нанкин, Китай
Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Кореспонденция: Китайски фармацевтичен университет, ул. Tongjiaxiang 24, Нанкин, Дзянсу 210009, Китай. Имейл: [email protected]
Кореспонденция: Китайски фармацевтичен университет, 639 Longmian Ave., Нанкин, Дзянсу 211198, Китай. Имейл: [email protected]
Джиангсу Ключова лаборатория за откриване на лекарства за метаболитни заболявания, Държавна ключова лаборатория за природни лекарства, Китайски фармацевтичен университет, Нанкин, Китай
Училище за науки за живота, Китайски фармацевтичен университет, Нанкин, Китай
Ключова лаборатория за молекулярни и медицински биотехнологии Джиангсу, Колеж по науки за живота, Нормален университет в Нанкин, Нанкин, Китай
Кореспонденция: Китайски фармацевтичен университет, ул. Tongjiaxiang 24, Нанкин, Дзянсу 210009, Китай. Имейл: [email protected]
Кореспонденция: Китайски фармацевтичен университет, 639 Longmian Ave., Нанкин, Дзянсу 211198, Китай. Имейл: [email protected]
РЕЗЮМЕ
СЪКРАЩЕНИЯ
МАТЕРИАЛИ И МЕТОДИ
Животни
Серологичен анализ
Кръвните проби се събират в нехепаринизирани епруветки и се центрофугират при 4000 об/мин за 10 минути при 4 ° С. Бяха събрани серуми и нивата на TG, TC, LDL-C и HDL-C бяха определени спектрофотометрично чрез използване на търговски комплекти, закупени от Института по биоинженерство в Нанкин Jiancheng (Нанкин, Китай).
Клетъчна култура
Първичните хепатоцити на мишки бяха изолирани от мишки, като се използва методът за перфузия на колагеназа IV (Thermo Fisher Scientific), както беше описано по-горе, и бяха култивирани в овлажнена атмосфера, която съдържаше 5% CO2 при 37 ° С (39). Миши AML-12 хепатоцити бяха култивирани в среда DMEM/F-12 (Thermo Fisher Scientific), която беше допълнена с инсулин-трансферин-селен (Thermo Fisher Scientific) и дексаметазон (40 ng/ml; Sigma-Aldrich). Всички експерименти за трансфекция бяха проведени в клетки AML-12, като се използва Lipofectamine 3000 (Thermo Fisher Scientific) в съответствие с инструкциите на производителя. За инвитро ОА обработка, запас, който съдържа 10 тМ ОА се приготвя чрез използване на стерилен DMSO.
Анализ на жизнеспособността на клетките
Анализът за токсичност CCK ‐ 8 се използва за анализ на потенциалните токсични ефекти на ОА върху жизнеспособността на първичните хепатоцити на мишки. Накратко, 1 × 104 клетки се посяват във всяка ямка на 96-ямкова плака и се култивират при 37 ° С за една нощ за прикрепване. След това клетките се прехвърлят в 100 ul среда, която съдържа или 0.1% DMSO или ОА при посочени концентрации и се инкубират в продължение на 24 часа. След това към всяка ямка се добавят 10 µl реагент WST ‐ 8 (EnoGene, Нанкин, Китай), смесват се със среда и се инкубират при 37 ° С в продължение на 2 часа. Накрая беше използван четец на микроплаки за измерване на абсорбцията при 450 nm.
Количествена RT ‐ PCR
Цялостната екстракция на РНК и количествената RT-PCR (qRT-PCR) бяха извършени, както е описано по-горе (40). Подробните последователности на грундовете бяха както следва: Pgc ‐ 1β: (напред) 5′ – GGCAGGTTCAACCCCGA – 3 ′; (назад) 5′ – CTTGCTAACATCACAGAGGATATCTTG – 3 ′; Фас (синтез на мастни киселини): (напред) 5′ – TCCTGGAACGAGAACACGATCT – 3 ′; (назад) 5′ – GAGACGTGTCACTCCTGGACTTG – 3 ′; Scd1 (стеароил-коензим А десатураза 1): (напред) 5′ – TTCTTACACGACCACCACCA – 3 ′; (назад) 5′ – GCAGGAGGGAACCAGTATGA – 3 ′; и 36В4: (напред) 5′ – GAAACTGCTGCCTCACATCCG – 3 ′; (назад) 5′ – GCTGGCACAGTGACCTCACACG ‐ 3 ′. Генът 36B4 се използва като вътрешен контрол. За количествено определяне на miRNA, наборите от изпъкнали miRNA qRT-PCR (един RT праймер и двойка qPCR праймери за всеки набор), които са специфични за miR-98-5p, са проектирани от RiboBio (Гуанджоу, Китай). miRNA изпъкналият цикъл беше обратно транскрибиран с реактивен комплект PrimeScript RT (Takara, Токио, Япония) и количествено определен чрез qPCR, използвайки SYBR Premix Ex Taq II (Takara), съгласно инструкциите на производителя. експресията на miRNA се нормализира до U6 snRNA, за да се получи относителното изобилие.
Уестърн блотинг
За анализ на протеини, чернодробни проби се лизират в RIPA буфер. Количествената концентрация на протеини е определена с BCA комплект за количествено определяне на протеини (Jiancheng). Равни количества протеин бяха заредени и разделени с 10% SDS-PAGE и след това прехвърлени върху PVDF мембрана (Millipore, Billerica, МА, САЩ). Мембраните се инкубират през нощта с подходящ първичен Abs при 4 ° С. След това свързаните Abs се визуализират с помощта на конюгиран вторичен Abs на конски пероксидаза. Абс срещу миши PGC-1β и FAS са закупени от ProteinTech (разреждане 1: 500; Чикаго, IL, САЩ). Ab срещу мишка SCD1 е получена от Santa Cruz Biotechnology (разреждане 1: 500; Santa Cruz Biotechnology, Dallas, TX, USA). Ab срещу глицералдехид 3-фосфат дехидрогеназа е закупен от Kangcheng Biotech (разреждане 1: 5000; Шанхай, Китай). Количествен анализ беше извършен в Western blot изображения с помощта на ImageJ софтуер (NIH).
Pgc ‐ 1β конструкция на промотор
Мишка Pgc ‐ 1β промотор (-793 до +100 bp) се амплифицира от геномната ДНК на мишката, като се използват следните праймери: (напред) 5'– AAGACGCGTGGTGGATGGCTGATTGGTGT – 3 ′; (назад) 5′ – GGACTCGAGATAGTTGAGGAAGAAGGACG ‐ 3 ′. Последователността беше валидирана чрез секвениране и клонирана в PGL3-основен вектор с използване Mluаз и XhoОграничавам сайтовете за намаляване на ензимите За репортерни тестове за луцифераза, 200 ng репортерни плазмиди са трансфектирани в AML-12 клетки. За всички трансфекции бяха използвани равни количества ДНК чрез добавяне на подходяща векторна ДНК. Тридесет и шест часа по-късно клетките бяха третирани със или без ОА за още 12 часа. Относителната активност на луциферазата се определя чрез използване на двойна луциферазна система (Promega, Madison, WI, USA). Данните са представителни за поне 3 независими експеримента.
анализ на разграждането на иРНК
Стабилността на Pgc ‐ 1β mRNA беше измерена чрез експерименти с преследване на α-amanitin (α-AMA). Първичните хепатоцити на мишки се инкубират в DMEM, който съдържа α-AMA (15 µM; Sigma-Aldrich) със или без OA (10 µM). Клетките се събират в посочените времеви точки и се подлагат на qRT-PCR анализ.
miRNA микрочипове и биоинформатични анализи
За идентифициране на miRNAs, които потенциално медиират ускоряването на Pgc ‐ 1β разграждане на иРНК, индуцирано от ОА, извършихме анализ на микроРНК на микроРНК (масив Affymetrix GeneChip miRNA 4.0; Gene Tech, Шанхай, Китай), като използвахме чернодробни проби, изолирани от мишки, получили остра инжекция на ОА. Когато се генерират данни, се използват уеб-базирани алгоритми за биоинформативно прогнозиране (miRanda и TargetScan) за избор на miRNAs, които са насочени Pgc ‐ 1β 3 ′ UTR регион.
Pgc ‐ 1β 3 ′ UTR конструкция за репортер на луцифераза
3 ′ UTR областта (536 nt) на мишката Pgc ‐ 1β cDNA, която съдържа 2 предполагаеми целеви места за miR ‐ 98-55p, се усилва чрез PCR, като се използват следните праймери: (напред) 5′ – GGCGGCTCGAGATATCAGCCTTAACCTTCG – 3 ′; (обратен) 5′ – AATGCGGCCGCAATCAGAGCCATAAATACA – 3 ′, вмъкнат между Xhoаз и НеОграничавам местата за рязане на ензими, непосредствено след гена на луциферазата във pmiR-RB-Report Vector (RiboBio). Генерирана е и версия с двоен мутант с мутация от 7 bp (TACCTCA, мутирала до AGTTAGT) от местата на перфектна комплементарност. Вложки от див тип (WT) и мутантни вложки бяха потвърдени чрез секвениране. За трансфекция, 200 ng WT или мутантни репортерни вектори бяха трансфектирани в AML-12 клетки заедно с miR-98-5p имитатори или инхибитори (проектирани и синтезирани от RiboBio). След това клетките се третират със или без OA (10 цМ) в продължение на 12 часа. Относителни луциферазни активности (съотношения на Ренила луциферазен сигнал, нормализиран до светулка луцифераза) се определят 48 часа след трансфекцията. Равни количества ДНК и имитатори/инхибитори бяха използвани за всички трансфекции чрез добавяне на подходящи вектори. Всички експерименти за трансфекция се извършват в три екземпляра.
Статистически анализ
Групите данни са представени като средни стойности ± sd. Данните бяха анализирани с помощта на еднопосочен ANOVA, последван от LSD на Fisher post hoc тест. Изчисленията бяха извършени с помощта на Origin 8 (версия 8.6; OriginLab, Northampton, MA, САЩ). Стойност на P
РЕЗУЛТАТИ
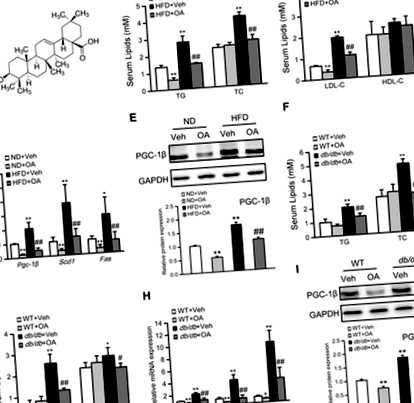
Острото и хронично лечение с ОА инхибира чернодробната експресия на PGC-1β
Инхибирането на PGC-1 β медиира редукцията на TG чрез OA
OA инхибира експресията на PGC-1β по автономен за клетките начин
Тъй като PGC ‐ 1β може да бъде стабилно регулиран от OA in vivo, след това изследвахме дали такава регулация съществува и в култивирани миши първични хепатоцити. Както е показано на допълнителна фигура S2, анализът на CCK ‐ 8 показва, че ОА не е токсичен за клетките, когато концентрацията е
OA ускорява Pgc ‐ 1β разграждане на иРНК
miR ‐ 98‐5p посредничи при индуцирана от OA Pgc ‐ 1β разграждане на иРНК
ДИСКУСИЯ
Въпреки че предишни проучвания показват, че природните агенти имат потенциала да регулират експресията на miRNA, повечето от тях са силно описателни и отчитат само ефектите от тези агенти върху нивата на експресия на miRNA - това е и ограничението на нашето проучване. В момента как OA регулира miR ‐ 98-5p все още не е известно. От една страна, като се има предвид, че експресията на miRNA може да бъде повлияна от епигенетични промени и че OA намалява нивата на фосфорилиране на хистон 3H, интересно е да се изследва дали OA влияе върху експресията на miRNA чрез епигенетични модификации (58). От друга страна, трябва да се отбележи, че пероралното приложение на ОА не е толкова ефективно, колкото интраперитонеално или подкожно инжектиране, що се отнася до инхибиране на възпалителните реакции, което предполага, че начинът на приложение е важен за ОА да упражнява своите фармакологични функции (59). Всъщност ниската разтворимост във вода е лоша in vivo бионаличността и неприемливият фармакокинетичен профил на природните агенти често ограничават тяхната ефикасност като терапевтични агенти (60). Следователно, разработването на синтетични аналози на OA въз основа на анализа на структурна активност и по-ефективния начин на приложение, като капсулиране на OA с липозоми или наночастици, е вълнуваща област на изследване.
В обобщение установихме, че хиполипидемичният ефект на ОА се медиира от оста miR-98-5p/PGC-1β при индуцирани от HFD хиперлипидемични мишки. Съобщава се, че ОА има и други благоприятни ефекти върху енергийния метаболизъм, като облекчаване на хипергликемия и инсулинова резистентност. Следователно това съединение е обещаващ агент, с който да се лекуват метаболитни нарушения, включително хиперлипидемия.
ПРИЗНАВАНИЯ
Тази работа е подкрепена от безвъзмездни средства от Националната програма за основни изследвания на Китай (програма 973; 2013CB911600), Националната фондация за естествени науки на Китай (31422028, 31271261, 31401009, 81373303, 81473080 и 81573299), Програма за десет хиляди таланти, Природна наука Фондация на провинция Дзянсу в Китай (BK20140041), Проект на срещата на върха на шест таланта, Проект на 333 таланта (BRA2015323), План за финансиране на докторски изследвания на Джиангсу (1601020A), Център за съвместна иновация за транслационна медицина на сърдечно-съдовите заболявания (Медицински университет в Нанкин) и Приоритетната академична академия Развитие на програмата на висшите учебни заведения от Дзянсу. Авторите не декларират конфликт на интереси.
ВНОСКИ НА АВТОРА
S. Chen, J. Liu и C. Liu са проектирали изследвания; S. Chen, X. Wen и W. Zhang извършиха изследването; S. Chen, X. Wen, J. Liu и C. Liu анализираха данните; C. Wang и J. Liu осигуриха реактиви; и S. Chen и C. Liu са написали статията.
- Как да контролираме високите нива на триглицеридите и пикочната киселина
- Високите нива на олово по време на бременност, свързани с детското затлъстяване Фолиевата киселина може да намали риска от затлъстяване
- Високи дози фолиева киселина в периконцептивния период и риск от ниско тегло за гестационна възраст
- Диетата с високо съдържание на киселини може да има отрицателни ефекти върху здравето на бъбреците - ScienceDaily
- Високите нива на пикочна киселина при малки деца могат да доведат до по-високо кръвно налягане по-късно - ScienceDaily