- Erratum към тази статия е публикуван в Nutrition Journal 2017 16: 8
Резюме
Заден план
Целта на този доклад е да се обсъди въпросът за хранителната терапия при пациенти, приемащи варфарин. На пациентите често се предписват диети без витамин К, без консултации по хранене, което води до възможни последици за здравето.
Представяне на дело
На 52-годишна жена със затлъстяване и хипертония е предписана нискокалорична диета от нейния семеен лекар в опит да насърчи загубата на тегло. След белодробна емболия тя е поставена на антикоагулантна терапия и при изписване от болницата й е предписана диета без витамин К, за да се избегнат взаимодействия. Предвид лошия контрол върху нейната антикоагулантна терапия, тя беше насочена към амбулаторната служба на нашето хранително звено.
Заключения
Този случай илюстрира значението на задълбочената медицинска оценка на храненето при лечението на пациенти със затлъстяване и необходимостта от промяна в диетичния подход на хранителната терапия при управлението на антикоагулантната терапия с витамин К. При пациенти, приемащи варфарин, данните сочат, че целта на хранителната терапия трябва да бъде поддържането на постоянен прием на витамин К в храната.
Заден план
Редица проучвания са установили значително повишен риск от дълбока венозна тромбоемболия (ВТЕ) и/или белодробна емболия при хора със затлъстяване [1–6]. Съотношение на риск от 2,7 за индекс на телесна маса> 40 е съобщено от Риск за атеросклероза в общностите (ARIC) и Сърдечно-съдово здравно проучване (CHS) [2].
Освен затлъстяването, много други фактори допринасят за увеличаване на риска от ВТЕ: тютюнопушене, увеличаване на възрастта, пациенти с фактор V Leiden или протромбинова генна мутация [7] и орална контрацептивна терапия [8].
Пациентите, които са имали VTE епизод, обикновено се лекуват с перорални антикоагуланти. Използването им е предизвикателство, тъй като терапевтичният обхват е тесен и дозирането се влияе от множество фактори, включително генетични вариации, лекарствени взаимодействия и диета [9]. Освен това, в сравнение с нормалното тегло, пациентите със затлъстяване и патологично затлъстяване са имали намален първоначален отговор на варфарин [10, 11].
Протромбиновото време е тест за оценка на външния път на коагулация. Международното нормализирано съотношение (INR) се използва за стандартизиране на протромбиновото време и оптималната интензивност на антикоагулантната терапия съответства на целевата INR от 2,5 (диапазон, 2,0 до 3,0) [12].
Както профилактиката, така и лечението на ВТЕ и белодробната емболия (РЕ) с антикоагуланти са свързани със значителни рискове от големи и фатални кръвоизливи. Както антикоагулантното лечение, така и промените в начина на живот трябва да бъдат индивидуализирани, за да се предотвратят допълнителни усложнения [9, 12].
Два основни фактора, които могат да доведат до лош контрол на INR, са неприемането на варфарин по подходящ начин и много ниският прием на витамин К в храната/дефицит на витамин К. Следователно храненето на тези пациенти е изключително сложно.
С настоящото описваме случай на белодробна емболия при затлъстял пациент, предоставящ ключови идеи за лечението с медицинска хранителна терапия и антикоагуланти.
Представяне на дело
Стационарна диагностика и лечение
През януари 2015 г. 52-годишна жена със затлъстяване и хипертония беше приета в кардиологичното отделение на болница в Северна Италия за остра диспнея и болки в гърдите. Компютърната томография ангиография разкрива дефекти на пълнене, засягащи десния и левия клон на белодробната артерия, предполагащи белодробна емболия (РЕ). Първоначално тя е била лекувана с интравенозен натриев хепарин и е свързана с варфарин като дългосрочен антикоагулант. Преди изписването от болницата й е предписана диета без витамин К, посочена в таблица 1 (b). Въпреки че общата препоръка е да се поддържа стабилен и последователен прием на витамин К, в клиничната практика се препоръчва на пациентите да избягват храна с високо съдържание на витамин К и им се дават общи диетични насоки.
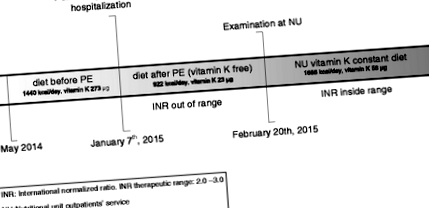
По време на първия й месец като амбулаторен пациент беше много трудно да получи нейния INR в терапевтичния диапазон. Нейният семеен лекар признава, че лошото хранене е важен фактор за установяване на терапевтични нива и тя е насочена към нашата амбулаторна служба за хранителна единица (NU) за хранителна оценка и специфична медицинска хранителна терапия. Фигура 1 показва графика на настоящото заболяване, интервенция и проследяване.
Амбулаторна хранителна единица
Медицинска история
Тя съобщава за дългогодишна история на затлъстяване и хипертония. Тя отрече алергии и пушене на цигари и съобщи за заседнал начин на живот без физическа активност. Пациентката е била в раждане и е била на орална контрацептивна терапия от 25-годишна възраст. Терапията е прекратена от нейните лекари след нейното РЕ. По време на прегледа тя е била на небиволол, алпразолам и варфарин, коригирани за INR, както и добавки с витамин В12 и фолиева киселина (400 μg). Семейната й история е отрицателна за тромбоза и сърдечно-съдови заболявания.
История на теглото
Пациентката съобщава, че тя е започнала да се бори със затлъстяването през детството си. Тя започва зряла възраст с тегло 90 кг (ИТМ 35,0 кг/м 2). Максималното и минималното тегло, съобщени от пациента, са 117,5 kg (BMI 45,9 kg/m 2) и 69 kg (BMI 27,0 kg/m 2) съответно на 51 и 26 годишна възраст. Скоро след достигане на върховото си тегло тя започва хипокалорична диета, както е предложено от нейния семеен лекар, Таблица 1 (а).
Хранителна оценка
Антропометрични, биоелектрични и клинични находки при физикален преглед са показани в таблица 2 с биохимични анализи. ИТМ на пациента е над 34,99 Kg/m 2, клас II затлъстяване съгласно класификацията на СЗО [13]. Мастната маса се изчислява чрез анализ на биоелектричния импеданс (BIA) с помощта на BIA 101 Akern s.r.l. (Италия). Изпитът, извършен при стандартизирани условия [14], разкрива важно увеличение на мастната маса, макар и нормално състояние на хидратация. Съотношението между талията и ханша показва разпределение на мазнините в Android. Доказателствата за увеличаване на висцералната мастна тъкан се показват чрез измерване на обиколката на талията.
Разходът на енергия в покой (REE) е оценен посредством прогнозни уравнения на Mifflin [15], което е по-вероятно от другите известни уравнения да оценят REE с точност до 10% [16].
Преди PE, пациентът е спазвал диетата, посочена в таблица 1 (а), която е предписана от нейния семеен лекар. Общият прием на енергия и хранителни вещества е анализиран от обучени диетолози, използвайки специален софтуер, разработен от нашия отдел по хранене, включващ „База данни за състава на храните за епидемиологични изследвания в Италия“ от Gnagnarella P, Salvini S, Parpinel M. (Версия 1.2015 Уебсайт http: //www.bda -ieo.it/).
Диетата, следвана от пациента преди PE, е нискокалорична диета, която не отговаря на диетичните препоръки за прием на протеини и микроелементи (LARN 2014) [17].
Хранителният състав на диетата, предписана на пациента след ПЕ при изписване от болницата, се отчита в Таблица 1 (б).
Диетите без витамин К обикновено липсват в зеленчуците, а след това недостатъчен прием на диетични фибри и фолиева киселина. Приемът на протеин, предписан на пациента, е далеч по-нисък от всяка стандартна препоръка (по-малко от 0,33 g/kg телесно тегло), докато общите мазнини и по-специално наситените са по-високи от стандартните препоръки (LARN 2014 и ESC 2012 [18]).
Лабораторните стойности на пациента по време на първия й преглед в нашата НУ са показани в Таблица 2. Тя е имала високи нива на хомоцистеин и ниски преалбумин. Тя също е с дефицит на витамин D, както може да се наблюдава при пациенти със затлъстяване [19].
Концентрациите както на фолиева киселина, така и на витамин В12 са в рамките на приетите нормални граници, вероятно поради нейната добавка, а не от приема на диета.
Терапевтична интервенция
След хранителната оценка беше предписана балансирана, нискокалорична диета, с особено внимание към приема на натрий и разтворими въглехидрати. Предписаният прием на протеин е еквивалентен на 0,8 g/Kg от действителното телесно тегло. Хранителният състав на диетата, предписан в нашата НУ, е показан в Таблица 1 (в).
За да се избегне рязка промяна в приема на витамин К, предписаният прием на витамин К е бил нисък (57,88 μg на ден). Постепенно приемът на витамин К се увеличава до 150 μg на ден. Предписана е добавка на фолиева киселина (400 μg на ден), както и добавка на витамин D (300 000 IU на всеки 3 месеца в продължение на 9 месеца) [20].
Ползата от това да я видят в НУ беше, че нашият персонал успя да отдели подходящо време, за да консултира пациента и да се увери, че разбира хранителните насоки и риска от усложнения, за да трансформира придобитите знания в промяна в поведението и да постигнете по-голямо придържане.
Последващи действия и резултати
Стойностите на INR на пациента бяха тествани редовно. Както е показано в таблица 3, стойностите на INR са терапевтични и остават постоянни веднага след започване на предписаната диета.
Заключение
Това казус представя хранителните проблеми на антикоагулантите в условията на затлъстяване. Представяме случай на 52-годишна пациентка със затлъстяване и хипертония, приемаща антикоагуланти поради анамнеза за скорошно ПЕ, лекувано в нашата амбулаторна служба в НУ.
Тя не е имала наследствена тромбофилия, нито предишна хоспитализация, обездвижване, травма, операция, злокачествено заболяване или инфекция преди PE и ние предполагаме, че може би това нежелано събитие може да е било причинено от комбинацията от затлъстяване, орална контрацептивна терапия и заседнал начин на живот. В действителност има сериозни доказателства, че оралните контрацептиви водят до статистически значим риск от ВТЕ, който е особено висок сред жените с високи индекси на телесна маса и анамнеза за тютюнопушене [21, 22]. Предишни проучвания показват, че оралните контрацептиви променят ефекта на затлъстяването върху риска от венозна тромбоза, с 10-кратно повишен риск сред жените при орални контрацептиви с ИТМ> 25 kg/m 2 в сравнение с жени с нормално тегло, които не използват орални контрацептиви [8, 23].
Затлъстяването се счита за рисков фактор за VTE и PE и е свързано с повишаване на прокоагулантните фактори (фактор VII, фактор VIII, фактор XII и фибриноген) [24-26] и с венозен застой [2], от своя страна увеличаващ тромботичния риск ( Триадата на Вирхов). Анализът на данните от Националното проучване за освобождаване от болница показва повишен относителен риск за VTE (RR 2.50, 95 CI 2.492.51) и PE (RR 2.21, 95% CI 2.202.23) при лица със затлъстяване [27].
Пациентката ни съобщи за дълга история на затлъстяване и 7 месеца преди епизода на ПЕ беше поставена на нискокалорична диета без официална хранителна оценка на специфичните й хранителни нужди.
Както е показано в таблица 1, диетата преди PE не е задоволила нуждите на фибри, протеини и микроелементи за този пациент вероятно поради ниския прием на плодове и зеленчуци.
Освен това и двете диети преди и след PE са били с много висок прием на натрий, което би било неподходящо при пациент с дълга история на хипертония. Нашият пациент също имаше хиперхомоцистеинемия, въпреки добавянето на витамин В12 и фолиева киселина. Високата плазмена концентрация на хомоцистеин може да се дължи на генетични дефекти в ензимите, участващи в метаболизма на хомоцистеина (т.е. хомозиготност за термолабилния вариант на метилен тетрахидрофолат редуктазата, MTHFR -TT генотип), хранителни дефицити във витаминните кофактори (фолат, витамин В6 и витамин В12). [29–32]) или други фактори, включително някои лекарства като орални контрацептиви. Като се има предвид липсата на мутация на MTHFR, най-вероятно нейната хиперхомоцистеинемия се дължи както на дългосрочната орална контрацептивна терапия, така и на диета с ниско съдържание на фолиева киселина. Тъй като са демонстрирани протромботични ефекти на хомоцистеин [33–36], важно е този параметър да бъде включен в хранителната оценка. Всъщност правилната оценка на пациентите със затлъстяване трябва да включва витаминния статус, особено при тези, изложени на риск от субклинични дефицити.
Този случай илюстрира необходимостта от задълбочена оценка на медицинското хранене при лечението на пациенти със затлъстяване. Терапията за отслабване не може да се фокусира само върху намаляване на калориите, но трябва да включва грижа за спазване на препоръките за макро и микроелементи, дори чрез добавки, ако е необходимо.
Диета без витамин К, като Таблица 1 (b), много често се предписва на пациенти, които са имали ПЕ и са на варфарин. Хората, приемащи варфарин, обикновено са чувствителни към колебанията в приема на витамин К и адекватният контрол на INR изисква внимателно внимание на количеството витамин К, погълнато от хранителни и други източници [37]. Този доклад за случая подчертава необходимостта от промяна в клиничния подход на пациентите, приемащи варфарин. Целта на хранителната терапия трябва да бъде да поддържа постоянния прием на витамин К с храната, вместо да го изключва напълно от диетата, което не е необичайно в клиничната практика. Няколко проучвания демонстрират връзката между приема на витамин К и контрола на INR [38–40], по-специално предполага, че пациентите трябва да бъдат съветвани да се хранят здравословно и да не избягват плодове и зеленчуци от страх да не променят INR.
Въпреки доказателствата, обичайната практика е да се предлагат диети без витамин К на всички пациенти на орална терапия с антикоагуланти. Основната последица от тази препоръка е изключването на зеленчуци и плодове от диетата, което води до недостиг на хранителни вещества и влошено здравословно състояние. Не трябва да забравяме, че премахването на тези много важни групи храни излага нашите пациенти на допълнителен риск.
В областта на сърдечно-съдовия риск и заболявания, терапията с медицинско хранене играе решаваща роля за осигуряване както на профилактика, така и на терапия. Правилната и пълна хранителна оценка е от съществено значение за ефективната терапия. Хранителната намеса трябва да бъде съобразена с индивидуалния пациент и трябва да осигури правилното количество макронутриенти, микроелементи и добавки с витамини или минерали, ако е необходимо.
- Следоперативна хранителна подкрепа на пациента с чревна гангрена - доклад за случая Journal of Health
- Хранително управление при детско затлъстяване
- Хранителна и метаболитна модулация при управление на хронична обструктивна белодробна болест Европейски
- Нощното изпотяване като ярък симптом на пациента, представящ се с белодробна емболия
- Затлъстяване и медийно обучение на пациентите UCSF Benioff Детска болница