Нурул Айни Мохд Азман
1 Катедра по химическо инженерство, Технически университет в Каталуния, Avinguda Diagonal 647, Барселона 08028, Испания; moc.liamg@namzainia (N.A.M.A.); [email protected] (M.G.G.); moc.liamg@jfaivoges (F.S.)
2 Факултет по химически и природни ресурси, Университет Малайзия Паханг, Lebuhraya Tun Razak, Паханг 26300, Малайзия; ym.ude.pmu@aneerus (S.A.); ym.ude.pmu@adylahs (S.M.S.)
Мария Габриела Галего
1 Катедра по химическо инженерство, Технически университет в Каталуния, Avinguda Diagonal 647, Барселона 08028, Испания; moc.liamg@namzainia (N.A.M.A.); [email protected] (M.G.G.); moc.liamg@jfaivoges (F.S.)
Франциско Сеговия
1 Катедра по химическо инженерство, Технически университет в Каталуния, Avinguda Diagonal 647, Барселона 08028, Испания; moc.liamg@namzainia (N.A.M.A.); [email protected] (M.G.G.); moc.liamg@jfaivoges (F.S.)
Сурина Абдула
2 Факултет по химически и природни ресурси, Университет Малайзия Паханг, Lebuhraya Tun Razak, Паханг 26300, Малайзия; ym.ude.pmu@aneerus (S.A.); ym.ude.pmu@adylahs (S.M.S.)
Shalyda Md Shaarani
2 Факултет по химически и природни ресурси, Университет Малайзия Паханг, Lebuhraya Tun Razak, Паханг 26300, Малайзия; ym.ude.pmu@aneerus (S.A.); ym.ude.pmu@adylahs (S.M.S.)
Мария Пилар Алмаджано Паблос
1 Катедра по химическо инженерство, Технически университет в Каталуния, Avinguda Diagonal 647, Барселона 08028, Испания; moc.liamg@namzainia (N.A.M.A.); [email protected] (M.G.G.); moc.liamg@jfaivoges (F.S.)
Резюме
Обикновената мечо грозде (Arctostaphylos uva-ursi L. Sprengel) е вездесъщ вечнозелен храст, разположен в Северна Америка, Азия и Европа. Плодовете са почти безвкусни, но растението съдържа висока концентрация на активни съставки. Антиоксидантната активност на екстракт от листа на мечо грозде в теста за радикални катиони на 2,2′-азино-бис-3-етилбензотиазолин-6-сулфонова киселина (ABTS) е 90,42 mmol еквиваленти на Trolox/g сухо тегло (DW). Извличането на способността на метаноловия екстракт от листа от мечо грозде срещу метокси радикали, генерирани в реакцията на Фентън, се измерва чрез електронен парамагнитен резонанс. Окисляването на липидите се забавя в емулсия масло-вода чрез добавяне на 1 g/kg лиофилизиран екстракт от мечо грозде. Също така, 1 g/kg лиофилизиран екстракт от мечо грозде, включен във филм на основата на желатин, показва висока антиоксидантна активност, за да забави разграждането на липидите в мускулните храни. Настоящите резултати показват потенциала на екстракт от листа от мечо грозде за използване като естествен хранителен антиоксидант.
1. Въведение
Окисляването на липидите в храната причинява сериозни проблеми, които водят до кратък срок на годност и загуба на хранителни качества [1]. Синтетичните антиоксиданти като бутилиран хидроксианизол (BHA), бутилиран хидрокситолуен (BHT) и трет-бутилхидрохинон (TBHQ) са били използвани като антиоксиданти в много хранителни продукти [2], но потребителите са загрижени за възможните токсикологични ефекти и често предпочитат естествените антиоксиданти за храни, консумирани като част от здравословна диета. По този начин много разследвания са фокусирани върху идентифицирането на нови антиоксиданти, които да бъдат тествани в моделни храни като емулсии и включени в опаковъчни филми.
Естествените антиоксиданти съдържат висока концентрация на фенолни съединения и обикновено се срещат в плодовете, зеленчуците и билките [3,4]. Мечото грозде (Arctostaphylos uva-ursi L. Sprengel) е вездесъщ вечнозелен храст, разположен в Северна Америка, Азия и Европа. Плодовете са почти безвкусни, въпреки че съдържат висока концентрация на активни съставки в много търговски продукти [5]. Антиоксидантният потенциал на листата от мечо грозде (BL) е изследван чрез множество химични анализи, включително анализ за намаляване на мощността, активност на извличане на радикали с помощта на 2,2-дифенил-1-пикрилхидразил (DPPH), липозомен модел, извличане на хидроксилни радикали (HO) и линолова киселина киселинна моделна система [6,7]. Основните съставки на BL са гликозидите арбутин (5% –15%), метиларбутин (до 4%) и малки количества от свободните агликони. Други съставки включват урсолова киселина, танинова киселина, галова киселина, р-кумарова киселина, сиринг киселина, галоиларбутин, гало-танини и флавоноиди, по-специално гликозиди на кверцетин, кемпферол и мирицетин [8]. Следите от полифеноли в BL са ги направили перспективни кандидати като потенциални протектори срещу липидно окисление и биологично стареене на тъканите.
2. Експериментална секция
2.1. Растителен материал
Търговски сушен BL е любезно доставен от Pàmies Hortícoles (Балагер, Испания), регистрирана билкова компания. Всички използвани реактиви и разтворители са с аналитично качество и са получени от Panreac (Барселона, Испания) и Sigma Aldrich (Gillingham, Англия).
2.2. Екстракция на екстракт от BL
Изсушеното BL се смила фино с помощта на стандартен кухненски кухненски робот. Смленият BL се екстрахира с 50:50 (v/v) етанол: вода винаги в съотношение 1:20 (w/v). Екстракциите се извършват на тъмно при 4 ± 1 ° С в продължение на 24 часа, при постоянно разбъркване. Разтворите на екстракт от BL се възстановяват чрез филтруване с помощта на филтърна хартия Whatman, 0,45 µm. Част от супернатантата беше взета за последваща употреба за определяне на антирадикалния капацитет. Останалата супернатанта беше измерена и излишният етанол беше отстранен под вакуум с помощта на ротационен изпарител (BUCHI RE111, Швейцария) и държан замразен при -80 ° С за 24 часа. Всички екстракти бяха изсушени в сушилня за замразяване (Unicryo MC2L -60 ° C, Мюнхен, Германия) под вакуум при -60 ° C за 3 дни, за да се отстрани влагата. Накрая, лиофилизираният BL се претегля, за да се определи разтворимата концентрация (g/L), както е описано от Zhang et al. [14].
2.3. Определяне на общото фенолно съединение (TPC)
Методът Фолин – Чиокалтеу се използва за определяне на общото съдържание на феноли, както е описано от Santas et al. [15].
2.4. Определяне на антиоксидантната активност чрез анализ на TEAC
Антиоксидантният капацитет на BL е измерен чрез модифициран TEAC анализ, както е описано от Skowyra et al. [16], който се основава на метода на Miller et al. [17].
2.5. Определяне на радикален анализ на активността при използване на електронен парамагнитен резонанс (EPR)
Активността на EPR за извличане на радикали беше измерена по метода на Azman et al. [18]. BL се екстрахират с MeOH в съотношение 1:10 (w/v) и разтворимата концентрация на BL се определя, както е описано в процедурата по-горе. Реакционна смес със спин-улавяне се състои от 100 μL 5,5-диметил-1-пиролин-N-оксид (DMPO) (35 mM), 50 μL H2O2 (10 mM) и 50 μL екстракт от BL екстракт при различни концентрации . Като еталон се използва ферулова киселина (0–20 g/L) и контролът е чист МеОН. Накрая, 50 μL FeSO4 (2 тМ) бяха добавени към сместа. Крайните разтвори се прехвърлят в тясна кварцова тръба и се въвеждат в кухината на EPR спектрометъра. Спектърът се записва в продължение на 10 минути. X-лентовите EPR спектри са записани със спектрометър Bruker EMX-Plus 10/12 (Bruker Española S.A., Мадрид, Испания) при следните условия: микровълнова честота, 9.88 GHz; микровълнова мощност, 30,27 mW; централно поле, 3522,7 G; ширина на почистване, 100 G; усилване на приемника, 5,02 × 104; честота на модулация, 100 kHz; амплитуда на модулация, 1.86 G; времева константа, 40.96 ms; време на преобразуване, 203.0 ms.
2.6. Определяне на антиоксидантната активност в хранителния модел
2.6.1. Отстраняване на токофероли от слънчогледово масло
Алуминиевият оксид се поставя в пещ при 200 ° С за 24 часа и след това се отстранява и се оставя да се охлади в ексикатор, докато достигне стайна температура. Слънчогледовото масло се прекарва два пъти през алуминиев оксид в колона за отстраняване на токоферолите, както е описано от Yoshida et al. [19]. Накрая, филтрираното масло се съхранява при -80 ° C до употреба.
2.6.2. Приготвяне на емулсия
Емулсията масло във вода се приготвя, използвайки метод, адаптиран от Azman et al. [20]. Крайните проби бяха приготвени с помощта на (1) контрол (без добавяне); (2) 0,2 g/kg BHA; или (3) 1 g/kg лиофилизиран BL. Емулсията за всяка проба се приготвя четирикратно, като се получават общо 12 проби и се съхранява на тъмно и се оставя да се окисли при 37 ° С. РН на пробите беше измерено четири пъти за всяка проба (рН метър GLP21, Crison Instruments, Барселона, Испания) като параметър за изследване на нейната корелация с пероксидна стойност (PV).
2.6.3. Определяне на пероксидната стойност (PV)
Продуктите на първично окисление бяха измерени, като се използва пероксидна стойност (PV) съгласно метода на тиоцианата на Асоциацията на официалните аналитични химици (AOAC) 8195 [21]. Разтворът на железен хлорид се приготвя в солна киселина (1 М) с добавяне на железен (II) хлорид (2 тМ, крайна концентрация). Разтворът на амониев тиоцианат се приготвя във вода (2 тМ, крайна концентрация). Изследването се извършва с капка емулсия между 0,007 и 0,01 g, разредена с етанол. От този разтвор необходимото количество проба, вариращо в зависимост от степента на окисление, се прехвърля в кювета и етанолът се добавя към пробата. Прибавят се разтвори на железен хлорид и амониев тиоцианат, всеки в пропорция 1,875% (v/v), крайна концентрация. Абсорбцията е измерена спектрофотометрично при λ = 500 nm. Резултатите са изразени като meq хидропероксиди/kg емулсия.
2.6.4. Приготвяне на желатинов филм с антиоксидантно покритие
Производството на желатинов филм с антиоксидантно покритие беше адаптирано и характеризирано по метода на Bodini et al. [22]. По време на охлаждането на филмогенния разтвор след разтварянето на сорбитол се добавят 1 g/kg екстракт от BL/желатин. Мастните и ставните тъкани бяха отрязани от постно месо (2000 g) и месото беше смляно през 8-милиметрови индустриални плочи. След това месото се формова до дебелина 1,5 cm. За всеки резен се поставят филми (5 × 5 cm2) от двете страни, с контролен филм (без добавяне на антиоксидант) или BL филм (1 g/kg лиофилизиран BL). Контролните проби бяха приготвени по същия начин, с изключение на това, че филиите не бяха покрити с никакъв филм. Впоследствие пробите бяха опаковани в полипропиленови тави преди съхранение при 4 ° С за 12 дни.
2.6.5. Реагиращи на тиобарбитурова киселина вещества (TBARS)
Измерването на TBARS се използва за измерване на степента на липидно окисление по време на периода на съхранение, както е описано от Grau et al. [23]. Пробата (1 g) се претегля в епруветка и се смесва с 3 ml/L воден EDTA. След това пробата веднага се смесва с 5 ml реагент на тиобарбитурова киселина, като се използва Ultra-Turrax (IKA, Германия) при скорост 32 000 об/мин за 2 минути. Всички процедури се провеждат на тъмно и всички проби се държат в лед. Сместа се инкубира при 97 ± 1 ° С в гореща вода за 10 минути и се разклаща за 1 минута по време на процеса, за да се образува хомогенна смес. Течната проба се възстановява чрез филтруване (филтърна хартия Whatman, 0.45 µm), след като пробата се охлажда за 10 минути. Стойността на абсорбцията за всяка проба беше измерена при 531 nm с помощта на спектрофотометър. Стойността на TBARS беше изчислена от стандартна крива на Malondialdehyde (MDA), приготвена с 1,1,3,3-тетраетоксипропан и анализирана чрез линейна регресия. Всички резултати са докладвани като mg малоналдехид/kg проба.
2.7. Статистически анализ
Беше извършен еднопосочен вариационен анализ (ANOVA), използвайки софтуерна програма Minitab 16 (Addlink Software Ciachingo, Барселона, Испания) (α = 0,05). Резултатите бяха представени като средни стойности (n ≥ 3).
3. Резултати и дискусия
3.1. Добив на екстракция, общо фенолно съдържание (TPC) и антиоксидантна активност
Добивът на екстракция, общите полифеноли (TPC) и антиоксидантната активност в екстракти от листа от мечо грозде, получени с 50:50 v/v етанол: вода, са показани в Таблица 1. Средно от 5 g екстракт от мечо грозде след 3 дни сушене чрез замразяване (p> 0,05) се възстановяват 1,6 ± 0,01 g екстракт от целулоза.
маса 1
Добив на екстракция, съдържание на полифенол и антиоксидантна активност на екстрактите от листа на мечо грозде.
| Добив на екстракция (%) | 32,1% ± 0,03% |
| Общо фенолно съдържание (mg GAE/g DW) | 102,11 ± 7,12 |
| TEAC (mmol TE/g DW) | 90,42 ± 1,83 |
*: Резултатите са изразени като средно ± стандартно отклонение (n = 3). Еквивалент на галова киселина (GAE), еквивалент на тролокс антиоксидантна активност (TEAC), еквивалент на тролокс (TE), сухо тегло (DW).
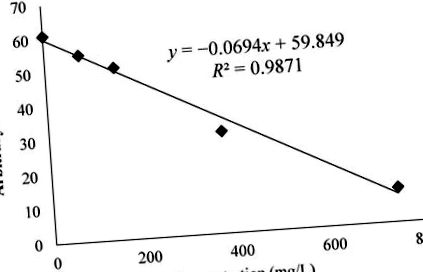
3.2 Анализ на тестовете за свободна радикална активност
където стойностите x са в mg/L.
Вариация в областта на спектрите на електронен парамагнитен резонанс (EPR) на радикалния адукт DMPO – OCH3, генериран от разтвор на H2O2 (2 mM) и FeSO4 (0.04 mM) с DMPO (14 mM) като спин капан в MeOH като разтворител. EPR сигналът е намален с повишаване на концентрацията на екстракти от BL метанол. EPR сигналът намалява при по-висока антиоксидантна активност.
Графиката показва експоненциалната стойност на сигнала от спектъра намалява с увеличаване на количеството екстракт от мечо грозде. Azman и сътр. демонстрира способността за почистване на катехини с метокси радикал, използвайки този анализ [18]. Тези катехини са открити и в екстракт от мечо грозде от Valjkovic et al. и тези съединения допринесоха за способността да избиват метокси радикал в този анализ [24]. Освен това, способността за почистване на BL е съобщена по-рано от Amarowicz et al. като се използват хидроксилни свободни радикали (HO •), измерени чрез EPR [11].
3.3. Антиоксидантни ефекти в съхранена o/w емулсия
Разработени са методи за разбиране на ефекта на естествените антиоксиданти в моделни храни като емулсии и опаковки с активен филм. Добавянето на естествени антиоксиданти към храната не само забавя процеса на окисление, но и подобрява хранителните качества на храната чрез директно поглъщане. В предишна работа ефектът на екстракта от листа на мечо грозде в емулсия масло-вода не е описан. Използвана е моделна емулсия за оценка на влошаването на липидите на два етапа на окисление, които са основните продукти на окисляване (Пероксидна стойност) и вторичните продукти на окисляване (TBARS). В допълнение се наблюдава промяната в рН, тъй като рН има тенденция да спада по време на окислението.
- Сини сливи (сушени сливи) Естествени храни за отслабване HowStuffWorks
- Соеви зърна Естествени храни за отслабване HowStuffWorks
- Естествени горелки за мазнини Храни, добавки и др
- Разпродажба Най-новите здравословни мумии Отслабнете с естествено тегло - Глобално проучване Великобритания
- Шафран Естествен мощен антиоксидант като обещаващо лекарство против затлъстяване