Ариана Майорана
Метаболитно отделение, Катедра по детска медицина, Детска болница Bambino Gesù, площад S. Onofrio 4, 00165 Рим, Италия
Лусила Манганоци
Метаболитно отделение, Катедра по детска медицина, Детска болница Bambino Gesù, площад S. Onofrio 4, 00165 Рим, Италия
Фабрицио Барбети
Катедра по експериментална медицина, Университет Tor Torgata и Детска болница Bambino Gesù, Рим, Италия
Силвия Бернабей
Клинично хранене, Отделение по гастроентерология, Детска болница Bambino Gesù, Рим, Италия
Джорджия Гало
Метаболитно отделение, Катедра по детска медицина, Детска болница Bambino Gesù, площад S. Onofrio 4, 00165 Рим, Италия
Рафаела Кусмай
Неврология, отделение по неврология, Детска болница Bambino Gesù, Рим, Италия
Стефания Кавилия
Отдел по психология, Отдел по неврология, Детска болница Bambino Gesù, Рим, Италия
Карло Диониси-Вичи
Метаболитно отделение, Катедра по детска медицина, Детска болница Bambino Gesù, площад S. Onofrio 4, 00165 Рим, Италия
Резюме
Заден план
Вроденият хиперинсулинизъм (CHI) е най-честата причина за хипогликемия при деца. В допълнение към повишеното използване на периферна глюкоза, нерегулираната секреция на инсулин предизвиква дълбока хипогликемия и неврогликопения чрез инхибиране на гликогенолиза, глюконеогенеза и липолиза. Това води до недостиг на всички мозъчни енергийни субстрати (глюкоза, лактат и кетони) и може да доведе до тежки неврологични последствия. Пациенти с CHI, които не реагират на медицинско лечение, могат да бъдат подложени на почти пълна панкреатектомия с повишен риск от вторичен диабет. Кетогенната диета (KD), чрез възпроизвеждане на състояние, подобно на гладно, при което телесното гориво произлиза главно от бета-окисляване, има за цел да осигури алтернативни мозъчни субстрати като кетонни тела. Възползвахме се от известния защитен ефект на KD върху невронално увреждане, свързано с дефицит на GLUT1, нарушение на нарушен транспорт на глюкоза през кръвно-мозъчната бариера, и приложихме KD при пациент с нереагираща на лекарството CHI, с цел да осигури на невроните енергиен източник, алтернативен на глюкозата.
Методи
Дете с резистентна към лекарства дългогодишна ХИ, причинена от спонтанна мутация, активираща GCK (p. Val455Met), страда от епилепсия и показва неврологични аномалии в развитието. След опит за различни терапевтични режими без успех, на родителите беше предложена почти пълна панкреатектомия, която поиска други възможности. Ето защо ние предложихме KD в комбинация с инсулинопотискащи лекарства.
Резултати
Прилагахме KD в продължение на 2 години. Скоро след първите шест месеца пациентът е освободен от епилептични кризи, представя нормализиране на ЕЕГ и показва значително възстановяване в психологическото развитие и качеството на живот.
Заключения
KD може да представлява ефективно лечение за подпомагане на мозъчната функция в избрани случаи на CHI.
Заден план
Методи
Резултати и дискусия
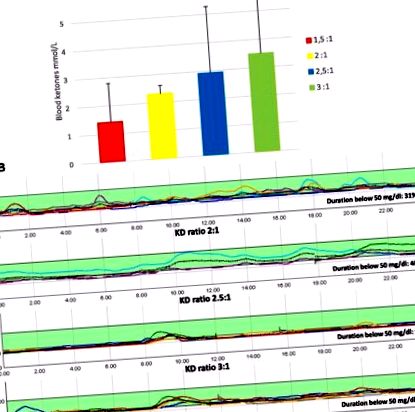
Докато е бил на KD, пациентът е продължил лечението с диазоксид и октреотид (съответно 10 mg/kg/ден и 35 μg/kg/ден). Шест месеца след началото на KD, поддържането на кръвни кетони между 2–5 mmol/L (фиг. 1, панел а) напълно разрешава неврогликопеничните признаци с паралелно изчезване както на епилептичната криза, така и на липсата на епилепсия, въпреки нивата на глюкоза в кръвта трайно под 5,5 mmol/L дори след хранене и почти 2,2–2,7 mmol/L през повечето време (фиг. 1, панел b). ЕЕГ се подобри и се нормализира през първата година на KD, като не показва промени дори по време на епизоди на хипогликемия (Фиг. 2). През първите 6 месеца на KD пациентът отслабна с 9 кг и нейният ИТМ се нормализира. Психологическата оценка разкрива засилване на социалните, когнитивните и вербалните способности (фиг. 3). Детето и нейното семейство съобщават за подобрение на физическото и психосоциалното благосъстояние, намаляване на страха от хипогликемични симптоми и осъзнаване на по-нисък риск от неврологично увреждане, с цялостно подобряване на качеството на живот, свързано с управлението на заболяването. Диазоксидът е спрян и понастоящем на пациента се дава октреотид, намален до 25 μg/kg/ден, без никакви неврогликопенични симптоми. KD се понася добре за период от 24 месеца, без странични ефекти и без промени в лабораторните тестове.
Кетони в кръвта и нива на глюкоза по време на KD. Кетоните прогресивно се повишават до 2–5 mmol/L, като същевременно се увеличава KD съотношението от 1,5: 1 на 3: 1 (панел а). 120h-непрекъснато проследяване на глюкозата на KD на 2 седмици, 3 месеца, 6 месеца, 12 месеца, показващи персистиране на хипогликемия (средно 52 mg/dl, 2,8 mmol/L, диапазон 40–84 mg/dl, 2,2–4,6 mmol/L) (Панел б)
Сравнение между мозъчната активност и гликемията преди и след 1 година KD. Изчезване на отсъстваща епилепсия или електрически признаци въпреки хипогликемия. Преди KD, продължителното наблюдение на ЕЕГ показва генерализирани разряди на шипове и вълни със загуба на контакт по време на хипогликемия. При KD продължителният мониторинг на ЕЕГ изглежда нормален, с липса на иктална ЕЕГ и епилептични прояви дори по време на хипогликемия
Когнитивни адаптивни умения преди и след 1 година KD. Нормализиране на когнитивните, социалните и вербалните възможности на KD. Скала за интелигентност на Weschsler за деца (WISCIII): нормална> 80, гранична 70–80; Скала за адаптивно поведение на Vineland (VABS): умерено висока 116–130, нормална 85–115, умерено ниска 70–84
Защитното действие на ЦНС на 3-хидроксибутират е успешно използвано за лечение на хипогликемична кома при плъхове [31] и множествен дефицит на ацил-КоА дехидрогеназа при хора [32]. Следователно ние предполагаме, че използването на 3-хидроксибутират може да бъде по-безопасен вариант и област на изследване при конкретни пациенти, като новородени с CHI, при които приложението на KD може да бъде опасно.
Заключения
Клиничното и неврологично подобрение, наблюдавано при нашия пациент с ХИ, предполага, че KD може да има невропротективен ефект въпреки персистирането на неврогликопенията. Необходими са допълнителни проучвания, за да се потвърди ефикасността на този нов терапевтичен подход в избрани случаи на ХИ в подкрепа на мозъчната функция чрез осигуряване на алтернативен източник на енергия за ЦНС.
Съкращения
| CHI | Вроден хиперинсулинизъм |
| KD | Кетогенна диета |
| GCK | Глюкокиназа |
| GLUT1 | Транспортер на глюкоза 1 |
| ЕЕГ | Електроенцефалография |
| FFA | Свободни мастни киселини |
| ROS | Радикални кислородни видове |
| ЦНС | Централна нервна система |
Бележки под линия
Конкуриращи се интереси
Авторите заявяват, че нямат конкуриращи се интереси.
Принос на авторите
- Здравословната диета може да предотврати свиването на мозъка
- Immunodietica Подход, базиран на данни за изследване на взаимодействията между диета и автоимунна система
- Зърнен мозък; s Дейвид Perlmutter за предимствата на диета с ниско съдържание на въглехидрати и високо съдържание на мазнини
- Подобрете диетата си, за да предотвратите ъгловия хейлит (ъглови пукнатини по устните) от Anna Smith Medium
- Зърнена мозъчна диета Пълният преглед и начинаещи; s Ръководство - Диета за самопомощ