Субекти
Резюме
Цели
За характеризиране на остатъчните концентрации на ванкомицин (Cmin) и оценка на връзките между Cmin, риска от нефротоксичност и персистиращ сепсис на CoNS.
Методи
В това 5-годишно ретроспективно проучване сред кърмачета, лекувани с ванкомицин, основният резултат е делът на тези с Cmin в стабилно състояние между 10 и 20 mg/L. Вторичните резултати са нефротоксичност и персистиращ сепсис на CoNS.
Резултати
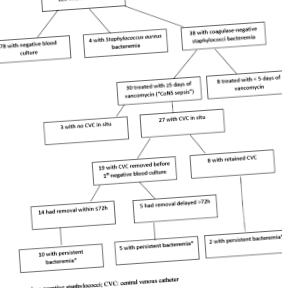
От включените 120 бебета, средното Cmin в първостепенно състояние е 12,4 mg/L, а 77 (64%) има Cmin между 10 и 20 mg/L. Шест процента развиват нефротоксичност. Този риск не е свързан с Cmin. От 30 бебета с CoNS сепсис, 17 (57%) са имали персистираща бактериемия и този риск не корелира значително с Cmin, CoNS минимална инхибиторна концентрация (MIC) за ванкомицин или Cmin/MIC.
Заключения
По-голямата част от бебетата са постигнали целеви нива на ванкомицин, но постоянната бактериемия е често срещана. Не идентифицирахме праг на Cmin, свързан с нефротоксичността, нито с микробиологичния клирънс.
Опции за достъп
Абонирайте се за Journal
Получете пълен достъп до дневник за 1 година
само 20,17 € на брой
Всички цени са нетни цени.
ДДС ще бъде добавен по-късно при плащане.
Наем или покупка на статия
Получете ограничен или пълен достъп до статии в ReadCube.
Всички цени са нетни цени.
Препратки
Clark RH, Bloom BT, Spitzer AlanR, Gerstman DR. Съобщена употреба на лекарства в отделението за интензивно лечение за новородени: данни от голям национален набор от данни. Педиатрия. 2006; 117: 1979–87.
Stoll BJ, Hansen N, Fanaroff AA, Wright LL, Carlo WA, Ehrenkranz RA, et al. Късен сепсис при новородени с много ниско тегло при раждане: опитът на мрежата за изследване на новородени NICHD. Педиатрия. 2002; 110: 285–91.
Patel SJ, Oshodi A, Prasad P, Delamora P, Larson E, Zaoutis T, et al. Употреба на антибиотици в отделенията за интензивно лечение за новородени и придържане към центрове за контрол и профилактика на заболяването 12 стъпка кампания за предотвратяване на антимикробна резистентност. Pediatr Infect Dis J. 2009; 28: 1047–51.
Pauwels S, Allegaert K. Терапевтичен мониторинг на лекарства при новородени. Arch Dis Child. 2016; 101: 377–81.
Jacqz-Aigrain E, Leroux S, Zhao W, Van Den Anker JN, Sharland M. Как да използваме ванкомицин оптимално при новородени: оставащи въпроси. Exp Rev Clin Pharm. 2015; 8: 635–48.
Rybak M, Lomaestro B, Rotschafer JC, Moellering R, Craig W, Billeter M, et al. Терапевтично наблюдение на ванкомицин при възрастни пациенти: консенсусен преглед на Американското общество на фармацевтите от здравната система, Американското общество по инфекциозни болести и Дружеството на фармацевтите по инфекциозни болести. Am J Heal Pharm. 2009; 66: 82–98.
Pacifici GM, Allegaert K. Клинична фармакокинетика на ванкомицин при новороденото: преглед. Клиники. 2012; 67: 831–7.
ван ден Анкер JN. Получаване на дозата на ванкомицин точно при новороденото. Int J Clin Pharm Ther. 2011; 49: 247–50.
Moise-Broder PA, Forrest A, Birmingham MC, Schentag JJ. Фармакодинамика на ванкомицин и други антимикробни средства при пациенти с инфекции на долните дихателни пътища на Staphylococcus aureus. Clin Pharmacokinet. 2004; 43: 925–42.
Frymoyer A, Hersh AL, El-Komy MH, Gaskari S, Su F, Drover DR, et al. Асоциация между минималната концентрация на ванкомицин и площта под кривата концентрация-време при новородени. Антимикробни агенти Chemother. 2014; 58: 6454–61.
Bhongsatiern J, Stockmann C, Roberts JK, Yu T, Korgenski KE, Spigarelli MG, et al. Оценка на употребата на ванкомицин при късно настъпил неонатален сепсис, като се използва площта под кривата концентрация-време до минималната инхибиторна концентрация> 400 цел. Ther Drug Monit. 2015; 37: 756–65.
Kim J, Walker S, Iaboni DC, Walker SE, Elligsen M, Dunn MS, et al. Определяне на фармакокинетиката на ванкомицин при новородени за разработване на практически препоръки за първоначално дозиране. Антимикробни агенти Chemother. 2014; 58: 2830–40.
Mehrotra N, Tang L, Phelphs S, Meibohm B. Оценка на режимите на дозиране на ванкомицин при недоносени и доносени новородени, използвайки симулации на Монте Карло. Фармакотерапия. 2012; 32: 408–19.
Ringenberg T, Robinson C, Meyers R, Degnan L, Shah P, Siu A, et al. Постигане на терапевтични ванкомицин чрез серумни концентрации с емпирично дозиране при пациенти в интензивно отделение за новородени. Pediatr Infect Dis J. 2015; 34: 742–7.
Frymoyer A, Stockmann C, Hersh AL, Goswami S, Keizer RJ. Индивидуализирано дозиране на ванкомицин при новородени, използвайки моделен подход. J Pediatr Infect Dis Soc. 2017; 00 (януари): 1–8.
Kato H, Hagihara M, Nishiyama N, Koizumi Y, Mikamo H, Matsuura K, et al. Оценка на оптималния режим на първоначално дозиране с модел на фармакокинетика на ванкомицин при новородени с много ниско тегло при раждане. J Infect Chemother. 2017; 23: 154–60.
McNeil JC, Kok EY, Forbes AR, Lamberth L, Hulten KG, Vallejo JG, et al. Свързана със здравеопазването бактериемия на Staphylococcus aureus при деца доказателства за обратна пълзене на ванкомицин и въздействие на минималните стойности на ванкомицин върху резултата. Pediatr Infect Dis J. 2016; 35: 263–8.
Национална мрежа за здравна безопасност (NHSN). Инфекция, свързана с централната линия, и инфекция на кръвта, която не е свързана с централната линия. 2019 г.
Furuichi M, Miyairi I. Рискови фактори за персистираща бактериемия при кърмачета с свързана с катетъра инфекция на кръвния поток поради коагулаза-отрицателен стафилокок в отделението за интензивно лечение за новородени. J Infect Chemother. 2016; 22: 785–9.
Abbott Laboratories. Архитект iVancomycin. 2008; 1–7.
Tseng S, Lim CP, Chen Q, Tang CC, Kong ST, Ho PC. Оценка на връзката между минималната концентрация на ванкомицин и 24-часовата площ под кривата концентрация-време при новородени. Антимикробни агенти Chemother. 2018; 62: 1–11.
De Hoog M, Mouton JW, Van Den Anker JN. Ванкомицин: фармакокинетика и схеми на приложение при новородени. Clin Pharmacokinet. 2004; 43: 417–40.
Linder N, Edwards R, MeClead R, Mortensen ME, Walson PKG. Безопасност на ванкомицин със или без гентамицин при новородени. Неонатална мрежа. 1993; 12: 27–30.
Yoo RN, Kim SH, Lee J. Влияние на първоначалната минимална концентрация на ванкомицин върху клиничните и микробиологичните резултати от метицилин-резистентната бактериемия на Staphylococcus aureus при деца. J Korean Med Sci. 2017 г .; 32: 22–8.
Wang JL, Lai CH, Lin HH, Chen WF, Shih YC, Hung CH. Високи минимални инхибиторни концентрации на ванкомицин с хетерорезистентни към междинния ванкомицин Staphylococcus aureus при пациенти, устойчиви на метицилин S. aureus бактериемия. Int J Антимикробни агенти. 2013; 42: 390–4.
Blanchard AC, Fortin E, Laferrière C, Goyer I, Moussa A, Autmizguine J, et al. Сравнителна ефективност на линезолид срещу ванкомицин като окончателна антибиотична терапия за хетерогенно резистентни на ванкомицин междинни коагулаза-отрицателни стафилококови инфекции, свързани с централната линия на кръвния поток в неонатологично отделение за интензивно лечение. J Антимикробна майка. 2017; 72: 1812–7.
Le J, Bradley JS, Murray W, Romanowski GL, Tran TT, Nguyen N, et al. Подобрено дозиране на ванкомицин при деца, използващи площ под излагането на кривата. Pediatr Infect Dis J. 2013; 32: e155–63.
Stockmann C, Hersh AL, Roberts JK, Bhongsatiern J, Korgenski EK, Spigarelli MG, et al. Предсказуемо представяне на фармакокинетичен модел на популация на ванкомицин при новородени. Infect Dis Ther. 2015; 4: 187–98.
Благодарности
Бихме искали да благодарим искрено на Надя Десмаре, д-р Caroline Quach и д-р Nicole Le Saux за подкрепата им по време на този проект.
Информация за автора
Принадлежности
Катедра по педиатрия, Centre Hospitalier de l’Université Laval, Québec, QC, Канада
Катедра по фармация, CHU Sainte-Justine, Монреал, QC, Канада
Брижит Мартин и Феликс Томпсън-Дезормо
Катедра по микробиология, инфекциозни болести и имунология, Университет на Монреал, Монреал, Квебек, Канада
Катедра по педиатрия, Университет на Монреал, Монреал, QC, Канада
Ахмед Муса и Джули Атмигвин
Изследователски център, CHU Sainte-Justine, Университет на Монреал, Монреал, QC, Канада
Ахмед Муса и Джули Атмигвин
Катедра по фармакология и физиология, Университет на Монреал, Монреал, QC, Канада
Отдел за клинична фармакология, Университет на Монреал, Монреал, Квебек, Канада
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Вноски
Всички изброени автори (IV-T, FT-D, BM, JB, AM, JA) са участвали в концепцията на този преглед. IV-T изготви първоначалната версия. Впоследствие всички съавтори преразглеждат ръкописа. И шестимата автори одобриха окончателната версия на рецензията. IV-T е съответният автор и като такъв има пълен достъп до данните и окончателна отговорност за решението за представяне за публикуване.
Автора за кореспонденция
Етични декларации
Конфликт на интереси
Авторите декларират, че нямат конфликт на интереси.
Допълнителна информация
Бележка на издателя Springer Nature остава неутрален по отношение на юрисдикционните претенции в публикувани карти и институционални принадлежности.
- Защо никое лекарство за затлъстяване никога няма да бъде следващият Lipitor
- Клиничният ефект на нова формула за кърмачета при доносени бебета със запек двойно сляп,
- Диетата на воините Плюсове, минуси и как работи
- Смъртоносната следа на убийствения наркотик за отслабване DNP
- Какви са плюсовете и минусите на аблация на ендометриума Андрю Крински, д-р, FACOG