Дейвид С. Ниман
1 Лаборатория за човешка ефективност, Изследователски кампус в Северна Каролина, Държавен университет в Апалачи, Канаполис, NC 28081, САЩ; ude.etatsppa@janosnomis
Анди Саймънсън
1 Лаборатория за човешка ефективност, Изследователски кампус в Северна Каролина, Държавен университет в Апалачи, Канаполис, NC 28081, САЩ; ude.etatsppa@janosnomis
Камила А. Сакагучи
2 Отдел по физикална терапия, Федерален университет на Сао Карлос, Сао Карлос 13565-905, Бразилия; moc.liamg@097ihcugakasalimac
Вей Ша
3 Отдел за биоинформатични услуги, Изследователски кампус в Северна Каролина, Университет на Северна Каролина в Шарлот, Канаполис, NC 28081, САЩ; ude.ccnu@ahsw
Тондра Блевинс
4 UNC Nutrition Research Institute, UNC-Chapel Hill, North Carolina Research Campus, 500 Laureate Way, Kannapolis, NC 28081, САЩ; ude.cnu@snivelb_ardnot (T.B.); ude.cnu@hguabattah_aniaj (J.H.); ude.cnu@reiemlhokm (M.K.)
Jaina Hattabaugh
4 UNC Nutrition Research Institute, UNC-Chapel Hill, North Carolina Research Campus, 500 Laureate Way, Kannapolis, NC 28081, САЩ; ude.cnu@snivelb_ardnot (T.B.); ude.cnu@hguabattah_aniaj (J.H.); ude.cnu@reiemlhokm (M.K.)
Мартин Колмайер
4 UNC Nutrition Research Institute, UNC-Chapel Hill, North Carolina Research Campus, 500 Laureate Way, Kannapolis, NC 28081, САЩ; ude.cnu@snivelb_ardnot (T.B.); ude.cnu@hguabattah_aniaj (J.H.); ude.cnu@reiemlhokm (M.K.)
Резюме
1. Въведение
Дългосрочният прием на напитки от катехин и кофеин от зелен чай е свързан с малък, положителен ефект върху загубата на тегло и поддържането на теглото [1,2]. Острото поглъщане на катехин-кофеинови смеси може временно да увеличи енергийния разход и окисляването на мазнините чрез инхибиране или стимулиране на няколко ензима, включително катехол О-метилтрансфераза (COMT), фосфодиестераза и хормон-чувствителна липаза и активиране на метаболитната активност на кафявата мастна тъкан [1,2, 3,4,5,6].
Пет проучвания при хора (n = 66 мъже, n = 16 жени), проведени в метаболитни камери, използваха дози кофеин от 150 до 600 mg с различни количества катехини от зелен чай и епигалокатехин-3-галат (EGCG) (240 до 1200 mg) [7, 8,9,10,11]. Увеличенията на 24 часа енергийни разходи (24 часа EE) със смеси от катехин и кофеин варират от 2% до 8% и са свързани повече или изцяло с кофеиновата част на добавката. Rudelle и сътр. [10] предложи увеличението на 24-часовата ЕЕ с остро поглъщане на кофеин (със или без катехини) да бъде оценено чрез това уравнение: ((mg кофеин × 0,12) + 43,2 килокалории).
Отговорът на плазмения кофеин към приема на кофеин може да помогне да се обясни високата вариация между отделните индивиди в промените в енергийните разходи, но това все още не е измерено. Връзката между приема на кофеин, нивата на кофеин в плазмата и вариацията в реакциите на ЕЕ за 24 часа може също да бъде повлияна от еднонуклеотидния полиморфизъм (SNP) rs762551, който кодира алела на цитохром P450 1A2 (CYP1A2) * 1F на гена CYP1A2, който произвежда ензим, отговорен главно за метаболизма на кофеина [12]. Заместване от А до С в позиция 163 (rs762551) в гена CYP1A2 намалява ензимната индуцируемост. Носителите на алела C, който се среща в 54% от населението (163A/C и 163C/C генотипи, CYP1A2 * 1F) метаболизират кофеина по-бавно от индивидите, хомозиготни за алела 163A/A (CYP1A2 * 1A).
Поглъщането на смеси от катехин и кофеин може да увеличи окисляването на мазнините по-добре, отколкото само кофеинът, но тази констатация не е последователно подкрепена в малкото налични проучвания. Две от петте проучвания показват, че по отношение на плацебо, катехин-кофеиновите смеси стимулират окисляването на мазнините над нивата, свързани само с кофеина [7,8], като три проучвания показват нулеви ефекти [9,10,11]. Високата вариация между отделните индивиди е често срещана находка в тези проучвания, с Rudelle et al. [10] съобщава, че шест от 31 участници в проучването не са отговорили с повишена 24 часа ЕЕ на дозата на добавката (300 mg кофеин, 540 mg катехини и 282 mg EGCG).
Острото поглъщане на други видове флавоноиди, включително флавоноли и антоцианини, може да повлияе на разхода на енергия и окисляването на мазнините, но са публикувани малко изследвания, базирани на метаболитни камери с човешки участници [13,14,15,16]. Данните от три проспективни кохортни проучвания, включващи 124 086 мъже и жени, показват, че по-висок прием на храни и напитки, богати на флавоноли (напр. Кверцетин от ябълки и лук), антоцианини (напр. От боровинки), флаван-3-оли (напр. Катехини от чай) и флавоноидните полимери (напр. проантоцианидини и теафлавини от чай, ябълки) е обратно свързано с промяната на теглото през интервали от четири години [17]. Едно проучване показа, че кверцетинът временно увеличава енергийните разходи при мишки [18], но това не се дублира в малко пилотно проучване с човешки участници, приемащи 150 mg кверцетин [16]. Острото поглъщане на екстракт от боровинки намалява повишаването на глюкозата след хранене чрез намаляване на скоростта на усвояване на въглехидратите и следователно може да е повлияло на окисляването на мазнините [19]. Къпините съдържат флавоноли, антоцианини и флаван-3-оли, а високият прием (600 g/ден) в продължение на 7 дни е свързан с повишено окисление на мазнините при мъже с наднормено тегло/затлъстяване, хранени с диета с високо съдържание на мазнини спрямо желатина [15].
Острото поглъщане на смесена добавка от флавоноид-кофеин (MFC), съдържаща екстракт от зелен чай, кверцетин и боровинки антоцианини и проантоцианидини, има потенциал да увеличи енергийните разходи и окисляването на мазнините над нивата, предвидени само за кофеина. Добавката MFC (678 mg флавоноиди в четири капсули), използвана в това проучване, съдържа кверцетин (200 mg), катехини от зелен чай (368 mg, 180 mg EGCG) и антоцианини (128 mg) от екстракт от боровинка и 214 mg кофеин. Въз основа на уравнението, предложено от Rudelle et al. [10], само дозата кофеин ще се изчисли да увеличи 24 часа ЕЕ с 69 kcal/ден. Броят на мъжете участници в проучвания, базирани на метаболитни камери, е нисък (n = 10 до 15 на проучване) и само едно проучване включва жени (n = 16) [10]. Дизайнът и схемите на дозиране варират значително, като две от петте проучвания включват 3-дневен период на допълване с измервания само на третия ден [8,10].
Целта на това проучване е да се измери ефектът от поглъщането на добавката MFC (четири капсули, разделени между закуска и обяд) в сравнение с плацебо върху енергийните разходи и окисляването на мазнините в метаболитна камера със здрави жени в пременопауза. За да се намали потенциалното влияние на объркващи фактори, участниците по време на двете посещения в камерата (произволен ред) следваха точно същия график и бяха държани в евкалорично състояние. Плазмените нива на кофеин бяха измерени три часа след втората доза добавка и беше проведено генотипиране за еднонуклеотиден полиморфизъм (SNP) rs762551, кодиращ алела CYP1A2 * 1F на гена CYP1A2, за да се определи дали тези резултати помогнаха да се обясни разликата в отговорите на енергийните разходи към плацебо и MFC изпитанията. Предположихме, че поглъщането на добавката MFC би увеличило енергийните разходи и окисляването на мазнините над нивата, измерени с плацебо и отчасти ще бъде свързано с плазмените нива на кофеин и rs762551 генотип.
2. Материали и методи
2.1. Участници в проучването
2.2. Изследователски дизайн
Това проучване използва рандомизиран, двойно заслепен, кръстосан дизайн, сравняващ острото поглъщане на смесената флавоноидно-кофеинова добавка (MFC) с плацебо контрола при здрави жени в пременопауза. Изследването се състои от два 23-часови периода на изследване в индиректния калориметър в Университета на Северна Каролина Chapel Hill Nutrition Research Institute (UNC NRI). 23-часовите периоди на изследване в метаболитната камера бяха с интервал от 4 седмици, за да се гарантира, че участниците в изследването са тествани през същата фаза на менструалния цикъл. Първичните изходни мерки бяха 22 часа енергийни разходи (22 часа EE) (8:30 до 6:30), използване на субстрата от дихателния коефициент (RQ) и броя на физическата активност. Периодът от 22 часа е избран, за да се намалят смущения в енергийните разходи, свързани с преходни времеви сегменти в началото и в края на сесията на камарата.
2.2.1. Допълнение
2.2.2. Изследване на изходно ниво преди проучване
Допустимостта беше определена в амбулаторния клиничен пакет в UNC NRI. Съставът на тялото (мастна маса и маса без мазнини (FFM)) се определя с двуенергийна рентгенова абсорбциометрия (DXA) (GE Lunar iDXA; Milwaukee, WI). Индексът на телесна маса (BMI, kg/m 2) се изчислява от измерената височина и тегло. Скоростта на метаболизма в покой (RMR) се изчислява с помощта на Mifflin-St. Уравнение на Жор [22]. Този изчислен RMR е използван за проектиране на приема на диетична енергия, докато е в метаболитната камера: RMR x ниво на физическа активност (PAL) от 1,3, с допълнителни корекции, направени по време на посещенията в камерата (подробности предоставени по-долу). Малка кръвна проба беше събрана за оценка на състоянието на хормона на щитовидната жлеза (Lab Corp, Burlington, NC, USA) и червените кръвни клетки бяха аликвотирани и замразени за rs762551 генотипиране. Направен е и тест за бременност в урината.
2.2.3. Непряка калориметрия
Метаболитната камера в UNC NRI в Канаполис, Северна Каролина, е индиректен калориметър с отворена верига. Анализаторите на CO2 и O2 са диференциални, с отчитане в пълна скала, зададено за 0–1%. Консумацията на кислород (VO2), производството на въглероден диоксид (VCO2), разходът на енергия EE) и RQ се записват всяка минута. Разходът на енергия се изчислява, като се използва съкратена формула на Weir (VO2 × 3.941) + (VCO2 × 1.106), където VO2 е обемът на консумирания кислород в L/минута, а VCO2 е обемът на въглеродния диоксид, отделен в L/минута. RQ се изчислява като VCO2/VO2. Скоростите на окисление на субстрата се изчисляват, както следва: Скорост на окисляване на мазнините (g/min) = (1.689 × VO2) - (1.689 × VCO2); скорост на окисляване на въглехидратите (g/min) = (4.113 × VCO2) - (2.907 × VO2). Спонтанната физическа активност се измерва всяка минута, като се използва общ стаен микровълнов сензор, който записва броя на всяка секунда, в която се открива движение (Museum Technology Source Inc., Wilmington, MA, USA).
2.2.4. Протокол на метаболитната камера
Участниците в изследването пристигнаха на гладно през нощта в UNC NRI в 7:00, след като избягваха упражнения за 24 часа и кофеин и алкохол в продължение на поне осем часа. Участниците бяха запечатани в камерата, като записването на метаболитни измервания започва в 8:00. Участниците останаха седнали и будни през целия ден, с интервали от 2 минути, определени на час за стояне, разтягане и тоалетни. MFC или плацебо добавки бяха приети в 8:30. И 13:00 (по 2 капсули всеки път). Закуската (9:00), обядът (13:30), закуската (16:00) и вечерята (19:00) бяха поднесени през въздушен шлюз и консумирани в рамките на 30 минути от сервирането. Кръвна проба беше получена в 16:00 за измерване на плазмените концентрации на кофеин. Осветлението беше изключено в 22:00, а времето за лягане беше настроено в 22:30. Участниците в проучването бяха събудени в 6:30 и им беше позволено да се придвижват из стаята, за да съберат вещите си. В 7:15 участниците в изследването излязоха от камерата и бяха претеглени. 22-часовата EE е изчислена от данните, събрани от 8:30 до 6:30, с премахване на първия и последния 30-минутен сегмент на прехода.
2.2.5. Диета с метаболитни камери
Eucaloric диетите са проектирани да осигуряват приблизително 35% мазнини, 50% въглехидрати и 20% протеини, отразявайки настоящите препоръки за тази група от населението. Меню с ниско съдържание на флавоноиди е разработено с помощта на софтуер за изчисляване на хранителните вещества и управление на храните (Nutribase: CyberSoft, Incorporated; Phoenix, AZ, USA) и се състои от валцуван овес, бял хляб, фъстъчено масло, мляко (1% мазнина), постна смляна пуйка, кафяв ориз, извара (1% мазнина), мюсли, сухи печени фъстъци, пилешки гърди без кости, сухи макарони и зехтин. Не бяха сервирани напитки или храни, съдържащи кофеин. И при двете посещения в камерата се сервираха едни и същи храни. Основно меню за всеки обект беше изготвено въз основа на прогнозните енергийни разходи (RMR × 1,3), а след това модифицирано (закуска и вечеря) според измерените данни за енергийните разходи за 7 часа.
2.3. Кофеин в плазмата
Приготвянето на пробата се извършва чрез утаяване на протеин от 50 μL плазма с 200 μL метанол, съдържащ 40 ng/ml вътрешен стандарт кофеин-d9. Концентрацията на кофеин в плазмата се анализира с помощта на ултра-ефективна течна хроматография на Waters Acquity (UPLC) -Quattro Premier XE Mass Spectrometry (Waters Corp., Milford, MA, USA). Хроматографското разделяне на кофеина и вътрешния стандарт кофеин-d9 се извършва на UPLC етилен мостов хибрид (BEH) C18 1,7 μm аналитична колона (2,1 × 100 mm, Waters Corp., Milford, MA, USA) с градиентно елуиране с използване на подвижна фаза Ацетонитрил във вода и подвижна фаза В, и двата съдържащи 0,1% мравчена киселина. Откриването се извършва с помощта на масспектрометъра в режим на положителен йон с йонизация с електроспрей. Анализът се извършва в режим на многократно наблюдение (MRM). Контролът на инструмента и събирането на данни бяха извършени с помощта на софтуерния пакет Masslynx (Waters Corp., Milford, MA, USA).
2.4. rs762551 Генотипизиране с анализ на TaqMan
ДНК проби бяха извлечени от 500 µl човешка кръв в буфер за консервиране с помощта на мини комплект за ДНК кръв на QIAamp. Количество от 20 ng ДНК се използва като вход за реакция на генотипиране, използвайки TaqMan SNP Genotyping Assay (ThermoFisher, Waltham, MA, USA). Предварително проектирани праймери са използвани за идентифициране на трите възможни rs762551 генотипа (анализ C_8881221_40). След qPCR реакция, пакетът за дискриминация на алели от софтуера CFX Maestro от Bio-Rad (Hercules, CA, USA) беше използван за определяне на генотипове за всяка проба, използвайки три положителни контроли от biobank на Coriell Institute за SNP повикване (Camden, NJ, USA). Изследванията за екстракция на ДНК и генотипиране бяха извършени в лабораторията за геномика на изследователския институт Дейвид Х. Мърдок (Kannapolis, NC, САЩ).
2.5. Статистически анализи
3. Резултати
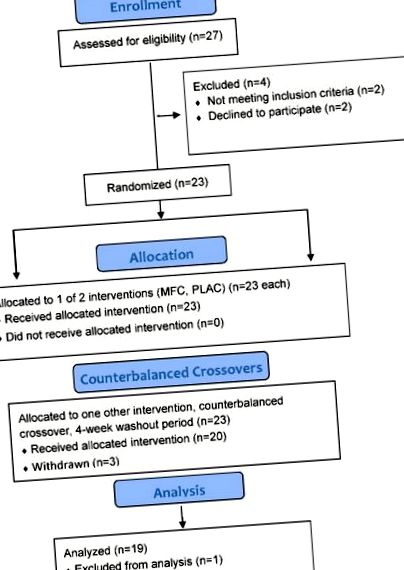
Диаграмата на участниците в изследването е показана на фигура 1. От 23 жени, участвали в проучването, 20 успешно са завършили всички фази на изследването, като едната е отпаднала от анализа поради техническа повреда в камерата (загуба на контрол на температурата). Участниците в проучването, завършили проучването (n = 19), са имали следните характеристики: възраст 30,7 ± 4,7 години, телесна маса 69,0 ± 9,0 kg, индекс на телесна маса (BMI) 25,7 ± 3,4 kg/m 2 и телесни мазнини 37,7 ± 6,6%.
Диаграма на потока на участниците в проучването. MFC = изпитване със смесен флавоноид-кофеин; PLAC = плацебо проучване.
Разходите за енергия (kcal/h) за MFC и плацебо проучванията са сравнени на Фигура 2 (ефект на лечение, p = 0,001). Общите енергийни разходи за 22-часовия период за MFC и плацебо изпитванията са средно съответно 1582 ± 143 и 1535 ± 154 kcal (средна разлика в опитите, 46,4 ± 57,8 kcal) (p = 0,003). Таблица 1 обобщава метаболитните данни за всеки определен времеви сегмент. Броят на активността и дихателният коефициент (RQ) не се различават значително между опитите или по време на всеки сегмент (Таблица 1). Разходът на енергия и консумацията на кислород за проучването с MFC са значително по-високи от плацебо (p Фигура 3 показва разликата в опита за енергийните разходи за всеки участник в проучването. Петима от 19 участници отговориха на добавката MFC с по-ниски енергийни разходи в сравнение с плацебо (т.е. не- За респондентите разликата в опитите е 70,9 ± 42,1 kcal. Възрастта, ИТМ и телесната мастност не се различават значително между респондентите и неотговорилите. Цветово кодирани ленти са използвани за представяне на генотипирането за SNP rs762551 (Фигура 3 Пробната разлика за енергийните разходи между тези с алел 1, A/A и тези с C/A или C/C не се различава (съответно 51,4 ± 42,8 и 31,3 ± 82,1 kcal/22 часа, p = 0,50 ).
Разход на енергия (kcal/22 h) пробна разлика (MFC минус плацебо) за всеки участник в проучването. Данните са изобразени във възходящ ред, с произволни идентификационни номера за участниците в проучването. Червените ленти показват участници в изследването с хомозиготен генотип A/A на еднонуклеотидния полиморфизъм (SNP) rs762551. Сините ленти показват участниците в изследването с генотипите C/A и C/C (само един участник, # 4). Черните ленти показват двама участници за генотипове, които не могат да бъдат определени. Пробната разлика в енергийните разходи между тези с генотип A/A и тези с генотипове C/A или C/C не е статистически значима (съответно 51,4 ± 42,8 и 31,3 ± 82,1 kcal/22 часа, p = 0,50).
Фигура 4 сравнява скоростите на окисление на мазнините на час между MFC и плацебо проучванията (ефект на лечение, р = 0,062). Окисляването на мазнини за MFC има тенденция по-високо от плацебо през дефинираните времеви сегменти (p = 0,054), без пробна разлика за въглехидратното окисление (Таблица 1). Окислението на мазнини за целия 22-часов период за MFC и плацебо проучванията е съответно 99,2 ± 14,0 и 92,4 ± 14,4 g/22 часа (p = 0,081).
Окисляване на мазнини (грамове/час) за MFC и плацебо проучванията (n = 19) (средно ± SD) (ефект на лечение, p = 0,062). Добавките бяха погълнати в 8:30 (час 1) и 13:00 (час 5). Закуската, обядът и вечерята бяха сервирани съответно в 9:00 (час 1), 13:30 (час 5) и 18:30 (час 10). Осветлението беше изключено за сън в 22:30 (час 14).
- Албутерол Кофеинът може да бъде обещаващ и безопасен () Структура против затлъстяване 13% остро увеличаване на енергията
- Остър миокарден инфаркт, свързан с поглъщането на хаптагон хапчета Доклад за случая
- Оценка на енергийните разходи в покой при юноши с наднормено тегло и затлъстяване в клинична обстановка
- Калории Общ прием на макронутриенти, енергийни разходи и нетни енергийни магазини - диета и здраве -
- 3 НАЧИНА КОФЕЙН ПОДИГА ВАШИЯ МЕТАБОЛИЗЪМ от VITER ENERGY Medium