От Отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
От Отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
От Отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
От Отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
От отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
От Отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
От отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
От Отдела по нефрология, Медицински колеж Baylor, Хюстън, Тексас.
Преглеждате най-новата версия на тази статия. Предишни версии:
Резюме
Хората имат повишена серумна пикочна киселина в резултат на мутация в гена на уратната оксидаза (уриказа), възникнала по време на миоцена. Предполагаме, че мутацията е осигурила предимство за оцеляване поради способността на хиперурикемията да поддържа кръвното налягане при диетични условия с ниско съдържание на сол, каквито са преобладаващите през този период. Леката хиперурикемия при плъхове рязко повишава кръвното налягане чрез зависим от ренин механизъм, който е най-явен при диетични условия с ниско съдържание на сол. Хроничната хиперурикемия също причинява чувствителност към солта, отчасти чрез индуциране на прегломеруларна съдова болест. Съдовата болест се медиира отчасти от индуцирана от пикочна киселина пролиферация на гладкомускулни клетки с активиране на митоген-активирани протеинкинази и стимулиране на циклооксигеназа-2 и растежен фактор, получен от тромбоцити. Въпреки че осигурява предимство за оцеляване на ранните хоминоиди, хиперурикемията може да има основна роля в настоящата епидемия от сърдечно-съдови заболявания.
Сърдечно-съдовите заболявания и хипертонията са епидемия в съвременното общество. Сърдечно-съдовите заболявания са причина за смърт номер едно в Съединените щати, отнемайки близо 1 милион животни годишно и представляваща 40% от смъртността от всички причини и повече смъртни случаи от следващите 7 водещи причини взети заедно. 1 Най-честата форма на сърдечно-съдови заболявания е хипертонията, която присъства в приблизително 20% от населението (50 милиона души) в Съединените щати и чиято честота нараства драстично с възрастта, засягайки по-голямата част от населението на възраст над 60 години. 2,3 Хипертонията значително увеличава риска от миокарден инфаркт, инсулт, застойна сърдечна недостатъчност, периферни съдови заболявания и краен стадий на бъбречно заболяване. 4,5 Лечението на хипертония намалява тези усложнения и може да намали броя на сърдечно-съдовите смъртни случаи, както и да подобри цялостното качество на живот. 6,7
Паралелни мутации в гена Uricase в ранните хоминоиди: еволюционни последици
Генът на уриказа също се променя в маймуните от Новия свят (Ceboidea) и Стария свят (Cercopithecoidea). Установено е, че серумната пикочна киселина е повишена при няколко вида маймуни от Новия свят, включително тамарина (Сагинус), капуцинът (Цебус), и вълнестата маймуна (Лаготрикс), докато пикочната киселина е била с ниско съдържание на маймуна катерица (Саймири) и маймуна сова (Aotus). 19 Нивата на пикочна киселина корелират с промените в активността на чернодробната уратна оксидаза при тези видове. Въпреки че проучвания за определяне на мястото на мутациите, отговорни за загубата на уриказа при маймуните от Новия свят, не са провеждани, мутациите вероятно са независими от тези, наблюдавани по време на еволюцията на хоминоидите, като има доказателства, че разминаването на инфрапортата на Platyrrhini (маймуните от Новия свят ) от Катарини (маймуни и хоминоиди от Стария свят), настъпили преди около 40 милиона години. 20 Интересното е, че въпреки че уратната оксидаза е била задържана при маймуните от Стария свят (Cercopithecoidea), ензимната активност е относително нестабилна в сравнение с други видове бозайници (непримати), което предполага, че еволюционните механизми, които нарушават активността на уратната оксидаза, също може да са действали в това суперсемейство. 19,21
Наблюдението, че няколко независими мутации с участието на уриказа са възникнали по време на еволюцията на хоминоидите и паралелно по време на еволюцията на маймуните от Стария свят и Новия свят, е интерпретирано като доказателство, че е трябвало да има еволюционно предимство за ранните примати при повишено ниво на пикочна киселина. 16,19,21 Времевата рамка на мутациите за гена на уриказа показва, че те са възникнали по време на миоцена (преди 24 до 8 милиона години). Поради това е важно да се разбере натиска върху околната среда, който се е появявал през този период от историята на хоминоидите.
Вкаменелостите показват, че най-ранните хоминоиди, като напр Проконсул, произхождат от Източна Африка преди около 22 до 17 милиона години, където са живели в буйни субтропични гори и влажни зони. 22–25 Тези ранни хоминоиди са били дървесни четириноги с диета, която е плодоядна (поглъща предимно меки плодове). 22–25 До ранния миоцен има многобройни хоминоидни видове, 22,23, особено в Евразия. 25 Въпреки това, към средата до късния миоцен (преди 14 до 8 милиона години) е имало изчезване на много миоценови маймуни, особено в Европа. 24,25 Изглежда, че това е свързано с екологична промяна в по-сух и по-сезонен климат и с промяна в местообитанието на по-отворени зони на савани, осеяни с тропически и субтропични гори. 25 В някои райони на Източна Африка може да са се запазили влажни и залесени местообитания. 26 Молекулярни ДНК изследвания показват, че през този период е имало бърз период на положителен подбор за различни гени, особено за генно семейство (морфей) в късото рамо на хромозома 16, 27 и имаше значителни промени в съзъбието и аксиалния скелет, които може да са улеснили адаптирането към по-суха среда. 22,23,28
Както беше обсъдено по-горе, приемът на натрий в ранните ловци в средата до късния плейстоцен беше в диапазона от 690 mg (1,9 g NaCl) на ден. Приемът на натрий в ранните хоминоиди по време на миоценската епоха (от преди 24 до 5 милиона години) вероятно е бил дори по-нисък, тъй като диетите се състоят предимно от плодове (плодоядни) или листа (листни). Итън и Конър изчисляват, че съдържанието на натрий в строго вегетарианска палеолитна диета може да е възлизало само на 225 mg натрий (10 mEq Na + или 0,6 g NaCl). 12 Така климатичното преминаване към по-сухи условия в средата към късния миоцен може да е оказало натиск за подбор на ранните примати към генотип, който максимално би запазил натрия с поддържане на кръвното налягане.
Пикочната киселина поддържа кръвното налягане при условия с ниско съдържание на натрий
Повечето автори 16,19,21 предполагат, че мутациите в гена на уриказа осигуряват еволюционно предимство, тъй като пикочната киселина може да функционира като антиоксидант. 29 Въпреки че антиоксидантната роля на пикочната киселина може да бъде един от механизмите за обяснение на полезните ефекти от мутацията на уриказа, ние разгледахме хипотезата, че пикочната киселина може да регулира кръвното налягане. Тази хипотеза се основава на предишни проучвания, доказващи, че серумната пикочна киселина корелира с кръвното налягане и прогнозира развитието на хипертония в популационни проучвания. 30–32
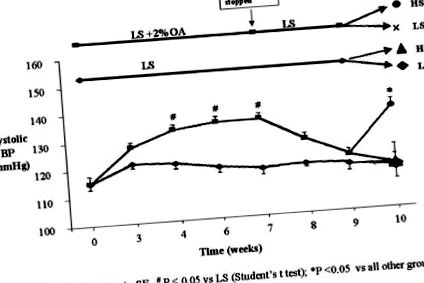
Фигура 2. Хиперурикемията поддържа кръвното налягане при диетични условия с ниско съдържание на сол при плъхове. Плъховете на Sprague-Dawley (n = 6), поставени на диета с ниско съдържание на Na + (0,125% NaCl), имат постепенно спадане на кръвното налягане, докато кръвното налягане се повишава при плъхове (n = 6) на диета с ниско съдържание на сол (LSD), на които се прилага инхибиторът на уриказата, оксонова киселина (ОА, 2%). Прилагането на алопуринол (150 mg/L в питейната вода, n = 6) предотвратява развитието на хиперурикемия и повишаването на кръвното налягане. Нива на пикочна киселина на 7 седмици: 2,1 ± 0,2 mg/dL, оксонова киселина; 1,3 ± 0,2 mg/dL, контрол с ниско съдържание на сол; 1,2 ± 0,3 mg/dL, оксонова киселина + алопуринол.
Първоначално Goldblatt предполага, че първичното бъбречно микроваскуларно заболяване може да бъде основният патогенен механизъм за есенциална хипертония. 33 Последните проучвания подкрепят тази хипотеза. 34 Индукцията на прегломеруларна артериоларна болест в експериментални модели води до тубулна исхемия, интерстициална инфилтрация на лимфоцити и макрофаги, генериране на локален окислител и промени в експресията на вазоконстриктори и вазодилататори, които благоприятстват локалната вазоконстрикция. 34 Тези промени водят както до намаляване на натриевата филтрация (причинено от намаляване на коефициента на ултрафилтрация, Kf) и повишена реабсорбция на натрий (чрез директни тубуларни ефекти) и водят до повишена реакция на кръвното налягане към натрий (чувствителност към сол). 34
Хиперурикемията предизвиква чувствителност към сол при плъхове
маса 1. Хиперурикемията предизвиква прегломеруларна микроваскуларна болест и интерстициално възпаление
Фигура 3. Хиперурикемията предизвиква чувствителност към солта. Плъховете на Sprague-Dawley получават оксонова киселина (2%) на диета с ниско съдържание на сол (0,125% NaCl) в продължение на 7 седмици (група OA-LS). През това време кръвното налягане се повишава в сравнение с контролите на диетата с ниско съдържание на сол (LS). Тогава диетата с оксонова киселина беше спряна, позволявайки нивата на пикочна киселина да се върнат до нива, еквивалентни на контролите с ниско съдържание на сол. На 9 седмици плъховете бяха рандомизирани, за да продължат диетата си с ниско съдържание на сол, или преминаха към диета с високо съдържание на сол (2% NaCl) (HS). Преди това хиперурикемичните плъхове развиха повишаване на кръвното налягане, документирайки развитието на чувствителност към солта; не се наблюдава промяна в кръвното налягане в контролната група при преминаване към диета с високо съдържание на сол. n = 6 на група; #P
Пикочната киселина стимулира размножаването на гладките мускулни клетки
По-нататък изследвахме механизма, по който пикочната киселина причинява съдови заболявания. Разтворима, без ендотоксин пикочна киселина (3 до 5 mg/dL) стимулира пролиферацията на съдови гладкомускулни клетки с активиране на митоген-активирания протеин (MAP) киназа, извънклетъчна регулирана киназа на сигнала (Erk1/2) и стимулиране на растежа, получен от тромбоцитите фактор (PDGF) и неговия рецептор (Фигура 4). Rao et al 35 също показват, че пикочната киселина индуцира експресия на PDGFA-верига и че пролиферацията на гладките мускулни клетки може да бъде предотвратена с неутрализиращи антитела към PDGF. Също така установихме, че пролиферацията на гладкомускулните клетки се медиира от индуцирана от пикочна киселина циклооксигеназа-2 (COX-2) експресия с генериране на тромбоксан (Duk-Hee Kang, Takahiko Nakagawa, Lili Feng, Marilda Mazzali, Susumu Watanabe, Lin Han, Luan Truong, Raymond Harris, Richard J. Johnson. Непубликуван ръкопис, 2002 г.) и отчасти чрез активиране на ренин ангиотензиновата система. 15
Фигура 4. Пикочната киселина индуцира пролиферация на гладкомускулни клетки, активиране на MAP киназа и експресия на PDGF. Съдовите клетки на гладката мускулатура на аортната плъх се гладуват в серум и се излагат на пикочна киселина (3 mg/dL) до 96 часа. Пикочна киселина (UA, 3 mg/dL) предизвиква фосфорилиране на ERK1/2 MAP киназа. A, пикочна киселина (3 mg/dL) също индуцира експресия на mRNA на PDGF-A-верига (B), C-верига (C) и α-рецептор (D), но не и експресия на mRNA на PDGF-B-верига. А, Western blot, показващ наличието на фосфорилирани p44 и p 42 (горен панел) и нефосфорилирани p44 и p42 MAP киназа (долен панел); В до D, анализ за защита на RNAase.
Повишаването на пикочната киселина, настъпило с мутация на уриказа по време на миоцена, следователно може да е осигурило предимство за оцеляване (Фигура 5). Очаква се стимулацията на ренин ангиотензиновата система да повиши остро кръвното налягане и реабсорбцията на натрий, докато прегломеруларното съдово заболяване, индуцирано от активиране на MAP киназа, PDGF и COX-2, би довело до хронична сол чувствителност. Нетният ефект ще бъде поддържането на кръвното налягане и натриевия баланс.
Фигура 5. Предложен механизъм, чрез който мутацията на уриказа предоставя полза за оцеляване на миоценовите хоминоиди. Налягането на околната среда през средата до края на миоцена доведе до предимство за оцеляване на хоминоидите, които биха могли по-добре да запазят натрия и да поддържат кръвното налягане. При животни, които са имали мутация в гена на уриказа, увеличаването на серумната пикочна киселина рязко повишава кръвното налягане и поддържа запазването на натрий поради действието на пикочната киселина за засилване на активирането на ренин ангиотензиновата система в отговор на диета с ниско съдържание на сол. Пикочната киселина също индуцира бъбречно микроваскуларно заболяване чрез стимулиране на пролиферацията на гладкомускулни клетки с активиране на MAP киназа и стимулиране на PDGF, COX-2 и ренин ангиотензиновата система. Развитието на бъбречно микроваскуларно заболяване и интерстициално възпаление причинява чувствителност към солта и хронично повишаване на кръвното налягане. Активирането на тези 2 основни пътя (ренин ангиотензин и COX-2 и PDGF-индуцирано микросъдово заболяване) води до трайно повишаване на кръвното налягане с поддържане на натриевия баланс.
Пикочна киселина: потенциална роля в хипертонията и сърдечно-съдовите заболявания в индустриализираните общества
Докато повишената серумна пикочна киселина може да е от полза за поддържане на кръвното налягане при диетични условия с ниско съдържание на сол, очаква се предизвикването на хронична чувствителност към солта да доведе до хипертония в съвременното общество с диета с високо съдържание на сол. Интересно е, че хиперурикемията предсказва развитието на хипертония и е силно свързана със сърдечно-съдови заболявания. 30–32,36,37 Серумна пикочна киселина също е по-висока в почти всички високорискови групи, включително мъже и жени в менопауза (тъй като естрогенът е урикозуричен), при синдром на резистентност към инсулин на затлъстяването (тъй като инсулинът може да стимулира реабсорбцията на пикочна киселина), при чернокожи и при пациенти с бъбречно заболяване (вследствие на намалена екскреция). 38,39 Може да се предположи, че по-високите нива на пикочна киселина в чернокожите могат да отразяват по-дълъг период на индуцирано от околната среда селекционно налягане след делецията на гена на уриказа.
По няколко причини съществуват противоречия относно ролята на пикочната киселина в сърдечно-съдовите заболявания. Първо, някои власти разглеждат хиперурикемията като „маркер“ за пациенти с повишен сърдечно-съдов риск, за разлика от това, че са наистина патогенни. 40 Това заключение се основава на няколко епидемиологични проучвания, които не могат да покажат, че пикочната киселина е независима от други фактори като хипертония за прогнозиране на сърдечно-съдови събития. 40 Факторът обаче не трябва да е независим, за да има причинно-следствена роля в болестния процес. Например, ако хиперурикемията е причина за хипертония, не се очаква да бъде независима от нея като рисков фактор за сърдечно-съдови събития. Доказателствата, че пикочната киселина може да има причинно-следствена роля при хипертония, се предлагат от експерименталните проучвания на лека хиперурикемия при плъхове. 14,15 Освен това, въпреки че хиперурикемията не винаги е независим рисков фактор за сърдечно-съдови събития, тя винаги е била установена като независим рисков фактор за развитие на хипертония. 30,31 Това предполага, че причинно-следствената връзка между пикочната киселина и хипертонията може отчасти да обясни разликата в епидемиологичните проучвания относно ролята на пикочната киселина в сърдечно-съдовите заболявания.
Второ, някои автори предполагат, че хиперурикемията може да бъде вторичен отговор на намаления бъбречен кръвоток, който е характерна хемодинамична находка при хипертония. Съществуват сериозни доказателства, че бъбречната вазоконстрикция води до повишена проксимална реабсорбция на урат и увеличаване на серумната пикочна киселина. 42 Хиперурикемия може да се появи и при пациенти със застойна сърдечна недостатъчност или периферна съдова болест поради тъканна исхемия, която увеличава генерирането на пикочна киселина (от разграждането на АТФ) и намалява екскрецията на урат (причинена от ефектите на лактата върху органичния анионообменник). Въпреки че няма съмнение, че тези състояния водят до повишаване на серумните нива на пикочна киселина, това не трябва непременно да означава, че повишаването на серумната пикочна киселина е без биологичен ефект. Наистина, нашите проучвания предполагат, че повишаването на пикочната киселина при тези състояния може да представлява механизъм за обратна връзка за увеличаване на ренин ангиотензиновата система, за да стимулира максимално реабсорбцията на натрий и да поддържа кръвното налягане, тъй като може да има намален бъбречен кръвоток и/или тъканна исхемия сигнализирайки на организма, че общият му обем на кръвта е нисък.
Перспективи
Представяме хипотезата, че мутацията на уриказа, настъпила по време на ранната еволюция на хоминоидите, първоначално е била изгодна, тъй като е помогнала за поддържане на кръвното налягане както остро (чрез стимулиране на ренин ангиотензиновата система), така и хронично (чрез индуциране на чувствителност към солта чрез развитие на бъбречни микросъдови и интерстициална болест). В съвременното общество преминаването към диета с високо съдържание на сол, заедно с тази мутация, може да има важна роля в настоящата епидемия от хипертония и сърдечно-съдови заболявания. Други хранителни фактори (като хранителни промени в калия и магнезия) и развитието на затлъстяване също вероятно ще бъдат фактори, допринасящи за развитието на хипертония. Въпреки че трябва да се внимава при тълкуването на експериментални модели, предлагаме да се извършат проучвания, за да се определи ефектът от понижаването на пикочната киселина при човека върху развитието на хипертония, особено преди развитието на значително микросъдово и бъбречно увреждане.
Тази работа беше подкрепена от безвъзмездни средства HL-68607 и DK-52121 от Националните здравни институти.
- Пикочна киселина и хранене на растителна основа
- Диета с пикочна киселина Отправна точка към подагра свобода
- Камъни в пикочната киселина Причини, симптоми, лечение; Предотвратяване
- Камък от пикочна киселина - общ преглед на ScienceDirect теми
- Пикочна киселина - общ преглед на ScienceDirect теми