Чанбин Лий
1 Катедра за интегрирана биологична наука, Национален университет в Пусан, 63–2, Пусандаехак-ро, Геумджонг-гу, Пусан 46241, Корея; rk.ca.nasup@201bcl (C.L.); rk.ca.nasup@nueij (J.K.)
Jieun Kim
1 Катедра за интегрирана биологична наука, Национален университет в Пусан, 63–2, Пусандаехак-ро, Геумджонг-гу, Пусан 46241, Корея; rk.ca.nasup@201bcl (C.L.); rk.ca.nasup@nueij (J.K.)
Йънгми Юнг
1 Катедра за интегрирана биологична наука, Национален университет в Пусан, 63–2, Пусандаехак-ро, Геумджонг-гу, Пусан 46241, Корея; rk.ca.nasup@201bcl (C.L.); rk.ca.nasup@nueij (J.K.)
2 Департамент по биологични науки, Национален университет в Пусан, 63–2, Пусандаехак-ро, Geumjeong-gu, Пусан 46241, Корея
Резюме
1. Въведение
2. Патогенеза на NAFLD/NASH
Натрупването на излишни мазнини в черния дроб води до оксидативен стрес и/или ендоплазмен стрес и в крайна сметка води до клетъчна дисфункция и апоптоза [63,64,65]. Повредените хепатоцити от липотоксичност се подлагат на апоптоза и тези умиращи хепатоцити произвеждат реактивни кислородни форми (ROS), свързани с увреждане молекулни модели, звукови таралежи от таралеж и др. [66,67,68,69]. Тези освобождаващи фактори допълнително стимулират възпалителните реакции чрез активиране на резидентните макрофаги и предизвикват фибротично възстановяване в черния дроб [70,71,72]. Тъй като хепатоцитите са основните чернодробни паренхимни клетки, изпълняващи основните функции на черния дроб, тежка загуба на хепатоцити и последваща компенсаторна пролиферация на непаренхимни клетки, като Kupffer клетки, чернодробни звездни клетки (HSC) и прогениторни клетки, водят до загуба на черния дроб функция и чернодробна недостатъчност и в крайна сметка загуба на живот [73,74,75]. Следователно, предотвратяването на смъртта на хепатоцитите чрез регулиране на липидния метаболизъм може да бъде терапевтична стратегия за лечение с NASH.
3. Естроген и естроген сигнализиране в черния дроб
Протеинът на разклонителната кутия А1 (FOXA1) влияе върху активността на естроген/ERα комплекс чрез индуциране на нуклеозомно пренареждане, което позволява на естроген/ERα комплекса лесно да оцени промоторно-проксималните области на целевите гени [113,114,115,116]. В черния дроб е известно, че FOXA1 участва в блокирането на натрупването на липиди в хепатоцитите чрез инхибиране на синтеза на TG и насърчаване на β-окислението [117]. Проучване показа, че експресията на FOXA1 в здравия черен дроб е по-висока при жените, отколкото при мъжете, и нивото му намалява в NAFL в сравнение със здравия черен дроб [117]. Тези резултати показват, че FOXA1 може да бъде свързан с неравенство между половете в развитието на NAFLD. Li et al. демонстрира, че FOXA1/2 играе доминираща роля в половия диморфизъм на развитието на HCC, като представя защитното действие на FOXA1/2 при женски мишки от индуцирано от диетилнитрозамин (DEN) развитие на HCC [113]. Анализът на целия геном показа, че целевите гени на ERα се припокриват до голяма степен с тези на FOXA1/2 и взаимодействието между FOXA1/2 и ERα е важно за модулирането на експресията на гени, свързани с HCC резистентност. Няма обаче преки доказателства, свързващи FOXA1 и естрогени в патогенезата на NAFLD/NASH и са необходими допълнителни проучвания.
4. Различия между половете в NAFLD/NASH
Патогенезата на NAFLD включва прогресивни етапи от натрупване на мазнини, до смърт на хепатоцити, до възпаление и фиброза [37,54]. Индуцираната от липотоксичност смърт на хепатоцитите е основният отличителен белег за прогресирането на NAFL в NASH [38]. Също така се свързва с възпалителен и фиброзен отговор [66,69]. Като се има предвид по-голямото разпространение на NAFLD при мъжете, отколкото при жените, и повишения риск при жените в менопауза и след менопауза [28,29], естрадиолът изглежда предпазва черния дроб от чернодробни увреждания, като потиска натрупването на липиди, възпалението и фиброзата. Следователно е необходимо да се разбере действието на естрогените в чернодробния отговор на увреждане, за да се разкрие разликата между половете в NAFLD/NASH и да се разработи терапевтична стратегия, основана на пола. В този раздел обобщихме и обсъдихме предишни доклади относно ефектите от пола, репродуктивното състояние и естрадиола върху прогресията на NAFLD/NASH.
4.1. Липидно натрупване и липотоксичност
Когато мастните киселини се доставят в излишък или тяхното изхвърляне е нарушено, те могат да служат като субстрати за генериране на липотоксични видове, които провокират ендоплазмен стрес и хепатоцелуларно увреждане [67]. По този начин нарушеният метаболизъм в черния дроб води до прекомерно натрупване на токсични липиди в хепатоцитите. Липотоксичността е една от основните причини за дисфункция на хепатоцитите и последваща хепатоцелуларна смърт, водеща до прогресиране на NASH [9,68,118]. Натрупващите се данни показват, че масивната смърт на хепатоцитите е ключов патогенен двигател, който допринася за възпалението на черния дроб и фиброгенезата по време на прогресията на NASH [8,9]. При липотоксичност увредените или умиращи хепатоцити освобождават различни цитокини, които активират възпалителни клетки и HSC [8,69]. Следователно липотоксичността и последващата хепатоцелуларна смърт се считат за важна връзка между NAFL и NASH [119]. Следователно е необходимо да се изяснят половите разлики в индуцираната от липотоксичност хепатоцелуларна увреда и ефектите на естрадиола върху оцеляването на хепатоцитите, за да се разберат разликите между половете в NAFLD/NASH.
4.2. Чернодробно възпаление
Възпалението е сложно свързано с хепатоцелуларна смърт [129]. Увредените хепатоцити, причинени от натрупване на липиди, освобождават паракринни стимули, за да предизвикат чернодробно възпаление, което придружава фиброза, като в крайна сметка ускорява прехода от NAFL към NASH [65,66,72,130]. По този начин възпалението с фиброза е основният отличителен белег на NASH [131]. Клетките на Kupffer, за които е добре известно, че участват в регулирането на чернодробното възпаление, се разширяват бързо в ранните стадии на NAFLD чрез секретиране на цитокини и хемокини, като интерлевкин-1β (IL-1β), интерлевкин-6 (IL-6), фактор на туморна некроза -α (TNF-α), моноцитен хемоаттрактант протеин-1 (MCP-1) и хемокин (CC мотив) лиганд 5 (CCL5), за да предизвика провъзпалителен отговор [70,132,133,134]. Получените от кръвта моноцити и неутрофилите, получени от костния мозък, също допринасят за инициирането и прогресирането на NASH, като насърчават производството на провъзпалителни медиатори, като IL-6 и TNF-α [135].
4.3. Чернодробна фиброза
5. Терапия, основана на пола за NAFLD/NASH
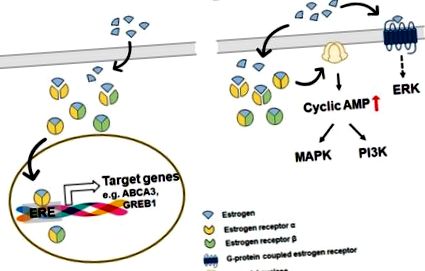
Схема, изобразяваща защитните действия на естрогена в черния дроб. Схемата изобразява хепатопротективните действия на естрогена срещу неалкохолна мастна чернодробна болест (NAFLD). Естрогените се свързват с естрогенните рецептори (ER) в чернодробните клетки и се транслокират в ядрото на целевите клетки, където регулират генната експресия. В хепатоцитите естрогенът, свързан с ERα (оцветен като жълто), облекчава липотоксичния стрес в тези клетки, като потиска de novo липогенезата и насърчава β-окислението. Естрогенът/ERα намалява експресията на свързани с липогенезата de novo гени, като синтаза на мастни киселини (FAS), ацетил-CoA карбоксилаза (ACC), стеароил-CoA десатураза (SCD) и стерол регулаторен елемент-свързващ протеин (SREBP) и увеличава експресията на гени, свързани с β-окислението, като карнитин палмитоилтрансфераза 1 (CPT1). Естрогенът се свързва с ERα в клетките на Kupffer, които са макрофаги, пребиваващи в черния дроб. Естроген-свързаният ERα инхибира производството на IL-6 и секрецията на провъзпалителни цитокини в тези клетки, като в крайна сметка намалява възпалението. В HSCs, естрогените, свързани с ERβ, регулиращи гените, свързани с апоптоза, и регулиращи профибротичните гени, като α-гладкомускулен актин (α-SMA), колаген и матрични металопептидази (MMP), намаляват фиброзата на черния дроб.
6. Заключения
Принос на автора
C.L., J.K. и Y.J. допринесоха за тази статия с концепцията и дизайна на изследването, прегледа и анализа на литературата и изготвянето и редактирането на ръкописа; Y.J. получи финансиране.
Финансиране
Тази работа беше подкрепена от Националната изследователска фондация (NRF) на Корея, финансирана от корейското правителство (MSIT) (2018R1A2A3075038) на Youngmi Jung.
Конфликт на интереси
Авторите не декларират конфликт на интереси.
- Модифицираното лекарство на Паркинсон показва потенциал за лечение на неалкохолна мастна чернодробна болест
- Средиземноморска диета и безалкохолна мастна чернодробна болест
- Безалкохолната мастна чернодробна болест и сърдечно-съдови заболявания Дойде време кардиолозите да го направят
- Безалкохолна мастна чернодробна болест (NAFLD) за предотвратяване ролята на средиземноморската диета и физическия
- Безалкохолна мастна чернодробна болест (NAFLD) ГАСТРОИНТЕСТИНАЛ; СПЕЦИАЛИСТИ ЗА ЧЕРЕН ДЪРВЪК НА TIDEWATER, PLLC