Фернанда Берти Роча Мендес
1 Медицински стажант в дерматологичния отдел на Регионална болница Presidente Prudente - Университет на Oeste Paulista (HRPP-UNOESTE) - Presidente Prudente (SP), Бразилия.
Адаукто Хиса-Елиан
2 г-жа професор - Катедра по дерматология, Медицински факултет, Университет на Serra dos Órgãos - (UNIFESO) - Teresópolis (RJ), Бразилия.
Марилда Апаресида Миланес Моргадо де Абреу
3 Професор (доктор) - Катедра по дерматология - Училищна медицина, ръководител на резиденцията по дерматология в болницата Regional de Presidente Prudente - University of Oeste Paulista (HRPP-UNOESTE) - Presidente Prudente (SP), Бразилия.
Virgínica Scaff Gonçalves
1 Медицински стажант в дерматологичния отдел на Регионална болница Presidente Prudente - Университет на Oeste Paulista (HRPP-UNOESTE) - Presidente Prudente (SP), Бразилия.
Резюме
Dermatitis herpetiformis (DH) или болестта на Duhring-Brocq е хронично булозно заболяване, характеризиращо се с интензивен сърбеж и усещане за парене в еритематозните папули и уртикарни плаки, групирани везикули с растеж на центрофуги и напрегнати мехури. Съществува връзка с генотипите HLA DR3, HLA DQw2, открити в 80-90% от случаите. Това е IgA-медиирано кожно заболяване, като отлаганията на имуноглобулин А се появяват в гранулиран вид в горната част на дермалната папила в областта на сублиминалната денза на базалната мембрана, която присъства както в засегнатата кожа, така и в здравата кожа. Същият протеин IgA1 с J верига се открива в лигавицата на тънките черва при пациенти с целиакия при възрастни, което предполага силна връзка с DH. Специфични антитела като антиендомизий, антиретикулина, антиглиадин и, наскоро идентифицирани, епидермални и тъканни подтипове трансглутаминаза, както и повишено производство на зонулин, са общи за двете състояния, заедно с чувствителната към глутен ентеропатия и DH. Автоимунните заболявания представляват по-високи нива на разпространение, като щитовидна жлеза (5-11%), пернициозна анемия (1-3%), диабет тип 1 (1-2%) и заболяване на колагеновата тъкан. Избраното лечение е дапсон и диета без глутен.
Резюме
ВЪВЕДЕНИЕ
Булозните заболявания представляват една от най-необикновените глави на дерматологията. Разнообразието от логически механизми на патофизио, подчинено на разнообразната им етиология, широк спектър от клинични прояви с често системно участие на заболяването, изисква добре проведен метод за медицинска оценка; следователно, да се превърне в изненадващи трудности, които изискват специализирано лечение и хабилитация при преодоляване на диагностичното и терапевтичното предизвикателство.
Мехурчетата са ефлоресценция, пълнеща се с течност, съставена от плазма и възпалителни клетки, в резултат на промяната на клетъчните структури и структурите на междуклетъчните връзки, отговорни за адхезията на епителната тъкан. 1-4 Везикулите са известни като диаметър на кухината по-малък от 0,5 cm, а мехурчето е по-голямо от 0,5 cm, интраепидермално, ако лезията присъства в базалния слой до роговия слой. 1-2 Чрез познаване на патофизиологията на равнината на разцепване, характеристиките на възпалителния инфилтрат и особено механизма на образуване на мехури, е възможно да се разграничат булозни дерматози. 1,2,5
ДЕРМАТИТ ХЕРПЕТИФОРМИС
Dermatitis herpetiformis (DH) е описан през 1884 г. от дерматолога Луис Дюринг, който го поставя в същата клинична категория като пемфигус и пемфигоид, като по този начин съставя класа на булозни заболявания. 2,6,7 През 1888 г. Brocq описва подобни кожни лезии, диагностицирани като „полиморфен сърбежен дерматит“ и след проучване на доклада на Дюринг, признава, че става въпрос за същата патология. Следователно, болестта на Дюринг-Брок сега се използва като синоним на DH. 2
През 1943 г., чрез разграничаване на везикулационния механизъм, Civatte диференцира пемфигус (интраепидермални були), пемфигоид и DH (образуване на мехури в зоната на базалната мембрана). 7
Връзката с цьолиакия, глутенчувствителна ентеропатия и DH се наблюдава през шейсетте години от Mards et al., Fry et al. и Shuster et al. 2,7
Епидемиологично DH е рядко заболяване. 3,8,9,10 Засяга предимно млади хора, въпреки че е диагностициран при кърмачета на възраст осем месеца, както и при възрастни хора на деветдесет години. 3,6,7,11,12 Мъжете са по-засегнати, със съотношение 2: 1, но при пациенти под 20 години съотношението е 12 жени за всеки 8 мъже. 3,13,14 Разпространението на DH варира в различните страни, като 1: 1 000 000 нови случая/година в Германия, 11 на 100 000 в Шотландия; 20-39 на 100 000 в Швеция и 58,8 на 100 000 в Ирландия. 7,9,15,16
Има съобщения за заболяване при други членове на същото семейство, било DH или целиакия при възрастни, в 2,3 до 10,5% от случаите. 7,11,14
Етиопатогенезата има имунологична причина, но не е напълно изяснена. Известно е, че има по-висока честота на генотипове HLA DR3, HLA DQw2 при 80-90% от пациентите, HLA B8 и HLA DQ8 в 1020% от случаите, както и на целиакия при възрастни. 1-3,8,9,13,16
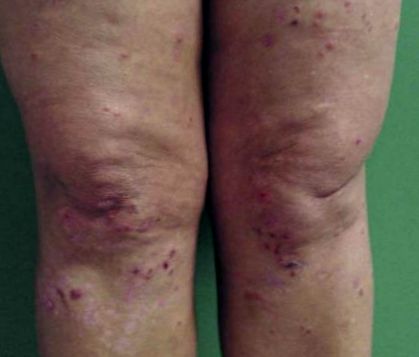
Кожните лезии започват със сърбеж или усещане за парене в еритематозни папули и уртикарни плаки. Има групирани везикули и напрегнати мехури с центробежен растеж, чието съдържание може да бъде серозно или хеморагично, със симетрично разпределение (Фигури 1, 2 2 и и 3). 3). 3,6,8,17,18 Булозните елементи се разкъсват, кулминирайки в оголени зони на ексулцирана кожа и кора. Впоследствие има остатъчна хипопигментация или хиперпигментация. 8,16
Херпетиформис на дерматит: еритематозни плаки, групирани везикули, ексулцерации и кръвна кора в долните крайници
Дерматит херпетиформис. Везикули, дисектирани с корички и остатъчни хипопигментирани макули на коленете
Дерматит херпетиформис. Еритематозни папули и уртикарни плаки, везикули с хеморагично съдържание, оголени, ексулцирани области и струпеи, с остатъчна хипопигментация на гърба и горния крайник
Топографията обикновено е засегната от разгъващите области: долни крайници (предно бедро и коляно), лакти, седалище и сакрална област, въпреки че рамото, скапуларната област и скалпът също могат да бъдат засегнати. 1,8 Лезиите в устната лигавица са необичайни. 8,9
Стомашно-чревна клинична проява на чувствителна към глутен ентеропатия може да се появи на всяка възраст, било то в детска възраст, когато зърнените храни се въвеждат в оралната диета, или в зряла възраст без предварителна реакция на непоносимост към храна. Симптомите включват диария, стеаторея, малабсорбция с получена анемия, метаболитно костно заболяване, загуба на тегло и недохранване. Въпреки това някои пациенти нямат стомашно-чревни признаци или симптоми, тъй като по-голямата част от пациентите с DH са безсимптомни, тъй като само 20% от тях развиват чревни симптоми. 19.
Глутенът е аморфен протеин, съставен от глиадин и глутенинови аминокиселини, които се намират в семена на зърнени култури от семейство Граменеи, като пшеница, ечемик, овес, малц и ръж. Те са зърнени култури, които съдържат нишесте, липиди и протеини (глиадин, глутенин, албумин и глобумин). Пшеничният протеин се състои специално от 68% глиадин и 32% глутамин, поради което той обикновено се нарича пшеничен глутен. Примери за хранителни продукти, които съдържат този протеин, са брашно, шоколадово мляко, което съдържа малц, топено сирене, бира, уиски, водка, горчица, кетчуп, майонеза и салам. 20,21
Типичната находка по отношение на DH е отлагането на IgA имуноглобулин в гранулиран модел в горната част на дермалната папила в областта на сублиминалната денза на базалната мембрана, което присъства както в засегнатите области на кожата, така и в здравата кожа. 8,9,19 Това може да бъде премахнато само чрез приемане на безглутенова диета в продължение на няколко години, тъй като дори лекарствената терапия не променя този модел. 2,3
Пациентите представят чувствителна към глутен ентеропатия, диагностицирана чрез атрофия на вили в биопсия на тънките черва, в допълнение към специфични антитела в серума, въпреки че повечето от тях са асимптоматични. 8,9,12,22-24
Същият протеин IgA1 с J верига и секреторен компонент, открит в лигавицата на тънките черва при целиакия при възрастни, също присъства в кожата на пациенти с DH, което предполага силна връзка между двете заболявания. 1,8 Други антитела като специфичен ендомизий, антиретикулина, глиадин и, наскоро идентифицирани, подвидовете на епидермалната и тъканната трансглутаминаза, както и свръхпроизводството на зонулин, се откриват и при двете състояния, заедно с ентеропатична чувствителност към глутен и DH. 25-29 IgM, IgG и C3 също могат да присъстват.
Проучванията показват, че кръстосаната реакция възниква между някои вещества, тъй като те представляват общи епитопи и следователно са признати като автоантигени, отключващи заболяването. 24
Автоимунните заболявания с висока асоциация включват щитовидна жлеза (5-11%), пернициозна анемия (1-3%), диабет тип 1 (1-2%) и заболяване на колагеновата тъкан. 8,9,14,16,30 По този начин Caproni et al. предлагат скрининг за автоимунни заболявания при пациенти с DH, като определяне на антипероксидазни антитела (присъстват в 20% от случаите), TSH, T4 и T3, анти-стомашни париетални клетки (10-25% положителни), ANF, anti -Ro/SSA и глюкоза. 16.
През 1970 г. Gjone & Nordoy са първите, които съобщават за повишена честота на лимфом при пациенти с DH, което е потвърдено в продължение на десетилетия, особено Т-клетъчен лимфом. 14,16,31-3 Въпреки това, Lewis et al, в проучване на 846 пациенти, публикувано през 2008 г., противоречи на тази връзка, като не открива повишен риск от смъртност при тези пациенти. 30
Въпреки че 100% от пациентите с DH имат чувствителност към глутенова ентеропатия, само малка част развиват симптоми на колики или чревна малабсорбция, описано е съотношението 1: 5. 7,10,20 Има доказателства, че безглутеновата диета сама по себе си води до подобряване или дори пълна ремисия на чревните симптоми и подобряване на кожните лезии при DH. 7,11,18
Кожната биопсия трябва да идва от нова, непокътната була. 14 Хистопатологични проучвания разкриват микроабсцеса на Piérard върху дермалната папила, образувана от неутрофили и еозинофили, неакантолитични мехури, които първоначално показват субепидермални мултилокуларни кухини, които се сливат, образувайки еднолокуларни кухини, и периваскуларен лимфоцитен възпалителен инфилтрат в горния дермис. 1,2,3,6 Патологията не диференцира DH от други автоимунни булозни заболявания като булозен пемфигоид, линейна IgA дерматоза и епидермолиза bullosa acquisita. 14.
Директната имунофлуоресценция на засегнатата перилезиална кожа е златният стандарт за потвърждаване на диагнозата с отлагане на IgA1 в гранулиран модел в lamina lucida на зоната на базалната мембрана (Фигура 4). 2,9,34,35 По-малко от 5% от случаите представят депозити на IgA в линеен модел, който трябва да се различава от линейна IgA дерматоза. 7 Съобщава се, че фибриларен IgA стандартен депозит е открит при 50% от японската популация с HD, но няколко автори се съмняват дали отговаря на вариант на DH, различно заболяване или само на променлив модел, последващ надлъжна и напречна ориентация на микрофибрилите, визуализиран чрез електронна микроскопия, както е предложено от Ko CJ et al. 36 Понякога е необходимо да се извърши втори тест за диагностика, тъй като по време на ранните етапи на заболяването тази типична характеристика може да не бъде открита. Депозитът на имуноглобулин А не се променя с дапсон, но приблизително две години безглутенова диета отменя тази констатация. 1
Директна имунофлуоресценция. Флуоресценция в гранулиран модел в зоната на базалната мембрана
Индиректната имунофлуоресценция може да бъде полезна за откриване на наличието на автоантитела и циркулиращи анти-ендомизиални, анти-глиадинови и анти-ретикулинови IgA и анти-епидермални трансглутаминазни антитела. 1,2
Тъканните трансглутаминазни антитела (anti-tTG) могат да бъдат измерени чрез ELISA, показващи повече от 90% специфичност и чувствителност от 47-95%. Използва се за диагностициране на DH и за оценка на придържането на пациентите към безглутенови диети и чревни увреждания. Anti-tTG е 64% хомоложна на антиепидермалната трансглутаминаза (anti-eTG), която действа срещу специфичния антиген в DH. 16,37 Jaskowski et al. предполагат, че 20% от пациентите имат анти-tTG отрицателни, но тези пациенти са antieTG положителни. Същите автори откриха по-висока чувствителност на анти-eTG, което може да помогне в случаи на трудна диагноза. Разпространението на анти-eTG намалява при деца в сравнение с възрастни. 37
IgA1 антителата срещу гладката мускулатура имат 100% специфичност и 52 до 100% чувствителност при диагностицирането на DH. Въпреки това, анти-tTG може да липсва при пациенти с диети без глутен. 16.
Проучванията показват, че 100% от пациентите с DH проявяват хистопатологични промени в целиакия, т.е. вилозна атрофия, характеризираща аспект плоски повърхнини кубоидни епителни клетки, които губят ориентацията на базовото ядро, увеличена пролиферация на криптова клетка, причиняваща хиперплазия и загуба на техните структури с повишени лимфоцити и плазмоцитни клетки в ламина проприа. Тези находки не са патогномонични за спру, но връщането на хистологичния модел след диета без глутен потвърждава диагнозата. 19.
Вилозна атрофия на биопсия на лигавицата на тънките черва, установена при повечето пациенти с DH, е по-малко тежка, отколкото при целиакия или липсва тропическа спру. 7-9 Тестът за абсорбция D-ксилоза се променя в 10-33% от случаите. Откриването на желязодефицитна анемия или мегалобластна анемия при дефицит на фолиева киселина и стеаторея не е необичайно. 2
Въпреки че клиничните прояви на D се различават силно в ЕС, и двете се подобряват значително при безглутенови диети. Тази мярка осигурява облекчаване на усещането за сърбеж и парене на везикуло-еритематозната папула, разпространена или локализирана върху кожата. Понякога причинява пълна регресия на кожните прояви. Това поведение изглежда чудесно за прогнозата на заболяването. Въпреки това е трудно и трудно у нас, тъй като глутенът е повсеместно вещество и не всички хранителни продукти на пазара съдържат изрична информация относно наличието или липсата на глутен. Освен това високата цена на алтернативни продукти, предлагани на пациенти с чувствителност към глутен, представлява финансова пречка за повечето бразилски граждани. По този начин е много трудно да се придържате и зависи от решителност, насоки и инвестиции. 9,38,39 Йодът строго ограничение също се предлага от някои автори. 13
Лечението е успешно при пациенти, които понасят дапсон. 2,3,6 Началната доза обикновено е между 100-200 mg на ден и отговорът настъпва в рамките на три часа до два дни, без да се появяват нови лезии. 2,9 Пациентът трябва да приема минимална доза, достатъчна за потискане на заболяването. Някои пациенти приемат 25 mg дапсон седмично, но други се нуждаят от 400 mg дневно. 2
Страничните ефекти на лекарствата са зависими от дозата. 50 mg дапсон могат да причинят известна хемолиза. Дози от 150 mg могат да намалят 2 грама хемоглобин, което може да бъде асимптоматично при здрави пациенти или да предизвика няколко симптоми и признаци при пациенти със сърдечни или белодробни заболявания или дори при възрастни хора. 2
Метхемоглобинемията е окисляване на желязо (Fe +2) от хемоглобин до желязо, (Fe +3), причинено от химично вещество. Прогресира с утаяване на еритроцити и хемолиза, характеризираща се с тела на Хайнц и „ухапани клетки“. Метхемоглобинът причинява отклонение на кривата на дисоциация на кислорода вляво, което води до недостатъчен кислород за тъканите. 19.
Метхемоглобинемията обикновено е под 5% и не надвишава 12% при DH. Признаците и симптомите се проявяват при метхемоглобин 3%, характеризиращ се с цианоза, сивкав цвят, слабост, главоболие, тахикардия, гадене и коремна болка. 2
Други неблагоприятни ефекти са периферната невропатия (обратима при намаляване на дозата); морбилиформно изригване, еритема нодозум, мултиформен еритем, ексфолиативен дерматит, токсична епидермална некролиза, тежка хипоалбуминемия с анасарка, левкопения, агранулоцитоза, която може да бъде фатална през първите три месеца, холестаза и хепатит. 2,40 Сулфоновият синдром обикновено се проявява в рамките на 6 седмици от лечението, независимо от дозировката, и се характеризира с ексфолиативен дерматит, хепатит, треска, лимфаденопатия, левкоцитоза, главоболие, повръщане и хемолиза. 41,42
Поради както страничните ефекти, така и тежестта на някои случаи, пациентите, приемащи дапсон, трябва да бъдат внимателно и непрекъснато наблюдавани. За да се избегнат катастрофални събития преди започване на лечението, трябва да се изследва дефицитът на ензима глюкозо-6-фосфат дехидрогеназа, тъй като той се развива с тежка хемолиза, тъй като ензимът метхемоглобин редуктаза - (NADPH-метхемоглобин редуктаза) - зависи от действието на NADPH. 2,19 Пълна хемограма трябва да се прави седмично през първия месец, на всеки две седмици в рамките на два месеца и често по време на лечението. Бъбречни и чернодробни тестове също трябва да се изискват преди започване на лечението с редовно наблюдение. 2
Пациентите, които не могат да понасят употребата на дапсон, могат да се възползват от сулфапиридин (1 до 1,5 g/ден, тетрациклин 2 g/ден, заедно с никотинамид 1,5 g/ден или циклоспорин за резистентни случаи). 2,11,42 Sacchidanand S. et. всички разкриха задоволителни резултати с импулсна терапия с дексаметазон-циклофосфамид. 43
Важно наблюдение е, че противовъзпалителните лекарства обикновено влошават DH. 43
Прогнозни курсове с периоди на ремисия и обостряне. 3,44 Емоционално събитие или инфекция може да предизвика ново влошаване на заболяването. 9
ЗАКЛЮЧИТЕЛНИ СЪОБРАЖЕНИЯ
Изключително важно е булозните заболявания да бъдат разпознавани от клиницистите, за да се предотврати влошаване на симптомите с противопоказани или неефективни лекарства, тъй като особените характеристики на булозната болест представляват висок риск от сериозни и системни последици, произтичащи от електролитен дисбаланс. 43,44
Бележки под линия
Финансова подкрепа: Няма.
Конфликт на интереси: Няма.
* Работа, извършена в Дерматологичния отдел в Регионалната болница на Президенте Пруденте - Университет на Оесте Паулиста (HRPP-UNOESTE) - Президенте Пруденте (SP), Бразилия.
- Преглед на доказателствата за диетичните влияния върху атопичния дерматит
- Безалкохолни мастни чернодробни заболявания и диети с ниско съдържание на въглехидрати Годишен преглед на храненето
- Безалкохолно мастно чернодробно заболяване Клиничен подход и преглед
- Skinny Gut Diet Shake Review
- Излагане на озон, сърдечно-белодробно здраве и затлъстяване Съществен преглед Химически изследвания в