В клинични проучвания повечето пациенти са постигнали клинично значима загуба на тегло ≥5% със Saxenda ®1
Пациенти, отслабнали със Saxenda ®
В едногодишно проучване 85% от пациентите, лекувани със Saxenda ®, са загубили малко тегло 1
В 56-седмично проучване на 3731 пациенти без диабет тип 2 и с ИТМ ≥30 или ≥27% с най-малко 1 свързана с теглото коморбидност, пациентите са рандомизирани или на Saxenda ® (n = 2 487), или на плацебо (n = 1 244), като всички пациенти получават нискокалорична диета (
500 kcal/ден дефицит) и консултации за физическа активност. 1
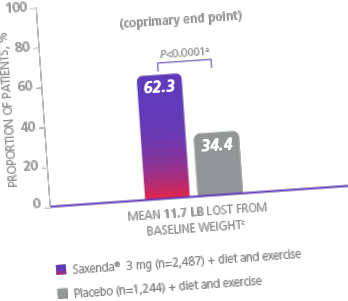
По-голямата част от пациентите са постигнали клинично значима загуба на тегло ≥5% със Saxenda ®1
Разлика от плацебо (най-малки квадрати [LS]) означава, 27,9% [95% CI, 23,9. 31.9]).
b Разлика от плацебо (LS средна стойност), 18,5% (95% CI, 15,2, 21,7).
c Загуба на тегло в лири (lb), изчислена като 5%, 10% или 20% от средното изходно телесно тегло.
d Въз основа на честотното кумулативно разпределение на промяната в кривата на телесното тегло.
- Първичните крайни точки бяха средно процентно изменение на теглото, процент на пациентите, постигнали ≥5% от изходната загуба на тегло, и процент на пациентите, постигнали> 10% от изходната загуба на тегло 1
- Загубата на тегло се определя като всяко намаляване на теглото от началото на проучването 1
- Средното изходно телесно тегло е 233,9 lb, а средният изходен ИТМ е 38,3 kg/m 2 1
Разлика от плацебо (най-малки квадрати [LS]) означава, 27,9% [95% CI, 23,9. 31.9]).
b Разлика от плацебо (LS средна стойност), 18,5% (95% CI, 15,2, 21,7).
c Загуба на тегло в лири (lb), изчислена като 5%, 10% или 20% от средното изходно телесно тегло.
d Въз основа на честотното кумулативно разпределение на промяната в кривата на телесното тегло.
- Първичните крайни точки бяха средно процентно изменение на теглото, процент на пациентите, постигнали ≥5% от изходното отслабване, и процент на пациентите, постигнали> 10% от изходното отслабване 1
- Загубата на тегло се определя като всяко намаляване на теглото от началото на проучването 1
- Средното изходно телесно тегло е 233,9 lb, а средният изходен ИТМ е 38,3 kg/m 2 1
Разлика от плацебо (най-малки квадрати [LS]) означава, 27,9% [95% CI, 23,9. 31.9]).
b Разлика от плацебо (LS средна стойност), 18,5% (95% CI, 15,2, 21,7).
c Загуба на тегло в лири (lb), изчислена като 5%, 10% или 20% от средното изходно телесно тегло.
d Въз основа на честотното кумулативно разпределение на промяната в кривата на телесното тегло.
- Първичните крайни точки бяха средно процентно изменение на теглото, процент на пациентите, постигнали ≥5% от изходното отслабване, и процент на пациентите, постигнали> 10% от изходното отслабване 1
- Загубата на тегло се определя като всяко намаляване на теглото от началото на проучването 1
- Средното изходно телесно тегло е 233,9 lb, а средният изходен ИТМ е 38,3 kg/m 2 1
Клинично значимо отслабване
По-голямата част от пациентите, лекувани със Saxenda ®, постигат и поддържат клинично значима загуба на тегло 1
разликата от плацебо е статистически значима. ITT-MI, намерение за лечение с множество импутации. 1
21-lb означава загуба на тегло
постигнато от пациенти на Saxenda ®, които са завършили проучването 2
- Средното изходно телесно тегло е 233,9 lb, а средният изходен ИТМ е 38,3 kg/m 2
Вторична крайна точка: Въздействие върху обиколката на талията
Голямата обиколка на талията е важен маркер за свързаните със затлъстяването рискове за здравето 3
Измерване на талията 3
Правилното измерване на обиколката е лесно да се научи и е важно да се знае
Saxenda ® намалява обиколката на талията с 3,2 инча срещу 1,6 инча при плацебо. 1
Средната обиколка на талията на изходно ниво е била 45,3 инча за пациенти, лекувани със Saxenda ® (n = 2,487) и 45,1 инча за пациенти, приемащи плацебо (n = 1 244) 1
Проучване 1 (едногодишно) 1,4
- Резултати от 56-седмично, рандомизирано, двойно-сляпо, плацебо контролирано проучване за оценка на безопасността и ефикасността на Saxenda ®
- Пациентите с ИТМ ≥30 или ≥27 с 1 или повече съпътстващи заболявания, свързани с теглото (N = 3,731), са рандомизирани да получават веднъж дневно Saxenda ® (n = 2,487) или плацебо (n = 1,244) във връзка с начина на живот програма за модификация, която включваше повишена физическа активност и диета с дефицит от 500 ккал/ден
- Пациентите претърпяха 4-седмичен период на повишаване на дозата, последван от 52 седмици с пълната доза
- Първичните крайни точки бяха средно процентно изменение на теглото, процент на пациентите, постигнали ≥5% от изходното отслабване, и процент на пациентите, постигнали> 10% от изходното отслабване на 56 седмици
- Вторичните крайни точки включват промени в обиколката на талията, кръвното налягане и липидите
- Средното изходно телесно тегло е 233,9 lb, а средният ИТМ е 38,3 kg/m 2
- Пациентите с диабет тип 2 бяха изключени от участие
Вижте пътя на Роберто за управление на теглото
Описание:
Станете свидетели на разговора между Роберто и неговия лекар, докато Роберто се бори да овладее теглото си. Когато Роберто повиши теглото си на лекаря си, той вече тренираше и се хранеше здравословно. Лекарят му знаеше, че трябва да има повече, за да помогне на Роберто да не тежи; точно тогава той препоръча Saxenda ® .
ПРЕПОРЪЧИТЕЛНО СЪДЪРЖАНИЕ
Устойчиво отслабване
Важна информация за безопасност при инжектиране на Saxenda ® (лираглутид) 3 mg
ПРЕДУПРЕЖДЕНИЕ: РИСК ОТ ТУМОРИ НА ЩИРОИДНИ КЛЕТКИ
Лираглутид причинява дозозависими и зависими от продължителността на лечението С-клетъчни тумори на щитовидната жлеза при клинично значими експозиции и при двата пола на плъхове и мишки. Не е известно дали Saxenda ® причинява С-клетъчни тумори на щитовидната жлеза, включително медуларен карцином на щитовидната жлеза (MTC), при хората, тъй като човешкото значение на индуцираните от лираглутид С-клетъчни тумори на щитовидната жлеза не е определено. Saxenda ® е противопоказан при пациенти с лична или фамилна анамнеза за MTC и при пациенти със синдром на множествена ендокринна неоплазия тип 2 (MEN 2). Консултирайте пациентите относно потенциалния риск от MTC с използването на Saxenda ® и ги информирайте за симптоми на тумори на щитовидната жлеза (напр. Маса в шията, дисфагия, диспнея, постоянна дрезгавост). Рутинното проследяване на серумния калцитонин или използване на ултразвук на щитовидната жлеза е с несигурна стойност за ранно откриване на MTC при пациенти, лекувани със Saxenda ® .
Показания и употреба
- Saxenda ® (лираглутид) инжекция 3 mg е показан като допълнение към диета с намалено съдържание на калории и повишена физическа активност за хронично управление на теглото при възрастни пациенти с начален индекс на телесна маса (ИТМ) 30 kg/m 2 или повече (затлъстяване) или 27 kg/m 2 или повече (наднормено тегло) при наличие на най-малко едно свързано с теглото коморбидно състояние (напр. хипертония, захарен диабет тип 2 или дислипидемия)
Ограничения на употребата
- Saxenda ® не е показан за лечение на диабет тип 2
- Saxenda ® и Victoza ® съдържат една и съща активна съставка, лираглутид, и поради това не трябва да се използват заедно. Saxenda ® не трябва да се използва в комбинация с други агонисти на GLP-1 рецептора
- Saxenda ® не е проучен при пациенти, приемащи инсулин. Saxenda ® и инсулин не трябва да се използват заедно
- Безопасността и ефикасността на Saxenda ® в комбинация с други продукти за отслабване, включително лекарства с рецепта, лекарства без рецепта и билкови препарати, не са установени
Важна информация за безопасност продължение.
Противопоказания
Saxenda ® е противопоказан при:
- Пациенти с лична или фамилна анамнеза за MTC или MEN 2
- Пациенти с предишна сериозна реакция на свръхчувствителност към лираглутид или към някоя от съставките на продукта
- Бременност
Предупреждения и предпазни мерки
- Риск от тироидни С-клетъчни тумори: Ако се измери серумен калцитонин и се установи, че е повишен, пациентът трябва да бъде допълнително оценен. Пациентите с възли на щитовидната жлеза, отбелязани при физикален преглед или образна диагностика на шията, също трябва да бъдат допълнително оценени
- Остър панкреатит: Остър панкреатит, включително фатален и нефатален хеморагичен или некротизиращ панкреатит, е наблюдаван при пациенти, лекувани с лираглутид в постмаркетинговия период. Наблюдавайте внимателно пациентите за признаци и симптоми на панкреатит (постоянна силна болка в корема, понякога ирадиираща към гърба със или без повръщане). Ако се подозира панкреатит, прекратете незабавно Saxenda ® и ако панкреатитът е потвърден, не рестартирайте
- Остра болест на жлъчния мехур: Значителната или бърза загуба на тегло може да увеличи риска от холелитиаза; обаче честотата на острата болест на жлъчния мехур е по-голяма при пациенти, лекувани със Saxenda ®, отколкото при плацебо, дори след като се отчете степента на загуба на тегло. При съмнение за холелитиаза са показани изследвания на жлъчния мехур и подходящо клинично проследяване
- Риск от хипогликемия при едновременна употреба на антидиабетна терапия: Когато Saxenda ® се използва с инсулинов секретагог (напр. Сулфонилурея), може да възникне сериозна хипогликемия. Помислете за намаляване на дозата на инсулиновия секретагог, за да намалите риска от хипогликемия. Наблюдавайте параметрите на кръвната захар преди започване на лечението със Saxenda ® и по време на лечението и коригирайте антидиабетните лекарства, ако е необходимо
- Повишаване на сърдечната честота: Средно увеличение на сърдечната честота в покой от 2 до 3 удара в минута (bpm) се наблюдава при пациенти, лекувани със Saxenda ®. Наблюдавайте сърдечната честота на редовни интервали и информирайте пациентите да съобщават за сърцебиене или усещане за учестено сърцебиене, докато са в покой по време на лечението със Saxenda ®. Прекратете Saxenda ® при пациенти, които изпитват трайно повишаване на сърдечната честота в покой
- Бъбречна недостатъчност: Съобщава се за остра бъбречна недостатъчност и влошаване на хронична бъбречна недостатъчност, която понякога може да изисква хемодиализа, обикновено във връзка с гадене, повръщане, диария или дехидратация. Внимавайте при започване или увеличаване на дози Saxenda ® при пациенти с бъбречно увреждане
- Реакции на свръхчувствителност: Съобщавани са сериозни реакции на свръхчувствителност (напр. Анафилаксия и ангиоедем) при пациенти, лекувани с лираглутид. Ако се появи реакция на свръхчувствителност, пациентите трябва да спрат приема на Saxenda ® и незабавно да потърсят медицинска помощ
- Самоубийствено поведение и идеи: В клинични проучвания 9 (0,3%) от 3 384 пациенти, лекувани със Saxenda ® и 2 (0,1%) от 1 941, лекувани с плацебо, съобщават за суицидни идеи; един от пациентите, лекувани със Saxenda ®, се е опитал да се самоубие. Наблюдавайте пациентите на Saxenda ® за възникване или влошаване на депресия, мисли за самоубийство или поведение и/или някакви необичайни промени в настроението или поведението. Преустановете лечението, ако пациентите изпитват мисли или поведение за самоубийство. Избягвайте Saxenda ® при пациенти с анамнеза за опити за самоубийство или активни мисли за самоубийство
Неблагоприятни събития
- Най-честите нежелани реакции, съобщени при ≥5%, са: гадене, хипогликемия, диария, запек, повръщане, главоболие, намален апетит, диспепсия, умора, световъртеж, коремна болка и повишена липаза
Лекарствени взаимодействия
- Saxenda ® причинява забавяне на изпразването на стомаха и има потенциал да повлияе абсорбцията на едновременно прилагани перорални лекарства. Следете за потенциални последици от забавената абсорбция на перорални лекарства, едновременно прилагани със Saxenda ®
Използване при специфични популации
- Няма данни за наличието на лираглутид в кърмата при хора; лираглутид присъства в млякото на лактиращи плъхове
- Saxenda ® не е проучен при пациенти под 18-годишна възраст и не се препоръчва за употреба при педиатрични пациенти
- Saxenda ® забавя изпразването на стомаха. Saxenda ® не е проучен при пациенти със съществуваща гастропареза
Моля, кликнете тук за информация за предписване на Saxenda ®, включително предупреждение в кутия.
- Нова снимка за отслабване Saxenda (лираглутид) Колко добре работи CBS News
- Лекарството за псориазис може също да помогне за отслабване - клиничен съветник
- Нашата най-добра диета за отслабване за почистване за еднодневни резултати
- Малки съвети за големи резултати при отслабване
- Феновете на Настя Каменских развълнувани от резултатите отслабване; Имате нужда поне от малко там; Бобр