Триптофанът е аминокиселина, необходима на всички форми на живот за протеинов синтез и други важни метаболитни функции (Moffett и Namboodiri, 2003) и отчита основния флуорофор, допринасящ за протеините в тъканите.
Свързани термини:
- Аминокиселина
- Ензим
- Пептид
- Протеин
- Тирозин
- Фенилаланин
- Серотонин
- Индолеамин 2,3 диоксигеназа
Изтеглете като PDF
За тази страница
Триптофан
Главна информация
Триптофанът е естествена есенциална аминокиселина, която се препоръчва като безвредна здравословна храна за лечение на депресия, безсъние, стрес, поведенчески разстройства и предменструален синдром. Наличието на аминокиселини в магазините за здравословни храни и съвременният интерес към природните лекарства доведоха до широко разпространено използване на триптофан за лечение на депресия. През 1976 г. се изчислява, че до този момент са проучени няколкостотин пациенти с афективни разстройства, като резултатите са докладвани в поне 21 статии [1]. Въпреки това, резултатите от клиничните изпитвания с l-триптофан при лечението на депресивни разстройства са противоречиви [2, 3].
Предполага се, че може да има известна полза от използването на триптофан при избрани пациенти, особено тези с психомоторна изостаналост [4]. За съжаление повечето от тези доклади се появяват като писма до редакторите на списания [5–7] или като предварителни съобщения [8]. В допълнение към възможното отсъствие на някакъв последователен ефект, има много правдоподобни причини да се обясни променливостта в отговор. Триптофанът е даван както в рацемична, така и в мономерна (левовъртяща се) форма, както самостоятелно, така и заедно с редица вещества, предназначени да повишат синтеза или наличността на серотонин, включително инхибитори на моноаминооксидазата (МАО) [9], калиеви или въглехидратни добавки [ 10] и ко-ензими като пиридоксин или аскорбинова киселина [11]. Предполага се също, че плазмените концентрации на триптофан имат терапевтичен прозорец [5] и че многократното приложение предизвиква чернодробна триптофан пиролаза, което води до понижени плазмени концентрации и загуба на терапевтичен ефект след 2 седмици лечение [9]. Правени са опити за подобряване на този проблем чрез едновременно приложение на никотинамид [5].
В допълнение към затрудненото тълкуване на възможните ползи, дължащи се на триптофан, има и малко информация за нежелани реакции. Това отчасти може да се обясни с предполагаемата безопасност на природно вещество, но за това допринася и предварителният характер на много комуникации. В поне две проучвания [6, 8], при които триптофанът е сравнен с трицикличен антидепресант, умишлено се избягва разследване за нежелани реакции, за да се защити двойно-сляпата цялост на изследването. Две проучвания съобщават за липсата на последователни или категорични промени в хематологичните стойности, серумните електролити, плазмените протеини или тестовете за чернодробна функция след 4 седмици лечение с 1-триптофан до 8 g/ден [8, 11]. Съобщава се за гадене в началото на лечението [12], замайване, което изглежда не е свързано с постурална хипотония [13] и влошаване на психичното състояние [14, 15]. Съобщава се за хипомания при комбиниране на триптофан с МАО инхибитор [15] и нежелани реакции, включително мускулен тремор, хипоманично настроение, хиперрефлексия и двустранни признаци на Бабински, са наблюдавани при пациент, приемащ фенелзин и триптофан.
Въпреки че L-триптофанът е оттеглен в много страни, през 1994 г. той отново се предлага във Великобритания за комбинирано лечение на пациенти с дългогодишна рефрактерна депресия, при стриктно условие, че трябва да се предписва само от болнични специалисти за пациенти с дългогодишни устойчива депресия [16]. Той все още се използва и в други страни, като Германия и Канада, но не и в САЩ.
Триптофан
Мартин Колмайер, в Хранителен метаболизъм, 2003
Транспорт и клетъчно усвояване
Кръвообращение: Плазмената концентрация на Trp (обикновено около 50 μmol/l) намалява в отговор на ниския хранителен прием (Kaye et al., 2000). Поглъщането от кръвта използва различни транспортери, включително система T (TAT1), LAT1 и LAT2, чиито модели на експресия варират значително в различните тъкани.
Кръвно-мозъчна бариера: Независимият от натрий транспортер TAT1 и закрепеният с гликопротеин комплекс LAT1 се експресират в мозъчните капилярни ендотелни клетки и със сигурност допринасят за транспортирането на Trp, но тяхното относително значение, местоположение и ролята на другите транспортери не е напълно изяснено. Trp се конкурира с аминокиселините с разклонена верига (валин, левцин, изолевцин) и други големи неутрални аминокиселини (метионин, тирозин, триптофан и хистидин) за транспорта в мозъка. Това може да означава, че повишените концентрации на фенилаланин в кръвта (особено при пациенти с фенилкетонурия, вродена грешка в метаболизма с дефектно използване на фенилаланин) или аминокиселини с разклонена верига (поради диета с високо съдържание на въглехидрати) ограничават наличието на Trp в мозъка.
Матерно-фетален трансфер: Обменникът LAT1 изглежда е основният път за Trp, пътуващ от майчината кръв в синцитиотрофобласта (Ritchie and Taylor, 2001). Трансферът през базолатералната мембрана може да продължи предимно чрез LAT1 и LAT2 (Ritchie and Taylor, 2001); принос от TAT1, който е силно изразен в плацентата (Kim et al., 2001), е оспорен (Ritchie and Taylor, 2001).
Развиваемост в биофизичната характеристика
17.4.2.4 Окисляване на триптофан
Триптофанът е друг остатък, който може да бъде повлиян от окисляването на неговата група на страничната верига. За разлика от метионина има много различни модифицирани атомни структури на страничната верига на триптофана след окисляване [51,56]. Подобно на окислението на метионин, окислението на триптофан може да се ускори с излагане на светлина. Също така, подобно на окислението на метионин, пептидното картографиране е основният метод за наблюдение. Хидрофобната взаимодействаща хроматография (HIC) може също да се използва за наблюдение на окислението на триптофан, тъй като окисляването на триптофани в CDR често променя потенциала на свързване към HIC колони. HIC може да бъде с по-висока производителност и да консумира по-малко проба от пептидното картографиране; обаче може да се наложи широко развитие на метода.
Спете
Неблагоприятни ефекти
Триптофанът обикновено се понася добре, въпреки че някои пациенти могат да проявят дневна сънливост, световъртеж и сухота в устата. При по-високи дози могат да станат очевидни допълнителни проблеми с гадене, липса на апетит и главоболие (Medical Economics, 2007). Тъй като триптофанът е успокоително, трябва да се избягва едновременната употреба на други съединения, които оказват подобни ефекти (например алкохол).
Триптофанът е свързан с малък риск от сърдечни дисфункции. Тъй като триптофанът се превръща в серотонин в мозъка, както и периферно, повишаването на серотонина може да стане очевидно в тъканите и мускулите, включително сърцето. Поради тази причина някои препоръчват добавките с триптофан да се приемат само с карбидопа, която блокира превръщането на триптофана в серотонин, докато не премине кръвно-мозъчната бариера (Xu et al., 2002).
Триптофанът трябва да се използва внимателно при пациенти, които са диагностицирани с диабет или имат фамилна анамнеза за диабет. Установено е, че един от метаболитите на триптофана, ксантуреновата киселина, има диабетогенен ефект при животните. Въпреки че не са докладвани случаи при хора, трябва да се внимава.
Аминокиселини: Метаболизъм
Триптофан
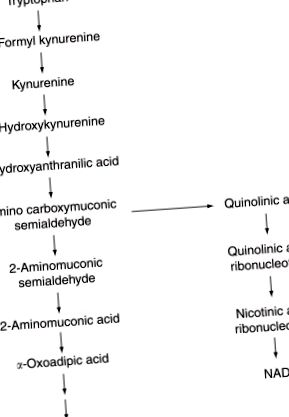
Триптофанът се окислява от хормоночувствителния ензим триптофан оксигеназа до N-формил кинуренинин, който след това следва серия от стъпки за получаване на амино-карбоксимуконов полуалдехид. Повечето от тях се подлагат на ензимно декарбоксилиране, което в крайна сметка води до ацетил КоА. Въпреки това, малка част се подлага на неензимна циклизация до хинолова киселина, което води до образуването на NAD. Ето защо излишният диетичен триптофан може да отговори на изискванията за витамин ниацин (вж. Фигура 9).
Фигура 9. Метаболизъм на триптофан.
Една от стъпките в катаболизма на триптофана се катализира от витамин В6-зависимия ензим кинурениназа. Ако състоянието на витамин В6 е неадекватно и се прилага голяма доза триптофан, голяма част от триптофана ще се метаболизира по алтернативен път на кинуреновата и ксантурена киселини, които ще се екскретират с урината. Това е основата на теста за натоварване с триптофан за състояние на витамин В6.
Малко количество триптофан се подлага на хидроксилиране до 5-хидрокситриптофан, който след това се декарбоксилира до физиологично активния амин 5-хидрокситриптамин (серотонин).
Вещества, участващи в невротрансмисията
Триптофан
Триптофанът също е една от 20-те стандартни аминокиселини, присъстващи в организма и използвани от клетките за синтезиране на протеини. Това е незаменима аминокиселина, което означава, че тя се приема само от диетата. Триптофанът се съдържа в голямо разнообразие от храни, съдържащи протеини, включително яйца, сирене, месо (особено пуйка), риба, пшеница, ориз, картофи и банани. Тъй като триптофанът трябва да се поглъща с храна, СЗО е определила типичен препоръчителен дневен прием за триптофан на 4 mg/kg телесно тегло (WHO, 2007).
При поглъщане на храна, която съдържа триптофан, молекулата се извлича по време на метаболитните процеси, протичащи в тънките черва, и се абсорбира в циркулацията. Там той пътува през тялото, пресича кръвно-мозъчната бариера и навлиза в невроните, където се метаболизира в индоламинови невротрансмитери, както и ниацин. Тъй като тялото не произвежда триптофан, той има ограничени способности да регулира количеството триптофан в клетките. Когато се погълне твърде много триптофан, той се разгражда чрез различни метаболитни процеси и понякога може да бъде реконвертиран, ако е необходимо. Въпреки това, когато се приемат ограничени количества, може да се прояви дефицит на триптофан, което води до потиснати количества серотонин, мелатонин, ниацин и други важни молекули. Депресията и нарушенията на съня могат частично да бъдат причинени от ограничени количества триптофан в организма.
Поради тази причина се прави опит за добавяне с триптофан и е бил популярен до края на 80-те години, когато над 30 смъртни случая са причинени от замърсени партиди триптофан. След това добавката беше забранена в Съединените щати (и много други страни), но напоследък беше разкрито, че проблемите в производството са отговорни за тези смъртни случаи и добавката е потенциално безопасна. Следователно продажбите на триптофан като добавка бяха възобновени през 2001 г., а забраната на FDA за внос на триптофан добавки беше отменена през 2005 г.
Клиницистите се съветват внимателно да обмислят дали е показана добавка с триптофан. Първо, трябва да се спазват препоръките на СЗО относно хранителния прием. В случаите, когато е очевидно, че диетичният прием пада значително под препоръчителните нива, може да се опита добавка. В противен случай добавката с триптофан може да бъде полезна при справяне с проблемите със съня (както е обсъдено в глава 9), а добавката с 5-HTP, трансформирана форма на триптофан, може да бъде ефективна при лечение на симптоми на депресия (обсъдена в глава 6) и тревожност ( обхванати в глава 8).
АМИНО КИСЕЛИНИ | Решителност
Триптофан
Триптофанът също присъства в ниски концентрации и значително се разгражда по време на киселинна хидролиза. Няма обаче измерим краен продукт и затова е нормално да се използва алкална хидролиза специално за анализ на триптофан. Натриевите, бариевите или литиевите хидроксиди могат да се използват при концентрации от 4 до 6 М, като често се препоръчват добавки като малтодекстрин, нишесте или тиодигикол за намаляване на загубите на триптофан. Хидролизата може да бъде в продължение на 8 часа при 145 ° C или 20 часа при 110 ° C, като се използват полипропиленови съдове. В идеалния случай триптофанът трябва да бъде отделен от интерфериращи съединения, например лизиноаланин (LAL) чрез IEC или RPC. Последното отнема само няколко минути и дериватизацията на предколона е ненужна, тъй като триптофанът може да бъде открит от неговата естествена флуоресценция.
Триптофанът също е оценен чрез киселинна хидролиза на непокътнати протеини в присъствието на нинхидрин, с който той реагира, преди да може да се разгради. Трябва да се направят корекции за тирозин.
Валериан и други CAM ботанически препарати при лечение на нарушения на съня
l -триптофан и 5-HTP
л - триптофанът е основна аминокиселина, която може да се приема като добавка или да се консумира в хранителни протеини както от животински, така и от растителни източници. l -триптофанът и неговият метаболит 5-хидрокситриптофан (5-HTP), непосредственият предшественик на серотонина, се използват за подобряване на съня, тъй като се знае, че серотонинът има множество функции в регулирането на състоянията на събуждане и сън [128]. Тъй като серотонинът е предшественик на мелатонина, насърчаването на съня чрез приложение на l -триптофан може също да е резултат от повишените нива на мелатонин. Докато превръщането на 1 -триптофан в серотонин е ограничено от наличието на метаболизиращия ензим триптофан хидроксилаза и протеинови транспортери, които се споделят с други аминокиселини, преобразуването на 5-HTP не е ограничено от тези фактори и може да бъде по-ефективно превърнато в серотонин [ 129], въпреки че са необходими повече изследвания за клиничните ефекти на тази разлика.
Ранните проучвания върху l-триптофан обикновено използват малки проби и дават смесени резултати. Някои изследвания показват, че добавките с l -триптофан или 5-HTP намаляват латентността на съня [129]. Освен това, някои доказателства сочат, че консумацията на храни, богати на l -триптофан, заедно с въглехидрати (което насърчава усвояването на l -триптофан) също намалява латентността на съня [130], а CBT стратегиите включват лека закуска преди лягане с храни с високо съдържание на тази аминокиселина. След появата на епидемия от 1989 г. на животозастрашаващото състояние синдром на еозинофилия-миалгия (EMS), свързан с l-триптофан, изследванията върху l-триптофан за сън прекратяват и едва наскоро изследователите започват да изучават неговите ефекти върху съня. Един двойно-сляп, плацебо контролиран RCT показа подобрение в самоотчетеното общо време за сън, ефективност на съня, общо време за събуждане и качество на съня както с фармацевтичен клас l-триптофан, така и със специално формулирани l-триптофан/въглехидратни хранителни барове [131]. Друго проучване показва, че REM потискането на съня, причинено от използването на антидепресант, инхибиращ обратното поемане на серотонина, е обърнато от едновременното добавяне на l-триптофан [132]. Понастоящем не съществуват достатъчно доказателства за определяне на клиничната ефикасност на l -триптофан и 5-HTP за нарушение на съня.
Загрижеността за безопасността по отношение на l-триптофана беше повдигната през 1989 г. след епидемия от EMS, която доведе до поне 37 съобщени смъртни случая [133]. В повечето случаи EMS е свързан със замърсен продукт от Япония, но индивидуалната чувствителност не може да бъде изключена като допринасящ фактор. Американската администрация по храните и лекарствата (FDA) издаде съвет и забрани продажбата на повечето продукти от триптофан. Едва наскоро търговията с l-триптофан отново е разрешена в Съединените щати, но остава в сила препоръка и остават ограничения за вносни продукти с l-триптофан [133]. Освен редкия, но сериозен риск от EMS, добавките l-триптофан и 5-HTP имат малко съобщени странични ефекти и не са свързани с остатъчна седация. Гаденето е често срещан страничен ефект на дозите на l-триптофан над 5 mg [103]. Въпреки че някои доказателства сочат, че едновременната употреба на прекурсори на серотонин (l-триптофан или 5-HTP) с антидепресанти може да бъде от полза, подобна употреба трябва да се избягва до повече е известно за потенциални взаимодействия на продукта поради риск от серотонинов синдром, опасно състояние, свързано с хипертермия, хиперрефлексия и риск от смърт.
Аминокиселини и протеини
Кристин Л. Уршел, Лори М. Лорънс, в Приложно и клинично хранене на коне, 2013
Триптофан
Триптофанът е включен като съставка в много успокояващи добавки (
13 mg/kg) и изложени на стимули, създадени да предизвикат реакция на страх, добавените с триптофан коне не показват никакви разлики в нито една от поведенческите мерки за страх или в параметрите на сърдечната честота в сравнение с нелекуваните коне, въпреки повишения циркулиращ триптофан (Malmkvist & Christensen 2007, Noble et al 2008). Понастоящем няма изследвания в подкрепа на използването на търговски успокояващи добавки с триптофан като основна активна съставка.
Синдром на еозинофилия – миалгия
Разпространение и причини за употребата на l- триптофан
l - Употребата на триптофан е широко разпространена в Съединените щати през 1989 г. В Орегон и Минесота приблизително 2% от анкетираните членове на домакинствата са използвали триптофан по някое време между 1980 и 1989 г. Най-честите причини за употребата на триптофан са безсъние, предменструален синдром и депресия; други причини включват тревожност, главоболие, поведенчески разстройства, затлъстяване и спиране на тютюнопушенето. Въпреки че повечето потребители купуват триптофан за терапевтична употреба, той се предлага на пазара като хранителна добавка и се предлага широко в Съединените щати без рецепта. Този продукт не е одобрен или регулиран от FDA.
l- Триптофанът е основна аминокиселина; достатъчно количество обаче присъстват в диетата на повечето северноамериканци, без да са необходими добавки. Типичната дневна диета за САЩ съдържа 1–3 g триптофан, който задоволява препоръчителната дневна доза от 3 mg kg -1 телесно тегло (или 210 mg (70 kg) -1 човек). Той се метаболизира до серотонин и следователно теоретично може да има седативни и антидепресантни свойства.
- Volar Plate - общ преглед на ScienceDirect теми
- Уилоу - общ преглед на ScienceDirect теми
- Токсокароза - общ преглед на ScienceDirect теми
- Зонова диета - общ преглед на ScienceDirect теми
- Терпентин - общ преглед на ScienceDirect теми