Жорж Раад
1 клиника Azoury-IVF, болница Mount Libanon, 5-ти етаж, бул. Camille Chamoun, Бейрут, Ливан
3 Université Cote d’Azur, Inserm, C3M (отбор 10), Ница, Франция
Мира Хазури
2 Факултет на науките 2, Ливански университет, Фанар, Ливан
Силвия Ботини
3 Université Cote d’Azur, Inserm, C3M (отбор 10), Ница, Франция
Микеле Трабуки
3 Université Cote d’Azur, Inserm, C3M (отбор 10), Ница, Франция
Джоузеф Азури
1 клиника Azoury-IVF, болница Mount Libanon, 5-ти етаж, бул. Camille Chamoun, Бейрут, Ливан
Валери Гранджиан
3 Université Cote d’Azur, Inserm, C3M (отбор 10), Ница, Франция
Свързани данни
Резюме
Продължи
Заден план
Сперматогенезата е строго регулиран процес, позволяващ производството на високоспециализирани клетки, сперматозоидите. За да се породи жизнеспособно потомство, сперматозоидите се нуждаят от две основни свойства: докато първото е да оплоди яйцеклетките, за да се получи диплоидна клетка, зиготата, втората е да доведе до зиготата половината от нейните генетични и епигенетични компоненти. Следователно можем да предположим, че фактори, които променят цялата физиология на индивида, могат да имат отрицателно въздействие върху качеството на спермата му, например случаят на затлъстяване.
маса 1
Таблица, показваща класификацията на наднорменото тегло и затлъстяването [147].
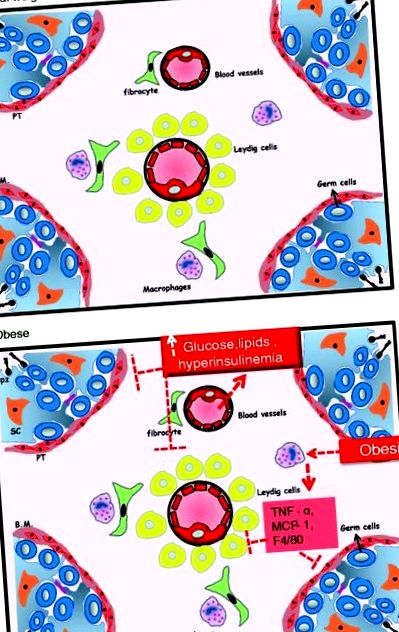
| Поднормено тегло | 6 Leydig клетки на тестис), имунни клетки, кръвоносни съдове, фибробласти и съединителна тъкан, а основната му функция е производството на мъжки полови хормони. Целостта на двете отделения е от решаващо значение за диференциацията на мъжките гамети (фиг. 1) [46]. |
Илюстрация на тестикуларна интерстициална тъкан при мъже с нормално тегло (а) и затлъстели мъже (б). Spz = сперматозоиди; sc = клетки на Сертоли; PT = перитубуларни клетки; Б.М. = базална мембрана. TNF-алфа: Туморен фактор некроза алфа; MCP-1 = моноцитен хемоаттрактант протеин-1; F4/80: определящ маркер на популациите от миши макрофаги
Ефект на затлъстяването върху клетъчната физиология на Leydig и андрогенната хомеостаза
За първи път описани през 1850 г. от Франц Лейдиг, клетките на Лейдиг чрез стероидогенеза секретират най-важния мъжки стероиден хормон, наречен тестостерон. Тези клетки могат лесно да достигнат до кръвоносните съдове, което позволява усвояването на лутеинизиращия хормон (LH) и холестерола от кръвообращението, за да се произведе тестостерон. Произведеният мъжки полов хормон се дифузира в интерстициалния и тръбния отдел, за да регулира сперматогенезата. Освен това, когато тестостеронът се освободи в кръвния поток, той играе различни роли в маскулинизацията на мозъка и сексуалното поведение, модулацията на растежа на ларинкса, стимулирането на синтеза на еритропоетин в бъбреците, узряването на мъжките полови органи, растежа на косата, регулирането на мускулната маса на костите и синтез на протеини в черния дроб [47].
Схематично представяне на оста на тестисите на хипоталамусната хипофиза и производството на хормони на тестисите при затлъстяване. Плътните линии представляват хормоналната регулация при мъжете с нормално тегло; пунктирани линии представляват инхибиращите ефекти на затлъстяването. AMH: анти-мюлериен хормон; ABP: андроген свързващ протеин; Е2: естроген; FSH: фоликулостимулиращ хормон; GnRH: гонадотропин освобождаващ хормон; LH: лутеинизиращ хормон; LHR: рецептор за лутеинизиращ хормон; SHBG: глобулин, свързващ половите хормони; STAR: стероидогенен остър регулаторен протеин
Ефект на затлъстяването върху функциите на клетките на Сертоли
Клетките на Сертоли играят решаваща роля в развитието на зародишните клетки, както и в регулирането на сперматогенезата. Тези клетки получават хормонални съобщения (FSH и тестостерон) и местни сигнали (автокринни и паракринни), за да секретират молекули, модулиращи собствената им функция, както и тази на зародишните клетки и клетките на Leydig [47].
Важно е да се отбележи, че бариерата на кръвните тестиси (BTB) може да модулира до известна степен усвояването на глюкоза и липиди в зависимост от тяхната наличност в кръвта [62]. Въпреки това, хистологичният анализ на тестисите от мишки на диета с високо съдържание на мазнини показа, че затлъстяването може да наруши целостта на BTB [65]. В същата перспектива затлъстяването може да заобиколи адаптивните механизми на BTB към променящите се условия на околната среда и по този начин да насочи основните си функции в селективен транспорт и пропускливост [62].
Ефект на затлъстяването върху сперматогонията
Сперматагониите са крайните зародишни стволови клетки, издигащи се от първичните зародишни клетки (PGC). Те се характеризират с капацитет за самообновяване и ангажираността им към сперматогенезата. Затлъстяването при мъжете също може да наруши оцеляването и диференциацията на тези клетки [66]. От особен интерес Интерлевкин 6 (IL-6) е цитокин, секретиран от мастна тъкан и макрофаги. При повишени концентрации предизвиква възпалителен отговор. Неотдавнашно проучване показа, че се установява високо ниво на IL-6 в серума и тестисите на затлъстели мишки. Можем да предположим, че това покачване може да намали нивото на протеин от цинков пръст (Zfp637) в сперматогонията. Намаляването на регулацията на Zfp637 намалява сперматогониалната диференциация [67]. Освен това затлъстяването може да предизвика тестикуларна хипертермия. Установено е, че специфичните сперматогонии (Adark) са по-уязвими на топлинен стрес поради високата им митотична активност [68, 69]. Като цяло тези данни подчертават отрицателното въздействие на затлъстяването върху оцеляването и диференциацията на сперматогонията.
Влияние на затлъстяването по бащина линия върху параметрите на спермата и развитието на ембриона
Бащинското затлъстяване влияе негативно на параметрите на спермата
Бяха проведени много систематични прегледи при хора, за да се оценят ефектите от мъжкото затлъстяване върху параметрите на сперматозоидите, фрагментацията на ДНК, потенциала на митохондриалната мембрана и резултатите за плодовитостта [11, 18, 70–72]. Въпреки че бяха забелязани някои несъответствия [11, 18], като цяло тези проучвания показват, че наднорменото тегло и затлъстяването при мъжете са свързани с висока честота на олигозооспермия и азооспермия [73–75], намаляване на процента на нормална морфология на сперматозоидите [11, 18], повишен процент на сперматозоидите с фрагментация на ДНК и анормален митохондриален мембранен потенциал [11, 75, 76].
Установено е, че някои от тези усложнения са свързани с оксидативен стрес на тестисите [77]. Всъщност сперматогенезата е свързана с висока скорост на консумация на кислород и произтичащата от това важна продукция на ROS от митохондриите, причиняваща оксидативен стрес [78]. Хипергликемията и хиперлипидемията биха влошили този резултат. Всъщност вътреклетъчното натрупване на липиди увеличава степента на β-окисление на мастните киселини. Когато са претоварени, стресираните тестикуларни митохондрии намаляват производството на АТФ и предизвикват свръхпродукция на ROS [56]. Нещо повече, високоенергийните диети биха намалили тестикуларната антиоксидантна система чрез намаляване на експресията на ROS-детоксикиращи ензими в тестисите като активирания от пролифератори γ коактиватор 1α (PGC-1α) и сиртуин 3 (SIRT3) [79]. Не е изненадващо, че проучвания при хора и гризачи показват, че затлъстяването е свързано с повишено производство на ROS на сперматозоидите [80, 81]. Високата ROS може да доведе до важни разрушителни ефекти в тъканите, причинявайки промени в мембраните, причинявайки необратими клетъчни увреждания. От друга страна, повишените нива на ROS могат да предизвикат увреждане на ДНК в сперматидите [81] и в зрелите сперматозоиди [82–86]. Като цяло тези открития разкриват, че затлъстяването предизвиква оксидативен стрес в тестисите и по този начин влошава качеството на сперматозоидите [56].
Затлъстяване по бащина линия и развитие на ембриона
Беше демонстрирано, че затлъстяването при гризачи има отрицателно въздействие върху развитието на ембриона преди имплантацията, по-специално ние посочихме по-висок процент на едноклетъчен ембрионален блок, забавено прогресиране на клетъчния цикъл, намален брой на бластоцистите и променен метаболизъм на въглехидратите [87, 88] . По отношение на развитието на човешки ин витро ембриони бяха публикувани много малко доклади. Докато две проучвания не откриха значителна разлика между мъже със затлъстяване и мъже с наднормено тегло по отношение на ембриологичните параметри, Bakos et al. забеляза значително намаляване на скоростта на бластулацията с увеличаване на ИТМ [84, 89, 90]. Поразително е, че неотдавнашен метаанализ, включващ 115 158 участници, показа, че затлъстяването по бащина линия може да намали равнището на живо раждане за цикъл на асистирана репродуктивна технология (ART) и увеличава с 10% риска от изправяне пред нежизнеспособна бременност [11]. Тези открития подчертават отрицателното въздействие на затлъстяването върху ембрионалното развитие.
Затлъстяване по бащина линия и последици върху метаболитното здравословно потомство
Възможни механизми за наследяване между поколенията и поколенията на бащинско затлъстяване
Модификации, за които е известно, че са част от епигенома, а именно метилиране на ДНК, хроматинова структура и некодираща РНК могат да участват в молекулярния механизъм на този процес [114].
ДНК метилиране и епигенетично наследяване
Докато тези проучвания показват, че променен подпис на ДНК метилиране на сперматозоиди от мъже с HFD може да бъде предаден през потомците [104], скорошно проучване показва, че метиломът на спермата се формира от генетични и епигенетични вариации, но не от диета [123].
Структура на хроматина и епигенетично наследство
Като цяло, тези открития ясно показват, че сперматозоидният хроматин може да бъде модулиран от диетичните условия и може да предава епигенетична информация на потомството.
РНК на спермата и епигенетична модификация
Както е описано по-горе, спермата е транскрипционно неактивна клетка, за която отдавна се смята, че е лишена от РНК. Въпреки това, няколко популации на РНК, включително малки некодиращи РНК като микроРНК (miRNAs), ендогенни малки интерфериращи РНК (ендо-siRNAs), Piwi-взаимодействащи РНК (piRNAs), бяха открити наскоро в сперматозоидите [137]. След откриването им няколко проучвания демонстрират своята роля както в ранната ембриогенеза, така и в епигенетичното наследяване [138, 139]. Например, използвайки експерименти за инжектиране на интра цитоплазмени сперматозоиди, Lui et al. установи, че сперматозоидите с частичен дефицит на миРНК и ендозиРНК, които се пренасят сперма, могат успешно да оплодят. Въпреки това, ембрионите, получени от тези сперматозоиди, показват различни ембрионални промени [139]. От друга страна, сперматозоидите microRNA-34c се откриват само в сперматозоиди и зиготи, но не и в ооцити. Доказано е, че е важно за синтеза на ДНК на едноклетъчен ембрион и първото разделяне на разцепването [138]. Като цяло тези данни демонстрират потенциалната роля на малката РНК в ембрионалния растеж.
Преди няколко години предоставихме първите доказателства, че малки некодиращи РНК молекули (sncRNAs) действат като трансгенерационни вектори на епигенетична информация при мишки. Всъщност ние демонстрирахме, че микроинжектирането на специфична микроРНК в един клетъчен ембрион предизвиква стабилни епигенетични модификации, водещи до специфични и наследствени фенотипове. По този начин сърдечната хипертрофия, анормалният растеж на възрастен и депигментацията на козината могат да бъдат предизвикани от микроинжектирането в мишки, оплодени яйцеклетки на miR-1, miR-124 и miR-221, съответно. Важното е, че всички тези фенотипове могат да се поддържат поне 2 последователни поколения [140–142].
Потенциална обратимост на новосъздадените епигенетични модификации
Предимството на епигенетичните промени пред генетичните мутации е тяхната потенциална обратимост [144]. Въз основа на това свойство редица скорошни експериментални проучвания целят да демонстрират обратимостта на новите епигенетични модификации, предизвикани от околната среда. По този начин не само метаболитните патологии, но и психиатричните разстройства могат да бъдат епигенетично наследени чрез бащата, изглежда, че те са частично предотвратени чрез диета/упражнения/намеса в околната среда при бащите [112] [143, 145, 146]. Тези проучвания обаче са извършени в експериментални модели на гризачи и има силна необходимост от разширяване на изследванията върху данните, базирани на популацията, за да се подобрят стратегиите за превенция. Към днешна дата само изследването на Barrès повдига този въпрос [13]. При хора със затлъстяване и наднормено тегло първо беше демонстрирано, че стресът от околната среда, като затлъстяването, може да предизвика епигенетични промени в човешките сперматозоиди. По-специално те показаха, че метилирането на ДНК на сперматозоидите и профилите на РНК са различни при затлъстелите и слабите мъже. Нещо повече, те забелязаха значителна дерегулация на експресията на piRNA. Нещо повече, те показаха при специфична кохорта от затлъстели мъже преди и след индуцирана от операцията загуба на тегло промяна в метилома на сперматозоидите. Това предполага обратимост на нововъзникналите от диетата епигенетични модификации, предизвикани от диетата.
Заключения
Има все повече доказателства в подкрепа на това, че затлъстяването влияе отрицателно върху качеството на спермата. Установено е, че промените на епигеном и малки некодиращи РНК при сперматозоиди при затлъстели индивиди оказват значително въздействие върху мъжкия потенциал за плодовитост и здравето на потомството. Поради обратимостта на такива промени, пациентите със затлъстяване често се насърчават да отслабнат, преди да им бъде препоръчана медицинска процедура. Въпреки това, може да се повдигнат някои съмнения относно предположението, че балансираната диета може напълно или частично да обърне епигенетичните и малки некодиращи промени на РНК.
Благодарности
Финансиране
G.R. беше подкрепен от стипендия от CNRS-L. Тази работа беше подкрепена от безвъзмездни средства на „Agence Nationale de la Recherche“ (ANR-12-ADAPT-0022) за VG, Fond Français pour l’Alimentation et la Santé (12-A-52), Франция за VG; ANR чрез „Инвестиции за бъдещето“ # ANR-11-LABX-0028-01 (LABEX SIGNALIFE) до MT.
Наличност на данни и материали
Съкращения
| 8-OHdG | 8-хидроксидезоксигуанозин |
| ABP | Андроген свързващ протеин |
| ADP | Аденозин монофосфат |
| AMH | Анти-мюлериен хормон |
| ИЗКУСТВО | Асистирана репродуктивна технология |
| ATP | Аденозин трифосфат |
| ИТМ | Индекс на телесна маса |
| BTB | Бариера за кръвен тестис |
| Casp12 | Каспаза-12 |
| Е2 | Естроген |
| Eftud1 | Фактор на удължаване като GTPase 1 |
| FSH | Фоликулостимулиращ хормон |
| GnRH | Гонадотропин освобождаващ хормон |
| H3K4me3 | Триметилиране (me3) на лизин 4 (K4) върху хистон Н3 |
| H3K56 | Лизин 56 на хистона 3 |
| H3K9 | Лизин 9 на хистона 3 |
| H3K9ac | Ацетилиране на лизин 9 (К9) върху хистон Н3 |
| H4K27me3 | Триметилиране (me3) на лизин 27 (K27) върху хистон Н3 |
| HDAC | Хистонови деацетилази |
| HFD | Диета с високо съдържание на мазнини |
| Il3ra2 | Рецепторът за интерлевкин 13 представя алфа 2 |
| IL-6 | Интерлевкин 6 |
| LH | лутеинизиращ хормон |
| m 2 G = N 2 - | метилгуанозин |
| m 5 C = 5- | метилцитозин |
| Маоа | Моноаминоксидаза |
| MDA | Малондиалдехид |
| miRNA | микроРНК |
| НХАН | Национално проучване за здравни и хранителни изследвания |
| НЕ | Азотен оксид |
| PGC-1α | Пролифераторите активират рецептор γ коактиватор 1α |
| PiIK3r1 | Регулаторна субединица на фосфатидилинозитол 3 киназа |
| PiK3ca | Каталитична субединица на фосфатидилинозитол 3 киназа |
| пиРНК | Взаимодействащи РНК на Piwi |
| Ppar | Пероксизомен пролифератор, активиран рецепторен алфам |
| PUFA | Полиненаситени мастни киселини |
| РНК | Messenger рибонуклеинова киселина |
| ROS | Реактивни кислородни видове |
| SGA | Малка за гестационна възраст |
| SHBG | Глобулин, свързващ половите хормони |
| SHBG | Глобулин, свързващ половите хормони |
| siRNAs | Малки интерфериращи РНК |
| SIRT | Сиртуин протеин |
| sncRNAs | Малка некодираща РНК |
| T2DM | захарен диабет тип 2 |
| тРНК | Прехвърлете рибонуклеинова киселина |
| tsRNA | тРНК-получени малки РНК |
| СЗО | Световна здравна асоциация |
| Zfp | Цинков пръстен протеин |
Принос на авторите
GR и VG са написали ръкописа. MH, MT, SB и JA са участвали в критичното редактиране на ръкописа. Всички автори прочетоха и одобриха окончателния ръкопис.
Бележки
Етично одобрение и съгласие за участие
Конкуриращи се интереси
Авторите заявяват, че нямат конкуриращи се интереси.
Бележка на издателя
Springer Nature остава неутрален по отношение на юрисдикционните претенции в публикувани карти и институционални принадлежности.
- Лошата диета може да повлияе на качеството на спермата на мъжете и на цялостното здраве
- Наднорменото тегло и затлъстяването са свързани с ниско качество на спермата
- Преодоляване на затлъстяването при по-възрастни кучета Качество на кучетата
- Доклад Канзас има седма най-висока степен на затлъстяване; Канзаски здравен институт
- Наднормено тегло и затлъстяване сред възрастните Здраве накратко Показатели за ОИСР 2019 OECD iLibrary