Резюме
Заден план
Доказано е, че пембролизумаб подобрява общата преживяемост (OS) и преживяемостта без прогресия (PFS) в сравнение с ипилимумаб при пациенти с нелекуван с ипилимумаб меланом; обаче няма публикувани данни за ефективността на разходите за пембролизумаб в сравнение със стандартните лечения, които в момента се използват в Хонконг за напреднал меланом.
Методи
Модел на разделена преживяемост, базиран на данни от скорошно рандомизирано проучване фаза 3 (KEYNOTE-006) и мета-анализ, е използван за извличане на време в PFS, OS и оцеляване след прогресията за пембролизумаб и химиотерапия, като дакарбазин (DTIC), темозоломид (TMZ) и комбинацията паклитаксел-карбоплатин (PC). За екстраполиране на PFS и OS криви е използвана комбинация от данни от клинични проучвания, публикувани данни, резултати от мета-анализ и данни от регистъра на меланома. Основният времеви хоризонт за модела е 30 години, като разходите и здравните резултати са намалени с 5% годишно. Данните за индивидуалното ниво на пациента за полезността и честотата на нежеланите събития са получени от окончателния анализ на KEYNOTE-006 (крайна дата: 3 декември 15) за пембролизумаб. Данните за разходите включват придобиване на лекарства, администриране на лечение, управление на нежелани събития и клинично управление на напреднал меланом. Разпределението на теглото на пациентите от популацията на Хонг Конг се прилага за изчисляване на разходите за лекарства. Анализите бяха извършени от гледна точка на платеца. Основният резултат е инкременталното съотношение на ефективност на разходите (ICER), изразено като цена в щатски долари (USD) за адаптирани към качеството години на живот (QALY).
Резултати
В основен случай, ICER за пембролизумаб като първа линия на лечение за напреднал меланом е 49 232 щатски долара в сравнение с DTIC, като стойностите на ICER са по-ниски от прага на ефективност на разходите в Хонконг. Резултатите, сравняващи пембролизумаб с TMZ и PC, са подобни на тези в сравнение с DTIC. Анализите на вероятностната чувствителност показват, че 99% от симулираните ICER са били под три пъти по-висок от брутния вътрешен продукт (БВП) на глава от населението за Хонконг (в момента при 119 274 $ // QALY праг). В анализ на сценарии, сравняващ пембролизумаб с ипилимумаб, прогнозният ICER е 8 904 щатски долара.
Заключения
Пембролизумаб е рентабилен в сравнение с химиотерапията (DTIC, TMZ и PC) и е изключително рентабилен в сравнение с ипилимумаб, за първа линия на лечение на напреднал меланом в Хонконг.
Ключови точки
Въпреки че са съществували предишни публикации, разглеждащи ефективността на разходите на инхибиторите на контролни точки при лечението на напреднали меланоми, повечето от тези предишни доклади са разглеждали ефективността на разходите между различни инхибитори на контролни точки (напр. Антипрограмирана клетъчна смърт-1 (PD-1) vs. антицитотоксичен свързан с Т-лимфоцитите протеин 4 — CTLA-4) или тяхното използване в комбинация. Цитотоксичните химиотерапии все още се използват рутинно като възможности за лечение от първа линия в различни юрисдикции. Остават оскъдни данни, насочени към разходната ефективност на инхибитора на контролния пункт спрямо цитотоксичните химиотерапии.
Извършихме модел на разделена преживяемост въз основа на данни, получени от рандомизираното проучване фаза 3 KEYNOTE-006 във връзка с предишни мета-анализи, използвани за извличане на време в PFS, OS и оцеляване след прогресия за пембролизумаб, както и химиотерапии.
За екстраполиране на PFS и OS криви са използвани комбинация от данни от клинични проучвания, публикувани данни, резултати от мрежов мета-анализ и данни от регистъра на меланома. Данните за разходите, включително придобиване на лекарства и администриране на лечение, са получени от актуализирана публикувана информация от болничната администрация в Хонг Конг, докато използването на ресурси, необходими за клиничното управление на нежелани събития, е определено от екип от клинични експерти.
Заключихме, че в Хонконг ICER за пембролизумаб като първа линия лечение при напреднал меланом в сравнение с цитотоксичните химиотерапии и ипилимумаб е съответно 49 232 и 8904 щатски долара. Анализите на вероятностната чувствителност показват, че 99% от симулираните ICER са под три пъти по-висок от брутния вътрешен продукт (БВП) на глава от населението за Хонконг (в момента на праг от 119 274 $/QALY).
Заден план
Въпреки че горните констатации са за Съединените щати, остава да се разгледа дали тези констатации са валидни и в други здравни заведения, където може да има основни разлики в структурата на финансиране на здравеопазването и наличните алтернативни възможности за лечение. Освен това в предишното проучване не е направено сравнение с конвенционалните цитотоксични вещества, които остават основата на противораковото лечение в голям брой юрисдикции, включително Хонконг.
В базовия случай оценихме ефективността на разходите на пембролизумаб срещу дакарбазин (DTIC) при пациенти с напреднал меланом в първата линия. Като част от анализа на чувствителността бяха разгледани по-нататък два сценария, включително сравняване на ефективността на разходите на (i) пембролизумаб спрямо ипилимумаб и (ii) пембролизумаб спрямо други цитотоксични химиотерапии (темозоломид-TMZ и комбинация от паклитаксел-карбоплатин-PC) при тази популация, въз основа на разходите за здравеопазване и наличните терапии в системата на общественото здравеопазване в Хонконг.
Методи
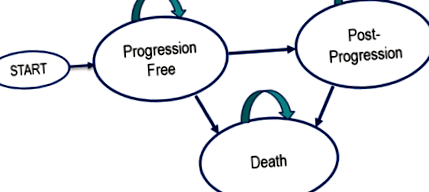
С помощта на Excel е изграден разделен модел на оцеляване с три взаимно изключващи се здравни състояния: без прогресия, след прогресия и смърт. Пациентите, моделирани след тези в проучването KEYNOTE-006, започват в състояние без прогресия (PF). Състоянието на прогресивно заболяване (PD) възниква след първата прогресия, определена в проучването от независим преглед на рентгенолог и онколог, използвайки критериите за оценка на отговора при твърди тумори (RECIST) версия 1.1 [3] (фиг. 1).
Преходна диаграма на симулационния модел
В модела пембролизумаб е дозиран от 2 mg/kg на всеки 3 седмици (Q3W) и е даван за период до 24 месеца. Тези, които все още са в преживяемост без прогресия (PFS) в края на 24 месеца, са имали право да получат до 12 месеца реиндукционно лечение, ако са имали прогресия на заболяването в рамките на 2-годишен период на проследяване.
Времевият хоризонт в анализа на базовия случай на модела беше 30 години, тъй като той улавя разликите в живота за ползите за здравето и разходите за тези възможности за лечение. Кратките хоризонти бяха тествани при анализи на чувствителността.
Моделирането на PFS и общата преживяемост (OS) за пембролизумаб (Q3W) се основава на данни от пациенти KEYNOTE-006, лекувани с пембролизумаб на всеки 3 седмици (т.е. общо 277 пациенти). Пропорциите на пациентите във всяко здравословно състояние са изчислени въз основа на действителните и прогнозирани криви на оцеляване за PFS и OS. За кривите на PFS бяха използвани оценки на Kaplan – Meier от KEYNOTE-006 през първите 13 седмици. Седмица 13 беше избрана като гранична точка за проектиране на дългосрочен PFS, тъй като в кривата на Каплан-Майер имаше прекъсване, свързано с радиологично сканиране, управлявано от протокол. След това моделът използва параметрични функции за оцеляване, приспособени към пробните данни от седмица 13 и след това за проектиране на PFS. За базовия случай беше използвано разпределение на Weibull, основаващо се на доброто състояние на статистиката за пригодност и клиничното мнение, че по-плоската опашка по-добре ще отразява дългосрочната полза от имунотерапията.
Моделът предполага, че най-добрата поддържаща грижа (включваща „без активно лечение“) е единствената последваща терапия, приложена след прогресия и за двете лечебни лекарства. Това предположение беше приложено, тъй като данните от изпитванията не показаха значителна разлика в употребата на наркотици след прогресията между двете рамена и други предположения биха наложили спекулации относно ефикасността от различни последователности и продължителност на употребата на наркотици.
Данните за качеството на живот и нежеланите събития са получени главно от окончателния анализ на продължаващото проучване KEYNOTE-006 [8] и други публикувани източници [9]. Използваните в анализа разходи са извлечени от различни публикувани източници, докладвани през 2018 г. [10] и са описани по-долу.
Разходи
Разходите за администриране на лекарства на доза се изчисляват от нивата, извлечени от местните данни в Хонконг. Моделът включва и разходи за рутинни онкологични посещения в кабинета, лабораторни тестове, сканирания и други ресурси, използвани в различните здравни състояния въз основа на изследването INTUITION (виж Таблица 1) [11]. Моделът включва и еднократни разходи за терминална грижа, за да се доближат разходите за здравеопазване през последните 6 месеца от живота, както се изчислява от Wong et al. 2007 г. [12].
Нежеланите събития (AE) от степен на тежест 3 до 5, които засягат поне 3% от пациентите в поне едно от лечебните рамена, са включени в модела за двете рамена [8, 9]. В допълнение, диарията от степен 2+ е включена поради икономическото си въздействие. Предполага се, че разходите за ендокринни нарушения се извършват веднъж на всеки 6 месеца [13]. Разходите за управление на включената степен 3–5 AE са взети от обявени цени от Наредбата за болничните власти (Глава 113) [14].
Резултати от полезността
Резултатите от полезността са базирани на данни за качеството на живот, събрани в проучване KEYNOTE-006 с изключени липсващи стойности. Европейският въпросник за пет измерения за качеството на живот (EuroQoL EQ-5D) - беше прилаган при определени посещения при пациенти с пембролизумаб и ипилимумаб. Също така се прилага при посещения за прекратяване на употребата на наркотици и последващи посещения за безопасност на ден 30. Отговорите на въпросника EQ-5D бяха преобразувани в базирани на популацията стойности на полезност, използвайки смесен алгоритъм (където базираните в САЩ оценки бяха приложени за пациенти в САЩ, използвани бяха базите в Обединеното кралство за пациентите в Обединеното кралство и базите в ЕС за всички останали пациенти) тъй като специфичният за Хонконг алгоритъм в момента не е наличен. Изчислени са средните резултати на EQ-5D, свързани със следните категории време до смърт: 360 дни или повече, 270–360 дни, 90–270 дни, 30–90 дни и под 30 дни. Смъртта е получила помощна програма от 0 [2].
Резултатите от полезността, свързани с пациенти с нежелани събития от степен 3-5, също са сравнени с тези, когато пациентите не са имали нежелани събития. Разликата между посещенията със и без нежелани събития от степен 3-5 са използвани за оценка на средната неточност, свързана с нежелани събития. За анализа на базовия случай беше използван средният декремент на полезност за AE от анализа на обединените данни (т.е. 0,15) и продължителността на AE беше взета за 8 седмици. За всяко здравословно състояние бяха зададени специфични тежести за корекция на разходите и качеството на живот за всеки 1-седмичен цикъл, за да се изчислят кумулативните разходи и кумулативните QALY през времевия хоризонт на модела.
Разходите, свързани с AE, и намаленията на полезността са приложени поотделно за всяко лекарство, като се приемат събитията, настъпили в началото на проучването. Разходите и QALY са намалени при 5% годишно. За да се направи оценка на ефективността на разходите, моделът беше използван за проектиране на разходи, години на живот, QALY и нарастващите разходи за QALY, получени, свързани с използването на пембролизумаб спрямо сравнители при нелекувани пациенти.
Анализи на чувствителността
Проведените анализи на чувствителността включват: анализи на сценарии, детерминирани еднопосочни анализи на чувствителност и вероятностни анализи на чувствителност.
Анализите на чувствителността на сценария изследват въздействието на алтернативни сравнители (понастоящем не се възстановяват или не се използват като терапии от първа линия в Хонконг), няколко различни методологии, използвани при екстраполация на кривите на оцеляването (PFS и OS), оценки на полезността, базирани на здравето, основано на прогресията състояния (т.е. за всяко здравословно състояние преди и след прогресията). различни времеви хоризонти, дисконтови проценти и различни предположения относно стратегията за лечение на пембролизумаб.
Анализите на чувствителност по сценарий, като се вземат предвид алтернативни сравнителни средства, които понастоящем не се възстановяват или не се използват като лечения от първа линия за напреднал меланом в Хонконг, включват сравнения на пембролизумаб с имунотерапевтичното лекарство ипилимумаб, както и други химиотерапевтични лекарства като TMZ и PC комбинацията. За ипилимумаб е използван подобен подход за моделиране на този на пембролизумаб, с клинична ефикасност и безопасност, получени главно от пациенти в рамото на ипилимумаб KEYNOTE-006, и дългосрочни данни за ипилимумаб от Schadendorf et al. [4] и данни на AJCC. За други химиотерапевтични лекарства се приемаше същата клинична ефикасност като тази за DTIC, тъй като непреки сравнения на лечението бяха възможни само за пембролизумаб спрямо DTIC. Въз основа на клиничното мнение, очаква се ефикасността при различните химиотерапии да бъде сходна. Това предположение се подкрепя от проучвания, които показват, че химиотерапиите е малко вероятно да имат полза за оцеляване от гледна точка на туморен отговор и подобрено време до прогресия, или подобрена обща преживяемост спрямо най-доброто поддържащо лечение (BSC) при пациенти с напреднал меланом [15,16,17]. Освен това няма рандомизирани контролирани проучвания, които да демонстрират подобрение в преживяемостта с DTIC спрямо BSC.
Цената в списъка за ипилимумаб е била 5897,43 долара за флакон от 50 mg и е прилаган в доза от 3 mg/kg. Въз основа на разпределението на теглото на пациента от местните данни в Хонконг, са необходими средно 4,40 флакона от 50 mg. Цената на TMZ в списъка е била 0,71 $ на mg, а при доза от 1000 mg/m 2 (200 mg/m 2 пет пъти седмично), цената на доза TMZ се оценява на 1249,50 USD. Паклитаксел и карбоплатин бяха на разположение на списъчните цени от 0,26 $ за mg и 0,07 $ за mg, съответно със съответните им дози от 175 mg/m 2 и 300 mg/m 2, давани веднъж на всеки 3 седмици (средна телесна повърхност = 1,75 m 2) . Очакваните разходи на тези алтернативни сравнители, разгледани в анализите на сценариите, са представени в таблица 1.
Детерминистични еднопосочни анализи на чувствителност, фокусирани върху променливи стойности на параметри на модела, свързани с сравнението на базовия случай на DTIC с пембролизумаб. Стойностите на параметрите варираха за екстраполационните функции през очакваните 95% доверителни интервали, комуналните услуги бяха модифицирани с плюс-минус 20%, разходите за управление на заболяването с 25% и разходите за управление на AE от 50 до 200% като най-добрите предположения за техния потенциален диапазон ограничени налични количествени данни.
Освен това е извършен анализ на вероятностния чувствителност (PSA) въз основа на 1000 комплекта едновременни проби от определени разпределения на вероятностите на входовете на модела. Основните разпределения включват бета разпределение, използвайки средната и стандартната грешка за помощните програми, базирани на клиничното изпитване, и регистрирайте нормалните разпределения за входящите разходи, използвайки средства, равни на основната стойност на случая и стандартни грешки, както се съобщава в литературата, или консервативно зададени при 20% от стойността на базовия случай. В допълнение, PSA включва несигурност във функционалните форми на екстраполационните функции въз основа на присвояване на разпределения за ключовите параметри, характеризиращи екстраполационните функции. Въз основа на 1000 оценки за нарастващите разходи за получена QALY, вероятността пембролизумаб и компаратор да бъдат рентабилни при различни прагове за готовност за плащане са показани с помощта на кривата на приемливост на рентабилността.
Резултати
Анализ на базовия случай
Подробни резултати от анализите на базовия случай са показани в Таблица 2 и Фигура 1. Пациентите, лекувани с пембролизумаб, са прекарали средно 2,36 години в състояние без прогресия и 5,48 години в състояние след прогресиране, което води до средно оценка на оцеляването от 7,83 години. В рамото с DTIC пациентите прекарват средно 0,61 години в здравословно състояние без прогресия и 2,13 години в състояние на PD за средно време на оцеляване от 2,74 години. Следователно, пембролизумаб е свързан с увеличение на средната преживяемост от 5,09 години.
По отношение на QALYs, пембролизумаб е свързан със средна (намалена) печалба от 2,64 QALY над DTIC. В допълнение, базовият модел прогнозира разлика от $ 95 052 в общите средни разходи за лечение на пациент с пембролизумаб спрямо DTIC. Следователно, ICER за пембролизумаб е бил $ 35,993/QALY ($ 18,668 на LY) за период от 30 години (Фиг. 2).
Моделирана без прогресия и обща преживяемост за пембролизумаб и DTIC (време в седмици)
- Лечение на диария Информация за първа помощ при диария
- Уважаеми дневник на храната - Какво да напиша в Грижата за лечението на моя диетичен дневник; Съвети
- Причини за студени ръце, болести, лечение - Всички грижи за моето семейство
- Диета и добавки за профилактика и лечение на рак на простатата Сиатъл Алианс за грижа за рака
- Clarins Масло-тоник за грижа за тялото (3