Катрин Е Олденбург
1 Фондация Франсис I. Проктор
2 Катедра по офталмология, Калифорнийски университет, Сан Франциско, Калифорния
3 Катедра по епидемиология и биостатистика, Калифорнийски университет, Сан Франциско, Калифорния
Али Сие
4 Center de Recherche en Santé de Nouna, Nouna, Буркина Фасо
Бубакар Кулибали
4 Center de Recherche en Santé de Nouna, Nouna, Буркина Фасо
Лусиен Оуерми
4 Center de Recherche en Santé de Nouna, Nouna, Буркина Фасо
Кларис Дах
4 Center de Recherche en Santé de Nouna, Nouna, Буркина Фасо
Карл Велики Тапсоба
4 Center de Recherche en Santé de Nouna, Nouna, Буркина Фасо
До Bärnighausen
5 Хайделбергски институт за обществено здраве, Хайделберг, Германия
6 Африкански институт за здравни изследвания, Сомхеле, Южна Африка
7 Департамент за глобално здраве и население, Харвардско училище за обществено здраве, Бостън, Масачузетс
Катрин Джей Рей
1 Фондация Франсис I. Проктор
Лина Джонг
1 Фондация Франсис I. Проктор
Сузи Къмингс
1 Фондация Франсис I. Проктор
Елоди Лебас
1 Фондация Франсис I. Проктор
Томас М Литман
1 Фондация Франсис I. Проктор
2 Катедра по офталмология, Калифорнийски университет, Сан Франциско, Калифорния
Джеръми Д Кийнън
1 Фондация Франсис I. Проктор
2 Катедра по офталмология, Калифорнийски университет, Сан Франциско, Калифорния
Туй Доан
1 Фондация Франсис I. Проктор
2 Катедра по офталмология, Калифорнийски университет, Сан Франциско, Калифорния
Свързани данни
Резюме
Заден план
Излагането на антибиотици може да доведе до промени в състава на чревната микробиота. Въпреки това са проведени малко опити и наблюдателните изследвания подлежат на объркване по индикация. Проведохме рандомизирано контролирано проучване, за да определим ефекта на 3 често използвани педиатрични антибиотици върху чревния микробиом при здрави деца в предучилищна възраст.
Методи
Деца на възраст 6–59 месеца са рандомизирани (1: 1: 1: 1) на 5-дневен курс от 1 от 3 антибиотици, включително амоксицилин (25 mg/kg/ден дози два пъти дневно), азитромицин (10 mg/kg доза на първия ден и след това 5 mg/kg веднъж дневно в продължение на 4 дни), котримоксазол (240 mg веднъж дневно) или плацебо. Ректални тампони бяха получени на изходно ниво и 5 дни след последната доза и бяха обработени с помощта на 16S rRNA генно секвениране. Предварително посоченият първичен резултат е обратният индекс на α-разнообразие на Симпсън.
Резултати
Разнообразието на Simpson след лечението беше значително различно в четирите рамена (P = .003). Средното α-разнообразие на Симпсън сред лекуваните с азитромицин деца е значително по-ниско, отколкото при лекуваните с плацебо деца (6,6; 95% доверителен интервал [CI], 5,5–7,8; срещу 9,8; 95% CI, 8,7–10,9; P = .0001 ). Разнообразието при деца, лекувани с амоксицилин (8.3; 95% CI, 7.0–9.6; P = .09) или котримоксазол (8.3; 95% CI, 8.2–9.7; P = .08), не се различава значително от плацебо.
Заключения
Азитромицин влияе върху състава на детския чревен микробиом. Ефектът на амоксицилин и котримоксазол върху микробиомния състав е по-малко ясен.
Регистрация на клинични изпитвания
Счита се, че излагането на антибиотици в детска възраст променя чревния микробиом [1–3]. Наблюдателни проучвания в условия с високи доходи предполагат, че има промени в чревния микробиом при деца, получаващи антибиотици, спрямо тези, които не са получавали антибиотици [3–5]. Антибиотиците нарушават състава на микробиотата, тъй като имат активност срещу коменсални и патогенни бактерии [2]. Дисбиозата на чревния микробиом е свързана с множество неблагоприятни последици за здравето, включително недохранване и затлъстяване, астма, диабет и някои форми на рак [6–14].
Неотдавнашно рандомизирано контролирано проучване оценява ефекта на единична доза азитромицин, използван за масово разпределение в програмите за контрол на трахома [15-17], върху състава на чревния микробиом сред деца в предучилищна възраст в Нигер [1]. Това проучване установи значително намаляване на разнообразието на чревния микробиом в популация от сравнително нелекувани деца. В много региони на Африка на юг от Сахара макролидите се използват по-рядко от пеницилините или сулфонамидите за лечение на често срещани детски болести [18–20]. Тук оценяваме ефекта на кратък курс от 3 често използвани детски антибиотици върху чревния микробиом. Ние предположихме, че и трите антибиотика ще доведат до намалено разнообразие в чревния микробиом в сравнение с плацебо.
МЕТОДИ
Настройка на проучването
Това проучване се проведе в 2 селски общности от сайта за здравно и демографско наблюдение (HDSS) в област Nouna, Буркина Фасо [21, 22]. Тригодишно преброяване се извършва в HDSS от Центъра за научни изследвания в Санте де Нуна (CSRN). Жителите на изследваните общности са предимно натурални фермери и стопани на говеда. Изследването се проведе през юли 2017 г., точно преди дъждовния сезон [23].
Участници и процедури
Общата цел на изследването е да изследва преките и косвените ефекти от употребата на антибиотици върху чревния микробиом на деца в предучилищна възраст. Набрахме домакинства в 2-те проучвани общности с 2 или 3 деца на възраст между 6 и 59 месеца въз основа на последното преброяване на HDSS. В домакинства с 3 деца всички деца са получавали изследвано лекарство, но само 2 произволно избрани деца са били наблюдавани като част от проучването. Децата имаха право да участват в проучването, ако бяха на възраст между 6 и 59 месеца и със съгласието на родителите. Не изключихме децата въз основа на съществуваща заболеваемост или скорошна употреба на антибиотици. Децата бяха оценени преди рандомизиране (изходно ниво) и след това отново 5 дни след последната доза антибиотик (след лечение).
Рандомизация
Използвахме двуетапна процедура на рандомизация. Първо, всяко домакинство беше рандомизирано по начин 1: 1: 1: 1 на 1 от 4-те проучвани рамена: 1) амоксицилин, 2) азитромицин, 3) ко-тримоксазол или 4) плацебо. Второ, всяко дете в домакинството е разпределено на случаен принцип или за лечение, или за плацебо. В домакинства с 2 деца 1 е рандомизирано за лечение, а другото за плацебо. В домакинства с 3 деца 2 са рандомизирани за лечение, а другото за плацебо. Имайте предвид, че в домакинствата с плацебо децата, назначени на лечение и плацебо, са получавали същото лекарство (т.е. плацебо). Настоящият доклад се занимава с преките ефекти на антибиотиците и следователно включва само 1 дете на домакинство, рандомизирано за лечение. Последователността на рандомизацията е генерирана от TCP в R, версия 3.3.1 (The R Foundation for Statistical Computing), като се използва маскирана стойност на семената [24]. Последователността на рандомизацията беше приложена на място чрез предварително зареждане на спринцовки с рандомизираното лечение на детето, които бяха обозначени с името на всяко дете (описано по-долу).
Интервенции
Маскиране
На лечебните екипи не е казана самоличността на изследваното лекарство, а оранжевото оцветяване на спринцовките е помогнало да се прикрие идентичността на изследваното лекарство. Поради различия във вкуса и външния вид обаче, лекуващият екип не е маскиран. За разлика от това, екипите за изследване са били маскирани за назначение на лечението, а лабораторният персонал е бил маскиран за назначение на лечение и времева точка.
Изходен въпросник
На изходно ниво болногледачът на всяко дете попълни кратък въпросник, свързан с детето и домакинството на детето. Въпросите за здравния статус включват дали детето наскоро е посещавало здравно заведение и ако е така, дали детето е било лекувано с антибиотици след посещението. Попитателите са попитани дали детето в момента кърми.
Оценка на резултатите
Определяне на размера на пробата
Изчислението на размера на извадката се основава на основния резултат, α-разнообразието на Симпсън. Въз основа на предишно проучване в Нигер се изчислява, че размерът на извадката от 30 деца на ръка осигурява най-малко 80% мощност за откриване на разлика от 1,5 единици в α-разнообразието на Симпсън [1].
Статистически методи
РЕЗУЛТАТИ
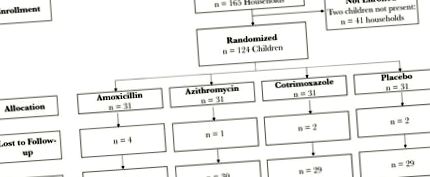
През юли 2017 г. 248 деца в 124 домакинства бяха записани и рандомизирани към 1 от 3-те антибиотични режима или плацебо (Фигура 1). От тях 124 деца са рандомизирани в домакинството си за лечение и са включени в този анализ. От тези деца на 120 (96,8%) е направен ректален тампон, взет 5 дни след последната им доза на антибиотик. Средната възраст (интерквартилен диапазон) е била 36 (21–51) месеца и 54,0% от децата са жени (Таблица 1). В момента една четвърт (27,4%) кърмеха, а 7,3% са получили антибиотик от здравно заведение през последния месец. Базовите характеристики бяха добре балансирани в четирите проучвания. Придържането към изследваните лекарства и нежеланите събития са докладвани по-рано [30]. Повече от 90% от децата са получили разпределеното си лекарство за изследване в повечето моменти от време. Нежеланите събития са необичайни и не се наблюдава диария в нито едно от антибиотичните рамена. 16S рРНК генният анализ на фекалните проби идентифицира 429 уникални рода. Както при изходното ниво, така и след лечението, най-често срещаният род е Prevotella spp. (Допълнителна фигура 1).
Консолидирани стандарти за отчитане на изпитвания на диаграмата.
маса 1.
Базови характеристики по проучване
| Възраст, медиана (IQR), месечно | 32 (23–48) | 29 (21–51) | 37 (23–48) | 38 (23–51) |
| Женски пол, № (%) | 15 (48,4) | 18 (58,1) | 20 (64,5) | 14 (45,2) |
| Наскоро посетено здравно заведение, № (%) | 6 (19,4) | 4 (12,9) | 6 (19,4) | 5 (16,1) |
| Скорошна употреба на антибиотици, № (%) | 2 (6.5) | 2 (6.5) | 3 (9,7) | 2 (6.5) |
| Кърмене, № (%) | 6 (19,4) | 11 (35,5) | 9 (29,0) | 8 (25,8) |
Съкращение: IQR, интерквартилен диапазон.
Таблица 2.
Алфа разнообразието на Симпсън и Шанън на изходно ниво и след лечение
| Симпсън (обратно) ефективно число, средно (95% CI) | 10.2 (8,8–11,5) | 8.3 (7,0–9,6) | 8.8 (7,5–10,1) | 6.6 (5,5–7,8) | 9.7 (8,2–11,2) | 8.3 (6,9–9,7) | 9.6 (8,6–10,7) | 9.8 (8,7–10,9) |
| Шанън (експоненциално) ефективно число, средно (95% CI) | 16.6 (14,5–18,7) | 13.9 (12,1–15,8) | 14.6 (13,0–16,2) | 11.0 (9,3–12,7) | 15.6 (13,4–17,8) | 13.5 (11,6–15,4) | 15.4 (14,1–16,7) | 16,0 (14,3–17,8) |
Съкращение: CI, доверителен интервал.
Разпределение на индексите на алфа разнообразие на Симпсън (A) и Шанън (B) на изходно ниво и 5 дни след окончателното проучване за деца, лекувани с плацебо (черни линии), азитромицин (червени линии), амоксицилин (сини линии) и котримоксазол (зелен линии).
Анализ на основните координати (PCoA), сравняващи евклидовото разстояние между плацебо и азитромицин (A), плацебо и амоксицилин (B) и плацебо и котримоксазол (C). Центроидите са изобразени с квадратни точки.
ДИСКУСИЯ
Курсът на азитромицин значително намалява чревното бактериално разнообразие и състав при деца в Буркина Фасо, в съответствие с предишно проучване в Нигер [1]. В предишното проучване децата са получавали единична доза азитромицин или плацебо, със същото дозиране, използвано от програмите за контрол на трахома и скорошно проучване, изследващо ефекта на азитромицин върху оцеляването на децата [15, 16, 31, 32]. Тук използвахме 5-дневен курс с дозиране, еквивалентно на Z-пакет, често срещан курс за лечение на леки инфекции при деца като отит на средното ухо. Взети заедно, резултатите от тези проучвания предполагат окончателно намаляване на чревното бактериално разнообразие след курс на азитромицин при деца.
Предишни проучвания в условия с високи доходи показват, че дисбиозата на чревния микробиом може да бъде свързана със заболеваемост при деца, включително астма [9], хранителна алергия [33] и затлъстяване [34]. В условия на ниски доходи се забелязват различия в чревното разнообразие при деца с различни форми на тежко остро недохранване [12] и при двойки двойки, несъответстващи на квашиоркор [8]. Доказано е, че антибиотиците водят до увеличаване на теглото при деца в рандомизирани контролирани проучвания [30, 35]. Промяната в чревния микробиом, предизвикана от употребата на антибиотици, може да повлияе на усвояването на хранителни вещества или енергийния метаболизъм, който може да повлияе на наддаването на тегло при деца [36, 37], или наддаването на тегло след употребата на антибиотик може да бъде медиирано чрез намаляване на тежестта на ентеропатогените. Клиничните последици от един курс на антибиотици обаче остават неясни.
Трябва да се отбележат няколко ограничения. Продължителността на проследяването в настоящото проучване е кратка и по този начин се оценяват краткосрочните промени в чревния микробиом след курс на антибиотици. Някои проучвания показват, че може да има дългосрочни промени в микробиома след употреба на антибиотици при деца [4]. Възможно е промените, наблюдавани в настоящото проучване, да са преходни или да продължат няколко месеца. Неотдавнашната употреба на антибиотици беше необичайна в изследваната популация, но можеше да се получи замърсяване на назначението на лечението, ако децата използваха антибиотици, различни от изследваното лекарство по време на проучването. Това проучване е проведено в селски район на Буркина Фасо, който се характеризира с висока инфекциозна тежест и висока смъртност. Резултатите от това проучване може да не са обобщителни за деца, живеещи в различни условия, тъй като микробиомът при деца се различава значително географски [38]. Резултатите от това проучване обаче подкрепят предишни наблюдателни и рандомизирани проучвания, които показват ефекти върху чревното микробно разнообразие след употреба на антибиотици [1, 4, 5, 39].
В това рандомизирано контролирано проучване на 3 често използвани антибиотици, ние демонстрирахме, че кратък курс на азитромицин води до значително намаляване на бактериалното разнообразие на чревния микробиом при деца в предучилищна възраст. Дозирането на амоксицилин и котримоксазол, съответстващо на дозата, използвана за профилактика при деца, живеещи с ХИВ, не води до значителна разлика в бактериалното разнообразие. Въпреки че клиничните последици от един курс на антибиотици са неясни, резултатите от това проучване показват, че чревният микробиом при малки деца е чувствителен към антибиотици.
Допълнителни данни
Допълнителни материали са достъпни в Open Forum Infectious Diseases онлайн. Състоящи се от данни, предоставени от авторите в полза на читателя, публикуваните материали не се редактират и са изцяло отговорност на авторите, така че въпроси или коментари трябва да бъдат адресирани до съответния автор.
Допълнителна таблица 1
Благодарности
Финансова подкрепа. Тази работа беше подкрепена отчасти от Изследването за предотвратяване на наградата за кариерно развитие на слепота (на C.E.O. и T.D.) и Националния институт за очите на Националните здравни институти под номер на награда K08EY026986 (на T.D.). Финансистите не играят роля в дизайна на проучването, анализа, интерпретацията на резултатите или решението за публикуване.
Потенциални конфликти на интереси. Всички автори: няма съобщени конфликти на интереси. Всички автори са подали формуляра ICMJE за разкриване на потенциален конфликт на интереси. Разкрити са конфликти, които редакторите смятат за релевантни на съдържанието на ръкописа.
- Детски безплатни пълнотекстови педиатрични затлъстели черен дроб и затлъстяване Не винаги е въпрос на безалкохолно
- Деца и антибиотици - защо трябва да бъдете предпазливи Крис Кресър
- Започване на ентерално хранене при деца, приети в педиатрични отделения за интензивно лечение след травматично
- Проблеми с храната, антибиотиците и поведението при децата - детско хранене
- Гломерулна болест (детска) CS Mott Детска болница Мичиган Медицина