Ахмед Мадиш
1 отделение по гастроентерология, интервенционална ендоскопия, 4 диабетология и остра гериатрия, болница KRH Siloah, Хановер
Виола Андресен
2 Медицинско отделение, Израелска болница, Хамбург
Пол Енк
3 Вътрешни болести VI: Психосоматична медицина и психотерапия, Университетска болница Тюбинген, Тюбинген
Йоахим Лабенц
4 Катедра по медицина, болница Diakonie Jung-Stilling, Siegen
Томас Фрилинг
5 Катедра по гастроентерология, болница Helios Krefeld, Крефелд
Майкъл Шеман
6 Катедра по човешка биология, ТУ Мюнхен, Фрайзинг
Резюме
Заден план
Функционалната диспепсия (ФД) е едно от най-често срещаните функционални разстройства, с разпространение 10–20%. Засяга стомашно-чревния тракт.
Методи
Тази статия се основава на публикации, извлечени чрез селективно търсене на PubMed, със специално внимание към контролираните опити, насоки и рецензии.
Резултати
Типичните диспептични симптоми при функционална диспепсия включват болка в епигастриума, усещане за натиск и пълнота, гадене и ранна субективна ситост. Етиологията на разстройството е разнородна и многофакторна. Причините, които допринасят, включват нарушения на подвижността, висцерална свръхчувствителност, повишена пропускливост на лигавицата и нарушения на автономната и чревната нервна система. Все още няма причинно-следствено лечение на функционална диспепсия. Лечението му трябва да започне с интензивно обучение на пациентите относно доброкачествения характер на разстройството и със създаването на терапевтичен пакт за дългосрочни грижи. Като се има предвид липсата на причинно-следствено лечение, лекарства за лечение на функционална диспепсия трябва да се дават за не повече от 8–12 седмици. Инхибиторите на протонната помпа, фитотерапевтичните лекарства и ликвидирането на Helicobacter pylori са интервенции, основани на доказателства. За неразрешими случаи трицикличните антидепресанти и психотерапията са допълнителни ефективни възможности за лечение.
Заключение
Нарушеното качество на живот на пациенти с функционална диспепсия предполага необходимостта от окончателно установяване на диагнозата, последвано от симптоматично ориентирано лечение за продължителността на симптоматичния интервал.
Терминът диспепсия (гръцки „дис“ [лош], „пепсис“ [храносмилане]) се използва за спектър от симптоми, локализирани от пациента в епигастралната област (между пъпа и мечовидния процес) и фланговете. Тези симптоми включват болка и парене в епигастриума (60 до 70%), чувство на подуване след хранене (80%), ранно насищане (60 до 70%), разтягане в епигастралната област (80%), гадене (60%) и повръщане (40%). Симптомите на диспепсия могат да бъдат остри, например при гастроентерит или хронични. В последния случай основните органични (напр. Язва, рефлукс, панкреатично заболяване, сърдечни и мускулни заболявания) или функционални фактори могат да бъдат отговорни.
Определение
Терминът диспепсия (гръцки „дис“ [лош], „пепсис“ [храносмилане]) се използва за спектър от симптоми, локализирани от пациента в епигастралната област (между пъпа и мечовидния процес) и хълбоците.
При диагностичната работа се установява, че 20 до 30% от пациентите с диспепсия имат заболявания, които отчитат техните симптоми (1, 2). Функционална диспепсия (синоним: синдром на раздразнен стомах) е налице, когато рутинните диагностични изследвания, включително ендоскопия, не идентифицират никакви причинно-следствени структурни или биохимични аномалии (1–6). Констатации като камъни в жлъчката, хиатусна херния, стомашни ерозии или „гастрит“ не обясняват непременно симптомите и следователно не противоречат на диагнозата функционална диспепсия.
На фона на професионалния ни опит извършихме селективно търсене на литературата в PubMed. Критериите за включване бяха следните:
Функционална диспепсия
Функционална диспепсия (синоним: синдром на раздразнен стомах) е налице, когато рутинните диагностични изследвания, включително ендоскопия, не идентифицират никакви причинно-следствени структурни или биохимични аномалии.
Пълен текст на английски или немски
Видове проучвания: „клинично изпитване“, „рандомизирано контролирано проучване“, „метаанализ“, „систематичен преглед“, „насоки за практиката“, „насоки“, „преглед“.
Учебни цели
След като завърши тази статия, читателят трябва:
Знайте как се определя функционалната диспепсия в съответствие с настоящите насоки
Бъдете запознати с критериите, според които функционалната диспепсия може да се прояви клинично
Да може да изпълнява общите мерки на първичната помощ и да е придобил познания за възможностите за медицинско лечение, за които има доказателства за ефективност срещу функционална диспепсия.
Определение за функционална диспепсия
Според наскоро преработените критерии „Рим IV“ (1), функционалната диспепсия се определя от:
Постоянна или повтаряща се диспепсия за повече от 3 месеца през последните 6 месеца
Няма демонстрация на възможна органична причина за симптомите при ендоскопия
Няма признак, че диспепсията се облекчава само чрез дефекация или от асоциация с нередности на изпражненията.
Този последен критерий е въведен, за да се изключи синдромът на раздразненото черво (IBS) като възможна причина за симптомите, въпреки че около 30% от пациентите с функционална диспепсия също имат IBS.
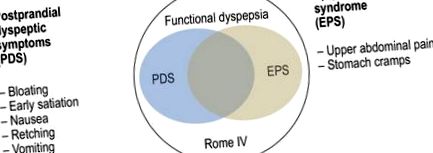
Настоящите критерии Рим IV (1) разделят функционалната диспепсия на две подгрупи според кардиналните симптоми (фигура 1):
Определение на функционалната диспепсия съгласно критериите от Рим IV (1)
Синдром на епигастриална болка (EPS) - преобладаваща епигастрална болка или парене
Постпрандиален дистрес синдром (PDS) - усещане за пълнота и ранно засищане.
Епидемиология и естествено протичане на болестта
Функционалната диспепсия е разделена на две подгрупи според кардиналните симптоми:
Синдром на епигастриална болка (EPS) - преобладаваща епигастрална болка или парене
Постпрандиален дистрес синдром (PDS) - усещане за пълнота и ранно засищане.
Диспептичните симптоми са често срещани и причиняват значителни преки (посещения при лекар, лекарства и др.) И особено непреки разходи (отсъствие от работа) (3). Около 18 до 20% от германците се оплакват от подуване на корема, метеоризъм, киселини и диария (6). В проспективното национално проучване за гастро ентерологично наблюдение (DIGEST) проучване на над 5500 души показва, че около една трета от интервюираните нормални лица съобщават за диспептични симптоми, включително остра диспепсия при 6,5% и хронична диспепсия в 22,5% от случаите (7, 8 ). Само при 10 до 25% социалното въздействие на техните симптоми е достатъчно голямо, за да се консултират с лекар (3). Както показва англо-американско проучване, тази група обаче причинява разходи в размер на няколко милиарда евро всяка година. Тези разходи са или преки, причинени от търсенето на здравни услуги, или непреки чрез отсъствие от работа и ранно пенсиониране (7, 9). Болестта показва периодичен ход, фази на леки или никакви симптоми, редуващи се с периоди на интензивни оплаквания. Само 20% от пациентите с функционална диспепсия се освобождават от симптоми в дългосрочен план (1, 2, 5, 6).
Патогенеза на функционалната диспепсия
Причините за функционалната диспепсия са разнородни и многофакторни. През последните десетилетия многобройни систематични патофизиологични проучвания, сравняващи пациенти с функционална диспепсия със здрави доброволци, показаха, че функционалната диспепсия е органично разстройство, въпреки че патофизиологично значимите фактори, обсъдени в по-нататъшния ход на тази статия, понастоящем не могат да бъдат открити чрез рутинна клинична работа (5, 10–13). Това включва нарушения на подвижността, сензорно-двигателна дисфункция, свързана със свръхчувствителност към механични и химични стимули, имунна активация, повишена пропускливост на лигавицата в проксималното тънко черво и нарушения на вегетативната и чревната нервна система (таблица 1) (12). Както е при много заболявания, причинната връзка между развитието на симптомите и органичните разстройства все още не е изяснена. Също така е важно нарушенията да не се появяват при всички пациенти и промените в подвижността и чувствителността да не се ограничават до стомаха. Освен това не са провеждани проучвания, за да се установи кои фактори се срещат заедно или в изолация един от друг.
маса 1
| Патофизиологично значими фактори | |
| Нарушения на подвижността | ● Нарушено обемно приспособяване на очното дъно ● Непропорционално разпределение на обема в стомаха (твърде много в антралната част, твърде малко в очното дъно) ● Нисък обем на поглъщане при изпитване на пиене ● Антрална хипомотивност и ↓ антрални миграционни двигателни комплекси (фаза III на междупоглъщаща моторика) ● Некоординирана антродуоденална подвижност ● Повишена постпрандиална подвижност на дванадесетопръстника ● Недостатъчни инхибиторни компоненти на перисталтичния рефлекс в тънките черва |
| Сензомоторни нарушения | ● Намалена възбудимост на чревните нерви в дванадесетопръстника ● Глиоза в дуоденалния субмукозен плексус ● ↓ Парасимпатиков тонус ● ↑ Киселинна чувствителност в дванадесетопръстника ● ↑ Мастна чувствителност в дванадесетопръстника, свързана с ↑ CCK чувствителност ● ↑ Концентрация на глад и след хранене CCK, но ↓ PYY концентрация ● ↓ CgA + ентероендокринни клетки в дванадесетопръстника |
| Висцерална свръхчувствителност | ● ↑ Чувствителност след разширяване на стомаха (на празен стомах и след хранене) ● ↑ Чувствителност след разширение на дванадесетопръстника, йеюналната и ректума |
| Постинфекциозна пластичност на дванадесетопръстника | ● ↑ CD8 + цитотоксични Т-клетки CD 68+ и CCR2 + макрофаги ● ↓ CD4 + Т-помощни клетки в дванадесетопръстника |
| Имунно активиране | ● ↑ GDNF, еозинофилни гранулоцити и макрофаги в проби от биопсия на дванадесетопръстника на лигавицата ● ↑ Дегранулация на еозинофилните гранулоцити в дванадесетопръстника ● TH2-медииран отговор в дванадесетопръстника ● ↑ Експресия на GDNF и NGF в H. pylori-позитивната стомашна лигавица |
| Дисфункционална чревна бариера | ● ↑ Пропускливост в проксималното тънко черво |
| Генетично предразположение | ● ↑ GNβ3-TT генотип (повишена сигнална трансдукция между рецептор и целеви протеин) ● ↓ CCK-A рецептор CC генотип |
| Биопсихосоциални фактори | ● ↑ Тревожност, депресия, соматизация, невротизъм ● ↑ Опит на злоупотреба, стресови събития в живота ● ↓ Функционална свързаност на мозъчните региони |
| Променена микробиота | ● ↑ Prevotella ● Helicobacter pylori |
CCK, холецистокинин; CgA, хромогранин А; GDNF, невротрофичен фактор, получен от глиална клетъчна линия; GNß3, G-протеин ß полипептид-3; NGF, нервен растежен фактор; PYY, пептид YY
Пациентите с функционална диспепсия имат нарушено акомодация на проксималния стомах както след балонна дилатация на стомаха, така и след хранене (14). Това се показва и в двата случая чрез неадекватно отпускане на очното дъно. Резултатът е непропорционално разпределение на съдържанието на стомаха, с по-голям обем в антралната част, отколкото в очното дъно (15). Установено е, че степента на антрално разширение е свързана с нарастваща тежест на симптомите (общ резултат от симптомите на ранно насищане, епигастрална болка, подуване на корема и гадене или повръщане) (14, 15). Освен това пациентите с функционална диспепсия също показват нарушена релаксация на фундуса след разширяване на дванадесетопръстника (16).
Епидемиология
Диспептичните симптоми са често срещани и причиняват значителни преки и особено косвени разходи (3). Около 18 до 20% от германците се оплакват от подуване на корема, метеоризъм, киселини и диария.
Както с празен стомах, така и след хранене, пациентите с функционална диспепсия страдат от висцерална свръхчувствителност, когато стомашният фундус е разширен (17, 18). Делът на пациентите, за които е установено, че имат тази свръхчувствителност, зависи от диагностичните критерии и от това дали свръхчувствителността се определя като анормална проекция на болка, алодиния и/или хипералгезия. Във всеки случай свръхчувствителността корелира с тежестта на симптомите (19). Дори пациенти с нормално настаняване на фундуса могат да реагират свръхчувствително на разширяване на стомаха (20), а някои пациенти с функционална диспепсия също реагират свръхчувствително на разширяване на дванадесетопръстника, йеюнума или ректума (21). Това откритие сочи към генерализирана, а не към локална висцерална сенсибилизация на еферентния или аферентния ентеричен нерв или на сензорните нерви, свързващи червата с централната нервна система (ос на червата и мозъка). Свръхчувствителността след разширяване на стомаха се подобрява чрез инхибиране на холинергичния тонус, но не и чрез активна мускулна релаксация чрез NO донорен нитроглицерин (22). Това показва преобладаващата роля на холинергичната ентерична инервация в произхода на свръхчувствителността.
Симптомите на функционална диспепсия се появяват след вливане на киселина в дванадесетопръстника (23) и вероятно са резултат от сенсибилизирани сензори за рН или недостатъчно отстраняване на киселината поради нарушена двигателна функция на проксималния дванадесетопръстник (24). Това е в съответствие с повишената чувствителност към капсаицин (25). Капсаицинът е TRPV1 агонист (преходен рецепторен потенциален катионен канал подсемейство V член 1), който се стимулира от, наред с други фактори, намалено рН.
Наличието на мазнини в дванадесетопръстника предизвиква симптомите на функционална диспепсия поради пряко невронно действие, повишена чувствителност на ентероендокринните клетки, системно или локално повишаване на концентрацията на холецистокинин и/или повишена чувствителност на холецистокинин-А рецепторите (26).
Ролята на психичните фактори в патогенезата
Психични фактори
Пациентите с функционална диспепсия имат по-висок резултат от тези без стомашно-чревни симптоми за депресия, тревожност и соматизация, които са по-силно свързани с намалено качество на живот, отколкото самите клинични симптоми.
Въпреки че функционалната диспепсия се различава както по симптоми, така и по клинични признаци от IBS (27), другите често срещани функционални разстройства в сферата на гастроентерологията, по отношение на значението на психичните фактори в патогенезата, диагностиката и лечението, има повече прилики, отколкото разлики между двете болести. На психометрични тестови скали пациентите с функционална диспепсия имат по-висок резултат от тези без стомашно-чревни симптоми за депресия, тревожност и соматизация, които са по-силно свързани с намалено качество на живот, отколкото самите клинични симптоми (13). Това сочи към „патологична” централна обработка на висцерални стимули, напр. Повишена бдителност спрямо специфични усещания от страна на стомашно-чревния тракт. Тази повишена бдителност може да възникне в контекста на постинфекциозна сенсибилизация. Честото свързване на функционална диспепсия с други чревни и извън чревни заболявания също показва "нарушение на соматизацията", подобно на IBS. Тези възможни биопсихосоциални фактори са показани като отделна категория в таблица 1 .
Потвърждение за функционална диспепсия
Потвърждението на диагнозата функционална диспепсия почива на:
Типичните симптоми и историята на пациента
Изключването на други заболявания на горната част на стомашно-чревния тракт и горните коремни органи, които могат да се проявят с подобни диспептични симптоми (1, 4, 6).
Типичните негастроинтестинални съпътстващи симптоми са общи вегетативни симптоми като повишено изпотяване, главоболие, нарушения на съня, мускулно напрежение, функционални сърдечни симптоми и раздразнителен пикочен мехур. При разпит пациентът обикновено съобщава за дълга история на оплакванията, променливи симптоми без ясна прогресия, дифузна болка с променливо местоположение, липса на неволно отслабване и зависимост на симптомите от стреса.
Единствените инструментални диагностични изследвания, за които се смята, че са достатъчно точни, са езофагогастродуоденоскопията, включително изследване за Helicobacter pylori и абдоминална ултрасонография, придружени при наличие на допълнителни симптоми на IBS чрез ендоскопска инспекция на дебелото черво. Тези изследвания са показани в случаите, когато медицинската история и симптомите са типични и предварителните лабораторни изследвания като кръвна картина, електролити и чернодробна и бъбречна функция, както и скоростта на утаяване на еритроцитите или CRP и, ако е приложимо, параметрите на периферната щитовидна жлеза са в нормалния диапазон (фигура 2) (1, 28).
- Инфекции на пикочните пътища (ИПП) при деца Симптоми, диагностика, лечение Ежедневието
- ИПП при деца Симптоми, причини, лечение и диагностика
- Какво е разстройство от преяждане Симптоми, причини, диагностика, лечение и профилактика Ежедневно здраве
- Рак на щитовидната жлеза - Видове, симптоми, лечение, стадиране; Диагностика MD Център за рак на Андерсън
- Какво е ректално кървене Симптоми, причини, диагностика, лечение и профилактика Ежедневно здраве