Елмар Айгнер
1 Първа медицинска катедра, Медицински университет Парацелз, Müllner Hauptstrasse 48, 5020 Залцбург, Австрия; Имейл: [email protected]
2 Отдел за изследване на затлъстяването, Медицински университет Парацелсус, Müllner Hauptstrasse 48, 5020 Залцбург, Австрия
Александра Фелдман
1 Първа медицинска катедра, Медицински университет Парацелз, Müllner Hauptstrasse 48, 5020 Залцбург, Австрия; Имейл: [email protected]
Кристиан Дац
2 Отдел за изследване на затлъстяването, Медицински университет Парацелсус, Müllner Hauptstrasse 48, 5020 Залцбург, Австрия
3 Отделение по вътрешни болести, Обща болница, Paracelsusstrasse 37, 5110 Оберндорф, Австрия
Резюме
Хомеостазата на желязото се влияе от затлъстяването и свързаната със затлъстяването инсулинова резистентност по многообразен начин. От една страна, дефицитът на желязо и анемията са чести открития при пациенти с прогресиращи стадии на затлъстяване. Това явление е добре проучено при затлъстели юноши, жени и субекти, подложени на бариатрична хирургия. От друга страна, хиперферитинемия с нормално или леко повишено насищане на трансферин се наблюдава при приблизително една трета от пациентите с метаболитен синдром (MetS) или неалкохолна мастна чернодробна болест (NAFLD). Това съзвездие е наречено „синдром на дисметаболитно претоварване с желязо (DIOS)“. Както повишените телесни запаси от желязо, така и дефицитът на желязо са вредни за здравето и за хода на състоянията, свързани със затлъстяването. Дефицитът на желязо и анемията могат да увредят хомеостазата на митохондриите и клетъчната енергия и допълнително да увеличат бездействието и умората на затлъстелите лица. Възпалението, свързано със затлъстяването, е тясно свързано с дефицита на желязо и включва нарушена абсорбция на дуоденално желязо, свързано с ниска експресия на дуоденален феропортин (FPN), заедно с повишени концентрации на хепцидин. Този преглед обобщава сегашното разбиране за дисрегулацията на желязната хомеостаза при затлъстяване.
1. Въведение
2. Патофизиологията на затлъстяването
Този параграф очертава важни патомеханизми на затлъстяването и свързаните с него състояния, особено тези, свързани с нарушената регулация на желязната хомеостаза.
Черният дроб, който е и ключовият регулатор на хомеостазата на желязото, при затлъстяване и IR се характеризира с липидно натрупване, наречено неалкохолна мастна чернодробна болест (NAFLD). Чернодробната стеатоза е предимно доброкачествена, но тежката форма на NAFLD, неалкохолен стеатохепатит (NASH), се характеризира с възпаление и фиброза и може да прогресира до цироза, краен стадий на чернодробно заболяване или хепатоцелуларен карцином при малка част от пациентите [14]. Повишена секреция на инсулин от панкреаса често се наблюдава при затлъстяване, за да компенсира развитието на тъканни IR, но в крайна сметка секреторната недостатъчност ще доведе до явен диабет тип 2.
3. Физиологията на метаболизма на желязото
През последното десетилетие бяха изяснени много аспекти на физиологичната регулация на човешката хомеостаза на желязото [15]. Желязото се абсорбира като Fe 2+ в проксималния дванадесетопръстник от двувалентния метален транспортер 1 (DMT1) [16]. След прехвърлянето му през дуоденалната базолатерална мембрана, улеснена от феропортина износител на желязо (FPN) [17], желязото се окислява от мембранно свързаната мед, съдържаща фероксидаза хефестин [18], преди да бъде включено в трансферина за по-нататъшен транспорт в обращение. Въпреки че хемът е важен източник на желязо от диетата и също така доставя желязо за нуждите на клетъчното желязо чрез повторно използване, механизмът за ентерално усвояване на хема все още не е идентифициран [19]. Повечето клетки придобиват желязо чрез поглъщане на свързано с трансферин желязо (Fe 3+) от трансфериновия рецептор (TfR1). Желязото се изисква главно за биосинтеза на хема в еритропоетичния костен мозък и други ензими, съдържащи хем (напр. Цитохроми), докато излишното желязо се съхранява в чернодробните хепатоцити. Желязото се изнася от хепатоцити, макрофаги и всички други клетки на бозайници чрез FPN, който досега е идентифициран като единственият износител на желязо [15].
Системната желязна хомеостаза се поддържа в хормоноподобен механизъм за отрицателна обратна връзка от 25-аминокиселинния пептиден хормон хепцидин (чернодробен бактерициден протеин) [20]. Хепцидин се секретира от хепатоцитите в отговор на претоварване с желязо, възпаление, хипоксия или анемия. Хепцидинът упражнява своите регулаторни функции върху хомеостазата на желязото чрез свързване с FPN, като по този начин води до FPN фосфорилиране, разграждане и следователно до блокиране на клетъчния износ на желязо, което предизвиква намаляване на серумното желязо [21]. Въпреки че в количествено изражение черният дроб е основният източник на циркулиращ хепцидин, макрофагите, островните клетки на панкреаса и мастната тъкан също могат да експресират хепцидин [22,23].
4. Железният фенотип на затлъстяването
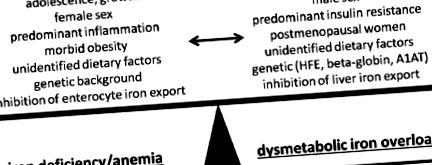
Изглежда противоречиво, че затлъстяването като условие за излишък на калории и хранителни вещества е свързано с ID. Дълбоките промени в енергийната хомеостаза в AT, черния дроб и други участващи органи са тясно свързани с отделни промени в хомеостазата на желязото. Дисрегулацията на желязото при затлъстяване може, по начина на римския бог Янус, да има две страни, обърнати в противоположни посоки. Данните от патофизиологичните проучвания категорично предполагат, че тези два различни клинични проблема всъщност са прояви на едни и същи основни механизми със свързан със затлъстяването дефицит на желязо от едната страна и DIOS от другата. Изглежда разумно да се предположи, че наблюдаваният фенотип на желязото накрая е резултат от нетния баланс на често конкуриращи се стимули. Фигура 1 представя обобщение на тези стимули, които изглежда са свързани с различен фенотип на хомеостаза на желязо при затлъстели и/или инсулиноустойчиви субекти.
Обобщение на потенциалните стимули и характеристики, които могат да повлияят на проявата на железния фенотип при затлъстяване. Както дефицитът на желязо, така и дисметаболитният синдром на претоварване с желязо представляват добре проучени прояви на неуредена хомеостаза на желязото. Нетният баланс на основните, често конкуриращи се стимули вероятно ще определи фенотипа на желязото при отделен пациент.
5. Клинични данни за дефицит на желязо, свързан със затлъстяването - юношество
По-ниски концентрации на серумно желязо с нарастващ ИТМ се наблюдават преди няколко десетилетия и се потвърждават в последващи изследвания [24,25,26]. Анализ от популацията на NHANES установи, че рискът за ID, дефиниран като ниско наситеност на трансферин и нисък серумен феритин, е два пъти по-висок при юноши с наднормено тегло в сравнение с юноши с нормално тегло [27], с подобни резултати от израелско население [28] . Сравними резултати са документирани в ирански и китайски разследвания [29,30]. По-нататъшно американско проучване установи силна връзка между ID и ИТМ при всички раси, възрасти и количества хранителен прием [31]. Тези проучвания недвусмислено демонстрират по-ниска наличност на серумно желязо с нарастваща AT маса при юноши. Освен това усвояването на желязо от дванадесетопръстника е ограничено при затлъстели в сравнение с деца с нормално тегло [32]. И обратно, проучване при предимно слаби или само леко наднормено тегло юноши без тежко затлъстяване е стигнало до извода, че по-високите серумни концентрации на феритин и наситеността на трансферин корелират с увеличаване на BMI квартилите - констатация, напомняща за асоциации, често отчитани при възрастни популации [33].
6. Зрелост
При възрастни няколко анализа показват по-ниски серумни концентрации на желязо с по-висок ИТМ, особено при жени. Резултатите обаче изглеждат много по-сложни при възрастни в сравнение с юноши. Следователно едно проучване съобщава за по-ниски серумни концентрации на желязо при жени с наднормено тегло, но няма разлики при мъжете [34]. В друго проучване не са документирани разлики в серумното желязо между затлъстяване и контрол на нормалното тегло [35]. При кохортите с болестно затлъстяване и бариатрична хирургия ID е идентифициран като типично и често състояние, както е описано по-долу [36].
Връзката между затлъстяването при възрастни и ниските запаси на желязо или анемията е оценена в скорошен мета-анализ на всички контролирани проучвания [37]. Въпреки че ID се явява типична находка при тежко затлъстяване, прегледът заключава, че повечето проучвания показват по-високи концентрации на хемоглобин и феритин при затлъстели лица в сравнение с възрастните с нормално тегло. Въпреки това, серумното насищане с желязо и трансферин намалява с увеличаване на ИТМ. Това се дължи главно на нарастващия ефект на свързаното със затлъстяването възпаление с нарастващи степени на затлъстяване.
В заключение, като се има предвид юношеството и зрелостта, може да се предположи, че повишеното търсене на желязо, поради физически растеж, увеличена мастна маса или обем на кръвта [27,38], заедно с намаленото усвояване на желязо при юношеското затлъстяване, може да обясни ясната категория асоциация на затлъстяването с дефицит на желязо в тази кохорта [28]. Тази връзка се губи през по-късните етапи от живота, напр. Жени в менопауза или инсулинорезистентни мъже и факторите, благоприятстващи натрупването на желязо, може дори да преобладават. Въпреки това, той остава актуален при изразени етапи на затлъстяване, като например кохорти с бариатрична хирургия или жени [39]. В тези кохорти менструалната загуба на желязо или изразеното AT възпаление може да наклони баланса към ID, докато това изглежда рядко откритие при мъжете, обобщено на фигура 1 .
7. Отговор на параметрите на желязото към намаляване на теглото
8. Уместност на ID за хода на затлъстяването
Данните са относително оскъдни по отношение на значението на ID за хода на затлъстяването. Няколко предположения за здравия разум обаче косвено се подкрепят от наблюдателни проучвания. ID и анемия могат да доведат до умора и по този начин до допълнително намаляване на физическата активност, допълнително влошаващо наддаването на тегло [45]. В допълнение, ID може да наруши митохондриалната активност на дихателната верига, като по този начин ограничи способността за упражнения и увеличи инсулиновата резистентност [26]. В подкрепа на тази редица доказателства беше демонстрирано подобрение на няколко метаболитни параметъра с корекция на ID [46].
9. Бариатрична хирургия и дефицит на желязо
Европейските насоки за бариатрична хирургия посочват, че бариатричната хирургия е показана, inter alia, при пациенти с ИТМ ≥ 40 kg/m 2 или ≥35 kg/m 2 със свързани със затлъстяването съпътстващи заболявания като метаболитни усложнения, кардиореспираторни или ставни заболявания [47] . Бариатричните операции се класифицират като рестриктивни или малабсорбционни. Roux-en Y стомашен байпас (RYGB), както и билиопанкреатична диверсия със или без дуоденален превключвател (BPD и BPD-DS), са комбинирани рестриктивни и малабсопторни процедури. Ограничителните операции включват гастректомия на ръкавите (SG), регулируема стомашна лента (AGB) и гастропластика с вертикална лента. Най-често извършваните методи са RYGB, AGB и SG [48]. Наскоро дуоденално-йеюнален байпасен ръкав (Endobarrier ®) беше въведен като нова, ендоскопски приложена възможност за лечение на затлъстяване и диабет тип 2 [49]. Към днешна дата не са провеждани изследвания върху промените в желязната хомеостаза при тези субекти.
Съгласно практическите насоки на Американското общество за метаболитна и бариатрична хирургия, състоянието на желязото трябва да се оценява при всяко последващо посещение след бариатрична хирургия. В случай на ID трябва да се осигури дневна доза от желязо от 150 до 200 mg чрез добавки. Освен това се препоръчва на пациентите с RYGB да получават 45 до 60 mg желязо дневно през първите шест месеца [62]. Въпреки това, според скорошно проучване на Gesquiere, пероралните добавки са недостатъчни за преодоляване на нарушената абсорбция след RYGB и поради това се препоръчва да се лекува тежък ID чрез парентерално заместване [63].
В обобщение, пациентите с бариатрична хирургия са изложени на висок риск да страдат от ID преди операцията. Малабсорбционните стратегии могат допълнително да доведат до ID, въпреки адаптивното регулиране на йеюналните транспортери на желязо, най-вероятно поради значителната загуба на абсорбираща повърхност [64,65]. След рестриктивна операция се наблюдава подобряване на функционалния статус на желязото при значителна част от пациентите, което изглежда е свързано със загуба на тегло и последователно подобряване на AT възпалението [39,66].
10. Механизми в основата на дефицита на желязо при затлъстяване
Централната находка на проучванията, изследващи хомеостазата на желязо при затлъстели лица, представлява нарушена способност за абсорбция на дуоденално желязо. Установена е забележимо по-ниска изотопно-белязана абсорбция на желязо при затлъстели в сравнение с лица с наднормено тегло и с нормално тегло със или без аскорбинова киселина [67]. Подобни наблюдения са докладвани при затлъстели мъже и деца от последващи разследвания [65,68]. По този начин, намаленото усвояване на желязо в храната поради по-ниската абсорбция на желязо в ентероцитите може да се разглежда като патофизиологичен белег на нарушената регулация на желязото при затлъстяване.
Съвременното разбиране на молекулярните връзки между затлъстяването и дефицита на желязо. Затлъстелата мастна тъкан се характеризира с повишено производство на няколко провъзпалителни цитокини и адипокини, за разлика от здравата постна мастна тъкан. Те могат директно да повлияят на абсорбцията на желязо от ентероцита. Освен това, противовъзпалителните цитокини като интерлевкин-1 и -6 представляват мощни индуктори на производството на хепцидин в черния дроб, което може допълнително да наруши абсорбцията на желязо. Както цитокините, така и хепцидинът водят до задържане на желязо в макрофагите на далака, черния дроб или костния мозък, като по този начин намаляват серумните концентрации на желязо и наличността на желязо за еритропоезата.
11. Заключения
Анормалните параметри на състоянието на желязо, показващи дефицит или претоварване с желязо, са чести открития при лица с наднормено тегло и затлъстяване. Недостигът на желязо представлява особен клиничен проблем през юношеството, когато нуждите от желязо са повишени, и при болестно затлъстяване през зряла възраст. Нарушеният функционален железен статус е свързан главно с възпаление на мастната тъкан и повишена експресия на системния железен регулаторен протеин хепцидин. Цитокините като TNF-α, IL-1 и IL-6 заедно с адипокини (лептин, резистин) или хепцидин могат да представляват сигнали от затлъстяване, възпалено AT, улесняващо промените във физиологичната желязна хомеостаза. Поради основния механизъм на нарушена абсорбция на желязо през червата, лечението на дефицит на желязо чрез перорално добавяне често е недостатъчно и поради това е необходимо парентерално заместване, особено при пациенти с бариатрична хирургия. Тъй като и дефицитът на желязо, и претоварването могат да имат вредно въздействие върху хода на състоянията, свързани със затлъстяването, усърден скрининг и лечение и на двете е оправдано.
Благодарности
Elmar Aigner се поддържа от PMU-Forschungsförderungsfonds (E-13/17/086-AIG). Подкрепата от SPAR Австрия на Christian Datz е признателна.
Принос на автора
Елмар Айгнер, Александра Фелдман, Кристиан Дац допринесоха за изготвянето и критичната ревизия на ръкописа и одобриха окончателната версия на ръкописа.
Конфликт на интереси
Никой от авторите няма потенциален финансов конфликт на интереси, който да декларира.
- Затлъстяването Нов рисков фактор за киселинността и газовете знайте повече
- Затлъстяването - рисков фактор или заболяване Какво могат да направят упражненията при затлъстели деца
- Затлъстяването като основен рисков фактор за рака
- Затлъстяването като цивилизационно заболяване и рисков фактор за рак на гърдата
- Затлъстяването като причинен рисков фактор за стеноза на аортния клапан на Американския колеж на