Има ли този пациент метаболитна ацидоза?
Метаболитната ацидоза обикновено се определя от наличието на ниска серумна концентрация на бикарбонат (нормален диапазон 22-28 mEq/L), въпреки че понякога могат да съществуват състояния, когато серумният бикарбонат е нормален с повишена анионна разлика (напр. Пациенти с лактатна ацидоза, които са получили инфузия на бикарбонат или пациенти на хемодиализа). По принцип метаболитната ацидоза се свързва с ниско рН на урината, но в зависимост от наличието или отсъствието на респираторна алкалоза, това може да бъде нормално или повишено. По този начин пациентът може да има ацидоза, но да не е киселинен.
Метаболитни ацидози се появяват, когато в плазмата има излишна киселина. В основното състояние тялото генерира около 12 000 до 13 000 mmol въглероден диоксид (CO2) и 1-1,5 mmol на килограм телесно тегло на нелетливи киселини. Тялото има голям буферен капацитет, като CO2-HCO3 е основната буферна система. Двата основни начина на екскреция на киселина са белите дробове (за CO2) и бъбреците (за нелетливи киселини)
Метаболитна ацидоза може да бъде причинена от три основни механизма: 1) повишено производство на киселина; 2) загуба на бикарбонат; и 3) намалено отделяне на бъбречна киселина
Повишеното производство на киселина води до метаболитна ацидоза с анионна междина (AG) и включва множество различни клинични процеси, виж Таблица 1. Ацидозата на анионната междина също може да доведе до поглъщане на киселинен товар.
Както загубата на бикарбонат, така и намалената екскреция на бъбречна киселина водят до метаболитна ацидоза с нормална анионна празнина (NG). Когато има загуба на HCO3, хлоридът се задържа, за да поддържа електрическа неутралност. Различните клинични процеси са обобщени в таблица 2.
Токсичното поглъщане е често срещана причина за метаболитна ацидоза на AG. Най-честите причини са интоксикацията с метанол и етиленгликол. Тези алкохоли се абсорбират бързо от стомашно-чревния тракт. Пиковите серумни нива обикновено се достигат в рамките на 1-2 часа. Непосредствено след поглъщането има голяма серумна осмоларна междина поради наличието на неизмерени, малки, незаредени молекули. Въпреки това, тъй като тези родителски алкохоли преминават през двуетапен метаболизъм (чрез алкохолна дехидрогеназа и алдехиддехидрогеназа), осмоларната празнина се решава, докато се развива ацидоза на анионната междина. Токсичността идва главно от техните метаболити.
Мравчената киселина е крайният метаболит на метанола, а гликолатът, глиоксилатът и оксалатът са крайни метаболити на етиленгликола. Те се натрупват и причиняват увреждане на крайните органи, след като алкохолът-майка достигне критично серумно ниво (
20 mg/dl). Въпреки това, поради бавния чернодробен метаболизъм, обикновено има латентен период от 24-48 часа, преди тези токсичности да се проявят, особено ако има едновременно поглъщане на алкохол (което конкурентно инхибира алкохолната дехидрогеназа). Ако не се започне лечение, може да настъпи трайно увреждане. Както метанолът, така и етилен гликолът се екскретират предимно чрез бъбреците, въпреки че белият дроб допринася за някаква степен на елиминиране на метанола.
Вдишването на толуен може да доведе както до AG, така и до NG метаболитна ацидоза. AG се причинява от метаболита на толуен, хипурова киселина. Хипуровата киселина обаче бързо се екскретира с урината и тъй като анионът е превишен, анионната междина пада с постоянна NG ацидоза. По принцип тези аниони се екскретират с калий и в резултат поглъщането на толуен може да доведе до изразена хипокалиемия.
5-оксопролинът е все по-призната причина за метаболитна ацидоза на АГ. Това е резултат от изчерпване на глутатиона. Това предотвратява инхибирането на обратната връзка на гама-глутамиловия цикъл и натрупването на оксопролин. Това води до метаболитна ацидоза на анионна празнина, но може също да причини NG ацидоза и хипокалиемия поради бързото бъбречно отделяне на аниона. Обикновено се наблюдава при пациенти с хроничен прием на високи дози ацетаминофен и особено въздейства на възрастните жени. Други рискови фактори включват сепсис, чернодробна и/или бъбречна дисфункция.
L-лактатната ацидоза се причинява или от свръхпроизводство на млечна киселина от тъканна хипоксия (тип А млечна ацидоза) или от недостатъчно използване на млечна киселина от дефицит на тиамин/чернодробни заболявания или от инхибиране на фосфорилирането на оксидатите, обикновено от лекарство (тип В лактатна ацидоза) Лактатна ацидоза тип А е най-често срещаната в клиничната практика и обикновено пациентите са хипотоници с очевидна лоша тъканна перфузия. Лекарствата, свързани с лактатна ацидоза тип В, включват метформин, фенформин, нуклеозидни инхибитори на обратната транскриптаза и пропофол.
D-лактатът е уникален, тъй като не се метаболизира от L-лактат дехидрогеназа при човека. Среща се при пациенти със синдром на късото черво. Когато тънкото черво се заобиколи, голямо количество въглехидрати се доставят в дебелото черво, където има изобилие от грам-положителни анаероби (например лактобацили). Въглехидратите се метаболизират в D-лактат, който след това се абсорбира. Тъй като D-лактатът не се измерва рутинно, когато се поръчва серумен лактат, той трябва да бъде изискан специално при съмнение за D-лактатна ацидоза
Кетоацидоза възниква, когато има повишено превръщане на мастни киселини в кетокиселини (ацетоацетат, β-хидроксибутират) при няколко патологични състояния, особено когато липсва инсулин. При диабетна кетоацидоза често се среща NG метаболитна ацидоза по-късно в хода поради бъбречната екскреция на кетокиселини. Това обяснява и тежкия дефицит на общ калий в тялото, който обикновено се наблюдава при тези пациенти.
Хроничното бъбречно заболяване с намалена бъбречна функция е честа причина за метаболитна ацидоза. В ранните фази с умерен функционален спад (етап 3 и ранен етап 4) бъбреците все още са в състояние да отделят органични киселини, поради което АГ ацидозата не е често срещана. Пациентите обикновено проявяват NG метаболитна ацидоза поради намалена екскреция на амоний. След като бъбречната функция спадне до критично ниво, обикновено в края на етап 4, киселините от протеиновия метаболизъм се задържат, което води до метаболитна ацидоза на AG.
Има три основни типа бъбречна тубулна ацидоза (RTA): 1) тип 1 (дистална, RTA-1); 2) тип 2 (проксимален, RTA-2) и 3) тип 4 (дистален от ниска устойчивост на алдостерон или алдостерон, RTA-4). RTA-1 е резултат от дефект в дисталната екскреция на тубулна киселина в резултат на намалена секреция на H + или обратно изтичане на секретиран водород. То може да бъде тежко и да доведе до прогресивна загуба на HCO3 (серумна концентрация
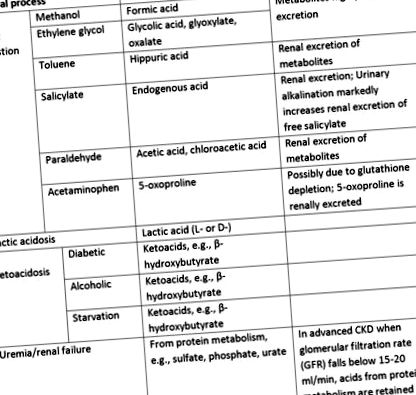
маса 1.
Диференциална диагноза на метаболитна ацидоза на AG
Таблица 2.
Диференциална диагноза на NG метаболитна ацидоза
Таблица 3.
Какви тестове да извършите?
Първо, измервайте артериалното pH, PCO2 и серумната концентрация на бикарбонат.
Когато е налице ниско съдържание на бикарбонат, анионната междина трябва да се провери, за да се определи дали това е празнина, непукнатина или смесено разстройство. PCO2 ще помогне да се определи дали има насложена респираторна ацидоза или алкалоза. Това може да се установи чрез изчисляване дали степента на дихателна компенсация е подходяща (Таблица 4).
Серум AG = серум Na - серум (Cl + HCO3). Анионната междина е конструкция, която наистина не съществува (електронеутралността винаги се поддържа) и представлява разликата между често измервания анион (Na) и катиони (HCO3 и Cl). По този начин, анионната празнина може да се промени или поради увеличаване на неизмерените аниони, или поради промяна в относителните количества хлорид и бикарбонат. За изчисления се използва измереният, а не коригираният серумен натрий. AG се състои предимно от отрицателни заряди върху серумните протеини, предимно албумин. Нормалният серумен AG варира от 8 до 12 meq/L, но варира в различните лаборатории. Важно е да се отбележи, че промените в серумната концентрация на албумин влияят върху AG и затова изчислената AG трябва да бъде коригирана за концентрацията на албумин. AG обикновено намалява с 2,5 meq/L за всеки 1 g/dl намаляване на серумния албумин под 4 g/dl.
При сложни смесени киселинно-алкални нарушения метаболитната ацидоза може да бъде по-малко очевидна. Важно е първо да се установи първичното киселинно-алкално разстройство, след което да се провери компенсаторната реакция, за да се оцени насложените киселинно-алкални разстройства (вж. Таблица 4).
За допълнителна оценка на метаболитната ацидоза, определете делта AG (ΔAG). ΔAG = AG (измерено) -AG (нормално). Ако ΔAG + серумен HCO3 28, тогава има и метаболитна алкалоза.
Ако се установи AG метаболитна ацидоза, трябва да се наредят допълнителни тестове за определяне на причините въз основа на историята и физическите находки.
Диагнозата D-лактатна ацидоза трябва да се поставя при пациенти със синдром на късото черво. Тези пациенти се срещат с AG ацидоза, отрицателни кетони и нормално ниво на серумен лактат чрез рутинно тестване на лактат. Диагнозата е вероятна, ако ацидозата се влоши при перорален прием. Изисква специално тестване за D-лактат.
Тъй като алкохолът забавя метаболизма на метанола и етилен гликола, AG ацидоза може да не е налице при пациенти, които поглъщат значително количество алкохол. В такива случаи повишената серумна осмоларна междина може да бъде полезна за установяване на диагнозата. Анализът на урината може да даде важна улика за наличието на етилен гликол. Кристалите на калциев оксалат са често срещани в урината (макар и неспецифични), ако е погълнато достатъчно етилен гликол. Окончателният тест за диагностициране на токсично поглъщане е измерването на нивата на токсина в серума. Въпреки това, тестът може да не е лесно достъпен, когато има нужда от спешно вземане на решение.
За NG метаболитна ацидоза, пикочната AG често се използва за разграничаване на бъбречните и извънбъбречните загуби на HCO3. AG в урината = урина (Na + K -Cl). Първичният неизмерен анион е амоний и в условията на метаболитна ацидоза с небъбречен произход трябва да има значително увеличение на екскрецията на амоний, която се екскретира с хлорид и по този начин води до отрицателна празнина на анион в урината. Положителната празнина в аниона в урината предполага, че има недостатъчно производство на амоний и предполага наличието на дистална RTA. Изключение от това обаче би било, когато има свободно филтриран анион, който причинява ацидозата (напр. Хипурат или кетокиселини), тъй като те ще се отделят с урината с амоний и по този начин разликата може да бъде положителна въпреки наличието на голям количество екскреция на киселина.
За да се направи разлика между различните видове RTA, както pH на урината, така и серум K са полезни. Алкална урина, хипокалиемия и хиперкалциурия с данни за образуване на камъни в бъбреците предполагат RTA тип 1, докато относителната кисела урина с хиперкалиемия предполага RTA тип 4. В допълнение, ацидозата при RTA тип 1 обикновено е тежка в сравнение с тези от тип 2 и 4.
След като NG метаболитна ацидоза бъде потвърдена, допълнителни тестове ще се основават на предполагаемите диагнози. Рентгенологичното изобразяване има ограничена роля при острото управление на метаболитна ацидоза, освен в редки случаи, изобразяването може да бъде полезно за установяване на тъканна/органна исхемия, нефрокалциноза и други процеси, свързани с конкретно киселинно-алкално разстройство.
Таблица 4.
Как трябва да се управляват пациентите с метаболитна ацидоза?
РН 10 meq/L => VOD = 0,5 x BW; ако серумен HCO3 между 5-10 meq/L => VOD = 0.75 x BW; ако серумен HCO3 VOD = 1 x BW. Дефицит на HCO3 на литър = целево ниво на HCO3 - първоначално серумно ниво на HCO3.
Интравенозният NaHCO3 се предлага като 8,4% разтвор. За да се приложи изотоничен разтвор, три ампера (150 ml) NaHCO3 се смесват с 1 литър D5W, за да се получи
150 meq/L NaHCO3. Перорален NaHCO3: една таблетка (650 mg) осигурява
Използването на бикарбонатна терапия за метаболитна ацидоза е противоречиво поради липсата на доказани ползи, както и редица потенциални усложнения, включително: 1) генериране на CO2, водещо до влошаване на вътреклетъчната ацидоза; 2) намаляване на йонизирания серумен калций, тъй като Ca и H + се конкурират за свързване с албумин. Бързото повишаване на pH може да доведе до повече свързване на Ca с албумин и намаляване на йонизирания Ca; и 3) обемно претоварване.
Употребата на бикарбонат в случаи на органична ацидоза (напр. Кетоацидоза и L-лактатна ацидоза) също е противоречива. При пациенти с тежка ацидоза (рН 50 mg/dl. Трябва да се отбележи, че тиаминът и пиридоксинът са използвани при интоксикация с етиленгликол, тъй като те участват в алтернативни пътища за елиминиране на глиоксилат. Към днешна дата няма данни, които да доказват тяхната ефикасност.
Тъй като отделянето на салицилат с урината може значително да се увеличи с алкална урина, често срещана практика е да се предизвика алкална диуреза. NaHCO3 iv (150 mmol, смесен в 1 литър D5W) се използва за повишаване на рН на урината до 7,5 или повече. Обикновено се инициира скорост от 0,5 mmol/kg/час и се титрира до целевото рН на урината. Важно е да се добави KCl (обикновено започва от 40 meq iv), тъй като изчерпването на калий в организма неизменно е налице и може да бъде маскирано от ацидоза.
- Относно водата в тялото - Хормонални и метаболитни нарушения - Ръководства на Merck Потребителска версия
- Откритото първенство на Австралия Алекс Зверев се шегува, че не носи синглетите в стил Рафаел Надал Sporting News
- Agata muceniece бързо отслабване; Новини за знаменитости
- Agata muceniece - биография, личен живот, снимки, филми, Пол Прилучни и последните новини
- Синьо-зелени водорасли - Consumer Health News HealthDay