С Мастронарди
1 Училище за медицински изследвания Джон Къртин, Австралийски национален университет, Канбера, ACT, Австралия
G J Paz-Filho
1 Училище за медицински изследвания Джон Къртин, Австралийски национален университет, Канбера, ACT, Австралия
Е Валдес
2 Медицински факултет на Университета в Маями, Маями, Флорида, САЩ
J Maestre-Mesa
2 Медицински факултет на Университета в Маями, Маями, Флорида, САЩ
J Licinio
1 Училище за медицински изследвания Джон Къртин, Австралийски национален университет, Канбера, ACT, Австралия
M-L Wong
1 Училище за медицински изследвания Джон Къртин, Австралийски национален университет, Канбера, ACT, Австралия
Резюме
Въведение
Основното депресивно разстройство (MDD) е сериозен проблем за общественото здраве. Понастоящем точковото разпространение на MDD е ∼4–7%, а оценката на разпространението през целия живот варира от 15 до 20%. 1, 2 MDD е водещата причина за инвалидност, измерена в години, загубени поради инвалидност, и най-голямата единична причина за нефатална тежест на болестта в Австралия. 3 Той ще се превърне във втория водещ фактор за глобалната тежест на болестите до 2020 г. (година на живот, коригирана към уврежданията). 4 Приблизително 59% от хората с MDD търсят помощ за своето състояние, а 35% получават лекарства или психологическо лечение. 3 Според здравното проучване на канадската общност, разпространението на употребата на антидепресанти за период от 12 месеца между 2001 и 2002 г. се оценява на 5,8%. 5
MDD е често срещано сложно разстройство, което засяга ∼121 милиона души по целия свят. В САЩ икономическата тежест на MDD е от порядъка на 100 милиарда долара годишно, като разходите на работното място са най-големият компонент. 6 Дозирането на антидепресанти се е увеличило значително през последните две десетилетия в западните страни. В Съединените щати антидепресантите се предписват на 27 милиона души и те са най-често предписваният клас лекарства. 7, 8 В Обединеното кралство, Франция и Австралия рецептите за антидепресанти са се увеличили значително от началото на 90-те години с навлизането на селективните инхибитори на обратното поемане на серотонин (SSRI) на пазара. 9, 10, 11
Проучванията, изследващи наддаването на тегло по време на дългосрочно лечение със SSRI, показват несъвместими резултати. Резултатите от голямо проучване с напречно сечение, базирано на базата данни на General Electric Medical Records на пациенти с MDD, лекувани с монотерапия с антидепресанти в продължение на поне 1 година, предполагат разлики в дела на пациентите, които са спечелили поне 7% от телесното си тегло (BW) по време на лечението. Най-високият процент от пациентите с наддаване на тегло е свързан с миртазапин (26%), последван от SSRIs (16–19%). 12 Лечението с антидепресанти може да бъде ефективно при MDD, но съответствието е ниско: в голямо европейско проучване на 7525 пациенти 56% са изоставили лечението в рамките на 4 месеца. 13
Общоприето е, че страничните ефекти като увеличаване на теглото могат да повлияят неблагоприятно на придържането към терапията, но според Bulloch и Patten, 5 основната причина за неспазването е забравянето (74,5% от отговорилите), последвано от „чувствах се по-добре“ ( 10,7%); като четвърта причина са докладвани нежелани реакции (5,9%). Обикновено се твърди, че пациентите се връщат към предишното си тегло, след като спрат да приемат антидепресанти, но това предположение не се основава на доказателства.
За да се усложнят нещата, клиничните данни и теглото на животните по време на лечението с антидепресанти са трудни за интегриране, защото изглежда, че поддържат различни ефекти; голямо количество изследвания потвърждават, че прилагането на няколко антидепресанти води до неуспех при напълняване или „парадоксална“ загуба на тегло при плъхове, особено при високи дози. 14, 15 Следователно, парадигмите на животните, които помагат да се запълнят някои от тези пропуски, биха могли значително да разширят нашето разбиране за интерфейса между затлъстяването и MDD. Съществува силна част от транслационната работа, която използва гризачи за изучаване на биологията на депресията и антидепресантите. Тези проучвания показват, че механизмът на действие на антидепресантите е да стимулира неврогенезата в хипокампуса на възрастни плъхове. 16 Животните модели на депресия включват парадигми на стреса (като неконтролируем стрес, хроничен лек стрес и повтарящ се стрес стрес (RRS)), за които е доказано, че намаляват клетъчната пролиферация в хипокампуса, а прилагането на антидепресанти може да блокира това понижаване на клетъчната пролиферация. 17
Употребата на антидепресанти нараства драстично от края на 80-те години с появата на селективните инхибитори на обратното захващане на моноамините. 27 Огромният брой хора са изложени на антидепресанти краткосрочно, тъй като обикновено не се постига дългосрочно съответствие. 3, 5 Такова повишено излагане дори на кратки курсове на антидепресанти временно съвпада с възникващата епидемия от затлъстяване, пред която са изправени развитите страни. Може ли настоящото драстично нарастване на затлъстяването да се отдаде поне отчасти на излагането на антидепресанти? По-рано е демонстрирано, че ефектите на лекарствата могат да продължат да се увеличават с течение на времето, дори след еднократна доза и тъй като нивата на лекарствата намаляват: това интригуващо явление е известно като зависима от времето сенсибилизация (TDS). 18.
Ние предположихме, че TDS, който е описан по време на краткосрочно лечение с антидепресанти, може да се прилага за регулиране на теглото след излагане на антидепресанти. За да проверим тази хипотеза, разработихме парадигма за животни, която съчетава RRS и поведенчески ефективно, краткосрочно антидепресантно лечение, последвано от дългосрочна диета с високо съдържание на мазнини. Това имитира клинична ситуация, преживяна от милиони хора: стресът/депресията са свързани с краткотрайно излагане на антидепресанти и с дългосрочно поглъщане на диети с високо съдържание на мазнини. В такава парадигма тествахме конкретната хипотеза, че дори краткосрочната експозиция на антидепресанти представлява дългосрочен рисков фактор за затлъстяване, проявяващ се продължително, когато е маскиран от фактори на околната среда, като диета с високо съдържание на мазнини.
Материали и методи
Животни
Всички процедури бяха извършени съгласно установените насоки за хуманна грижа и използване на плъхове и бяха одобрени от Институционалния комитет по грижа и употреба на животните в Университета в Маями и от Комитета по етика на Австралийския национален университет. При пристигането, млади възрастни мъжки плъхове Sprague-Dawley без вируси и антитела (Harlan, Indianapolis, IN, USA) бяха настанени при 24 ° C и 12 часа светлина/тъмно (светлините са включени от 0600 до 1800 h) в стрес -безплатна среда и разделена на две проучвания: (1) хронично лечение с антидепресанти и (2) стрес, антидепресант и диета (оттук нататък, проучване за диета срещу стрес-антидепресант).
Проучване за лечение на хроничен антидепресант
Младите растящи плъхове (150–200 g) бяха настанени по двама в клетка в среда без стрес за поне 5 дни преди започване на експерименталните процедури. Плъховете бяха разпределени на случаен принцип в две експериментални групи: контролна (0.9% физиологичен разтвор; Hospira, Lake Forest, IL, САЩ), n = 10 и флуоксетин 10 mg (SSRI, Sigma-Aldrich, St Louis, MO, USA), n = 10 . Животните са получавали ежедневно 0,5 ml интраперитонеални инжекции от 0,9% физиологичен разтвор или 10,0 mg флуоксетин, разтворени в 0,9% физиологичен разтвор, в продължение на 5 седмици. Дозата и продължителността на лечението се основават на предишни доклади. Ежеседмично се измерва 19, 20, 21 BW.
Стрес-антидепресант-диета проучване
Плъховете (200–230 g) бяха настанени по един на клетка (11 ″ широки × 8,5 ″ високи × 14,5 ″ дълги). Приемът на храна (FI) и BW се измерват няколко пъти седмично, започвайки един ден след пристигането (експериментален ден 1). Плъховете получиха свободен достъп до храна и вода, освен по време на сесиите на RRS. Този експеримент продължи 177 дни.
Плъховете бяха разпределени на случаен принцип в две основни групи: (1) група с неограничен контрол (не-RRS) (n = 26) и (2) група с ограничена функция (RRS) (n = 38). Животните от групата, която не е от RRS, не са инжектирани или задържани и тази група включва две подгрупи: (i) NR-CC (n = 13), включваща животни, които не са RRS, хранени с редовна чау-диета през целия експеримент; и (ii) NR-CF (n = 13), включващ животни, които не са RRS, хранени с диета чау до ден 11 и след това хранени с коригирана мастна диета (TD95217; Harlan, Saint Louis, MO, USA).
Животните от RRS групата са били подложени на RRS, както е описано по-долу, и са получили коригирана мастна диета (TD95217; Harlan) след ден 11. Групата RSS включва две подгрупи: (i) RC група (n = 13), включваща RRS животни, които са получили веднъж дневно интраперитонеално инжектиране на 0,5 ml физиологичен разтвор (0,9% NaCl; Hospira); и (ii) R-AD група (n = 25), включваща RRS плюс третирани с антидепресанти животни, получаващи ежедневна интраперитонеална инжекция на антидепресанти в продължение на 7 дни по време на RRS периода. Тези животни са получили имипрамин (Sigma-Aldrich) 10 mg kg –1 (R-IMI, n = 13) или флуоксетин (Sigma-Aldrich) 10 mg kg –1 (R-FLX, n = 12).
Повтарящ се стягащ стрес
Използвахме прозрачни акрилни ограничители с плоско дъно (20,3 × 8,3 см) (Кат. № 544-RR; Plas Labs, Lansing, MI, САЩ). RRS сесиите се проведоха през периода от 0900 до 1600 часа и продължиха по 6 часа; те са се появили 7 последователни дни (дни 5–11).
BW и FI
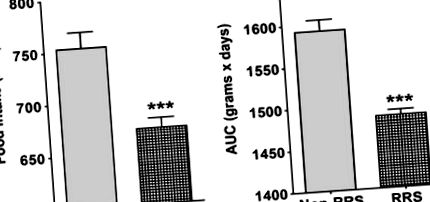
По време на RRS периода, BW и FI се измерват ежедневно при всички животни; BW печалбата се изчислява като площта под BW кривата за не-RRS (n = 26) или RSS (n = 38) групи между дни 5 и 11 (Фигура 2b). След периода на задържане, BW и FI се записват три пъти седмично до края на изследването на ден 177.
Взаимодействия с повтарящ се ограничителен стрес (RRS) и краткосрочно лечение с антидепресанти върху приема на храна и телесно тегло по време на RRS сесиите. (а) Кумулативен абсолютен прием (kcal) по време на периода на задържане (5-11 дни) при не-RRS (n = 26) и RRS плъхове (n = 38); през този период всички животни са били хранени с редовно чау. Не-RRS консумират по-голямо количество ккал. (б) Увеличаването на телесното тегло се изчислява чрез получаване на площта под кривата на теглото (AUC, g × ден) по време на периода на задържане. Животните извън RRS са по-тежки от тези на RRS. *** P –1 за обикновената чау-чау и 4.3 kcal g –1 за коригираната мастна диета). Средният кумулативен калориен прием се изчислява отделно за периода на ограничение за групите, които не са RRS и RRS. Кумулативният прием през периода след ограничението (между 12 и 177 ден) е начертан като функция от времето за двете основни групи с ограничение, а именно R-C и R-AD.
Ежедневен калориен прием: Дневният калориен прием е изчислен между 133 и 163 дни, период, включващ общо 14 периода. Индивидуалните приращения на FI се превръщат в дневен калориен прием чрез разделяне на общото количество калории, определено между две последователни измервания на дневния интервал (2 или 3 дни). Тези индивидуални стойности на калориен прием са осреднени за всеки период за всяка експериментална група (R-C и R-AD).
Линеен растеж, мастна маса и поведение
Дължината на тялото и костите и двигателната активност бяха определени при подгрупа плъхове (R-C, n = 5; R-IMI, n = 5; и R-FXT, n = 4).
Измервания на тялото: Ано-назалната дължина се определя седмично (четири пъти) между 133 и 150 дни.
Измервания на костите: В края на проучването (ден 177) плъховете бяха евтаназирани и левите им задни крака също бяха дисектирани и нагрявани в продължение на 2 часа при 80 ° C в разтвор, съдържащ 3 ml амонячен разтвор (7 N в метанол) и 25 мл вода за улесняване на костната дисекция. Дължините на разчленени бедрени кости и пищяли са измерени с шублер.
Мастна маса: В края на проучването (ден 177) плъховете бяха евтаназирани и епидидималните мастни накладки бяха дисектирани и получени свежи тегла.
Локомоторна активност: По време на периода след задържане (14–67 дни), подмножество плъхове (RC, n = 5 и R-AD, n = 9) бяха представени на 7 седмични 60-минутни сесии на открито (между 1400 и 1600 ч). Животните бяха поставени индивидуално в прозрачни акрилни кутии (40,64 × 40,64 cm), оборудвани с монитори за активност Digiscan (Omnitech Electronics, Columbus, OH, USA) с инфрачервени светлочувствителни детектори, разположени на 2,5 cm на две перпендикулярни стени. По протежение на противоположната стена бяха разположени инфрачервени светлинни лъчи, насочени към детекторите. Регистрира се един брой хоризонтални активности всеки път, когато животното засече лъча. Общото разстояние (TD) беше получено като отчитане на хоризонталната активност, а централното разстояние (CD) беше получено като отчитане на хоризонталната активност в центъра на кутията. Във всяка сесия TD, CD и съотношението CD/TD, използвани като индекс на тревожност, бяха изчислени за R-C и R-AD групите. Впоследствие техните средства бяха осреднени през седемте сесии.
Статистически анализ
Диета с мазнини
Коригираната диета с мазнини е започнала на 11-ия ден на изследването и е причинила по-тежки животни (NR-CF) от тези, които получават редовно чау (NR-CC) (съответно 503,0 ± 8,5 и 477,4 ± 6,5 g, P = 0,025).
Период на възстановяване след стрес
Измервания на мастната тъкан на епидидима: Както се очаква, диетата с мазнини увеличава общото съдържание на телесни мазнини, измерена чрез прясното тегло на мастните подложки на епидидима (12,6 ± 0,7 g за NR-FC и 7,4 ± 1,0 g за NR-CC, P = 0,001) и епидидима съотношения мастна тъкан/BW (23,3 ± 0,9 × 10 –3 за NR-FC и 14,9 ± 1,8 × 10 –3 за NR-CC, P = 0,0003), но тези параметри не се различават съществено между стресираните и нестресираните животни ( 12,8 ± 0,7 g за RRS и 11,9 ± 1,7 g за не-RRS, P = 0,53; 23,4 ± 0,9 × 10 –3 за RRS и 22,8 ± 2,4 × 10 –3 за не-RRS, P = 0,8).
Нашите данни показват, че лечението с антидепресанти има сложен ефект върху регулирането на BW в зависимост от факторите на околната среда. При стандартни лабораторни условия и диета, нестресираните плъхове, получаващи хронично лечение с флуоксетин, тежат по-малко от третираните с физиологичен разтвор контроли, което е съвместимо с литературата. 15 В нашето проучване на диета срещу стрес-антидепресанти, животните, подадени на RRS, консумират по-малко калории и са по-леки по време на стресовия период.
Това, което се съобщава тук като ново откритие, е, че животните, на които е била дадена мастна диета след края на стресовия период, са постигнали пълно възстановяване на теглото: теглото на нетретираните животни (RC, контролна група с физиологичен разтвор) не се различава значително от тези на нестресираните животни, приемащи мазнини (NR-CF). За разлика от това, нелекуваните плъхове, получаващи редовно чау, може да не възстановят загуба на тегло, причинена от сдържаност. 29 RSS животни, получили антидепресантно лечение (R-AD), са имали поведенчески прояви на антидепресантно действие, както е документирано от намалено поведение, което се дължи на стреса и безпокойството на открито. Нашето най-забележително и ново откритие беше, че когато комбинацията от стрес и краткосрочно лечение с антидепресанти беше последвана от дългосрочна диета с високо съдържание на мазнини, след като антидепресантите бяха прекратени (Фигури 1а и б), животните наддават по-голяма тежест в сравнение с плъховете, подадени на същата парадигма, но никога не е изложен на антидепресанти (RC). Тъй като нашите открити данни не подкрепят намаляване на двигателната активност в групата, изложена на антидепресанти (Фигура 4), малкото, но значително увеличение на теглото при тези животни може да се обясни с малкия им, но значително по-висок калориен прием в сравнение със стресираните животни, които не са изложени на антидепресанти.
Това проучване предполага, че „парадоксалният“ ефект на лечението с антидепресанти при BW при хора в сравнение с гризачите може да се обясни с опростената експериментална парадигма, обикновено използвана при гризачи, която не отчита фактори на околната среда, като стрес и диета, или значимо дълъг период на проследяване. Тук показваме, че включването на фактори на околната среда след лечение с антидепресанти може да предизвика дългосрочно наддаване на тегло при гризачи; следователно обяснението по подразбиране, че разликите в метаболитните и невроендокринните пътища, регулиращи апетита и енергийния метаболизъм, са необходими, за да се обясни несъответствието на антидепресантните ефекти при BW между хора и гризачи 14, трябва да бъде преразгледано и тъй като такива разлики в действителност могат да бъдат малки или не съществуващ.
Като се има предвид, че несъответствието с лечението с антидепресанти изглежда високо сред общата популация (> 50%), 13 нашите данни подчертават необходимостта да се изследва дали тези лекарства имат ефекти върху регулирането на BW, които продължават дългосрочно след прекратяването им. Тревожно е, че SSRI лекарствата са станали толкова популярни, че вече са наричани лекарства за „начин на живот“. 36, 37 В Съединените щати процентите на затлъстяване започват да се увеличават значително в края на 80-те години, което съвпада временно с въвеждането на SSRI. Годишното увеличение на процентите на дозиране на антидепресанти 7 изглежда успоредно с увеличаването на процентите на затлъстяване; 38 обаче са необходими подробни анализи на тези тенденции на ниво популация, за да се установи клинична асоциация.
В заключение тук предлагаме, че лечението с антидепресанти, възникващо в контекста на висок стрес и прием на мазнини, може да е скрит, коварен и дълготраен принос за наддаването на тегло, дори след като антидепресантите са спрени за дълго време, което е съвместимо с феномена TDS. Необходими са допълнителни изследвания, за да се разберат пътищата и патофизиологичните механизми, участващи във взаимодействията между фармакологията и околната среда, които са в основата на продължителните ефекти на антидепресантите върху приема на калории и размера на тялото и теглото. Бъдещите проучвания също трябва да разгледат ролята на стреса и диетите с високо съдържание на мазнини върху дългосрочните резултати от BW по време и след лечение с антидепресанти в клинични условия. Би било особено важно да се разбере дали дълготрайното нарастване на телесното тегло се наблюдава и при животни, хранени с различни диети, след излагане на стрес и ограничено във времето лечение с антидепресанти.
Благодарности
Това изследване беше подкрепено отчасти от Националния здравен институт Grant K24RR017365 за MLW и от институционални средства от Университета в Маями и Австралийския национален университет. Финансистите не са играли роля в дизайна на проучването, събирането и анализа на данни, решението за публикуване или подготовката на ръкописа. Благодарим на д-р Сари Изенвасер за нейната безценна помощ при поведенчески експерименти и настройка.
Бележки
Авторите не декларират конфликт на интереси.
- Дългосрочни асоциации на консумацията на ядки с телесно тегло и затлъстяване
- Лираглутид (Отслабване) Подкожно приложение, странични ефекти, взаимодействия, снимки, предупреждения; Дозиране
- Джой-Анна Дъгър разкрива тайната за отслабване след достигане на целите на тялото след бебето Новини
- Медицински Отслабване Д-р Дел Кастило Браунсвил Дългосрочни резултати
- Влияние на телесното тегло и загубата на тегло върху бионаличността на лекарствата, сърдечно-съдови рискови фактори и