РЕЗЮМЕ:
Въпреки постигнатия напредък в разбирането на биологията на аутистичния спектър (ASD), ефективните биологични интервенции за основните симптоми остават неуловими. Поради етиологичната хетерогенност на ASD, идентифицирането на подход за „универсален подход за лечение“ вероятно ще продължи да бъде предизвикателство. Свикана е среща в Университета на Мисури и Центъра Томпсън, за да се обсъдят стратегии за стратификация на пациентите с ASD с цел преминаване към прецизна медицина. Представената тук „бяла книга“ формулира предизвикателствата и предлага предложения за бъдещи решения.
КОМПЛЕКСИ НА АВТИЗМНОТО НАРУШЕНИЕ НА СПЕКТРА
Разстройството от аутистичния спектър може също да бъде свързано с редица съпътстващи медицински и/или психиатрични състояния, включително припадъци, стомашно-чревни състояния, нарушения на съня, агресивно поведение, симптоми на тревожност и дефицити на внимание. Тези състояния могат или не могат да бъдат свързани с когнитивно увреждане. Едно скорошно проучване също така включва съпътстващи се медицински и биологични променливи при генерирането на управлявани от данни фенотипни клъстери, разкриващи клъстери за (1) циркадна и сензорна дисфункция, (2) имунни аномалии, (3) невроразвиващо забавяне и (4) стереотипни поведения в един анализ на свързани с ASD характеристики. 12 Въпреки че най-добрият курс на лечение е ясен за някои от тези състояния (т.е. лечение на гърчове с антиепилептични лекарства), не е известно как тези различни съпътстващи се фенотипни аспекти могат да бъдат свързани с потенциалното целенасочено лечение на основните характеристики.
КАКВО Е "BIOMARKER"? СА ЛИ БИОМАРКЕРИТЕ ЗА ПОВЕДЕНСКО СЪСТОЯНИЕ ТАКВО, КАКТО ASD ОПРЕДЕЛЯ СЪЩИЯ НАЧИН, КАТО ТЕЗИ ЗА БОЛЕСТ, КАТО РАК?
Инициативата за критерии за изследване на домейни (RDoC) в Националния институт за психично здраве 38 е насочена към специфични домейни като подход към изследване на редица психични разстройства, което е важно съображение в светлината на подчертаната хетерогенност на ASD. Той предлага използването на насочване към домейни на симптомите, вместо да се фокусира върху насочване към диагноза, която представлява съзвездие от симптоми. При ASD ще бъде важно да се определи как тежестта на специфичните симптоми се косегрегира с наличието на генетични или негенетични биомаркери, включително анатомични и функционални показатели за промени в нервните системи, като същевременно се отчита съответното въздействие на траекторията на развитието, за да се улесни най-добре специфични за симптомите индивидуални подходи за лечение. Въпреки че предишната работа, описана в предишния раздел, е изследвала връзката между генетиката и клиничните маркери, 17,19,28,29 включване на други молекулярни данни (напр. Транскриптоми 39) също ще трябва да се разгледа.
В допълнение към гените, кодиращи протеини, некодиращите РНК също могат да играят роля в причината за ASD, както е показано от нарушена регулация на микроРНК при ASD. 40–44 Неотдавнашно изследване за асоцииране в целия геном (GWAS) идентифицира значителна асоциация с единичен нуклеотиден полиморфизъм, който не е локализиран в кодиращата област, а по-скоро се намира в некодираща РНК, която е антисенс инхибитор на гена за мизин, протеин който регулира невронната архитектура. 45 Това откритие демонстрира потенциалния принос на некодиращата РНК в риска от ASD. Освен това са съобщени доказателства за конвергенция на молекулярните пътища при алтернативно сплайсинг 46,47 и ниво транскриптом 48, а значението на експресията на иРНК се подчертава все повече през последните години. 32,33,49 Други епигенетични маркери също са идентифицирани във връзка с ASD. 50,51
Като цяло ролята на ДНК метилирането, хистоновото ацетилиране и микроРНК маркерите в ASD понастоящем са по-слабо разбрани. Тези проблеми обаче стават все по-важни в други области на медицината, като например при лечението на рак. С много различни видове рак, скорошни изследвания разкриха значението, което биомаркерите играят при оптимизирането на подходите за лечение. Моделите на метилиране на ДНК са предсказали кой е най-вероятно да реагира на определени терапии с глиобластом, 52 и е широко известно, че хормоналните маркери предсказват отговора на хормоналната терапия при рак на гърдата. 53 Следователно свързаните подходи могат да станат все по-важни при ASD.
Особено внимание трябва да се обърне и на биомаркери, които имат съответна функция или връзка с невронни системи, отговорни за експресията на определен фенотип (и) по време на специфични епохи на развитие. Например, определени синапси или регионални вериги могат да бъдат възбуждащи по време на една фаза на развитие, но инхибиторни през друга епоха. Тази синаптична физиология може да повлияе различно на експресията на даден фенотип или биомаркер по време на специфични периоди на развитие. Аномалии в глутаматергичната и GABAergic система са наблюдавани с известна последователност при ASD при мозъчни изследвания след смъртта, 54-56 и in vivo, при регионални находки от магнитно-резонансната спектроскопия (MRS), 57,58 или когато се изразява като съотношение на GABA към глутамат с MRS. 59 Възможно е също да има потенциал за периферни измервания. 60 Мутации, засягащи GABAergic системата, също са свързани с ASD. 61,62 Тъй като последните големи клинични проучвания се опитват да насочат към глутаматергични (мемантин) и GABAergic (арбаклофен) системи, 5 маркера, представляващи активност в тези системи, както се оценява от MRS или други прокси маркери като ЕЕГ активност на гама лента, 63 би изглеждало силно от значение.
Други маркери, които могат да бъдат от значение за лечението, могат да включват имунни маркери, които често са нетипични при ASD, 64,65 пълнокръвен серотонин, 66,67 генетични полиморфизми, които влияят на серотонинергичната система, 68 или серотонинови лигандни маркери върху позитронно-емисионната томография. 69–73 Оксидативна реактивност, 74 и психофизична реактивност, показващи симпатиковия/парасимпатиковия тонус, 75 могат да идентифицират субекти, които могат да бъдат по-отзивчиви към метаболитни или адренергични лечения.
Какви са примерите за биомаркери, които са ръководили клинично лечение?
КАКВИ ОПИТВАНИЯ ПРИ РАЗРАБОТВАНЕ НА БИОМАРКЕРИ ЗА ASD СА БИЛИ ИЗПЪЛНЕНИ ИЛИ ВЪПРОС?
КАКВА Е РОЛЯТА НА ФЕНОТИПИРАНЕТО ПРИ ОТКРИВАНЕ НА БИОМАРКЕРИТЕ ЗА ASD?
Въпреки че биомаркерите сами по себе си могат да предоставят критична информация по отношение на биологията, свързана с основното разстройство на аутистичния спектър (ASD), фенотипната информация би предоставила допълнителни критични данни, които също са по-лесно достъпни в клиничната обстановка, което ще позволи на изследователя или клинициста да избере оптимално индивидуализирано лечение за всеки пациент. Допълнителна клинична информация може допълнително да взаимодейства с връзката между биомаркер и терапевтичен отговор. Такова включване на богата поведенческа и фенотипична информация заедно с биологичната информация позволява на клинициста да идентифицира характеристики, които могат да бъдат свързани с тези биомаркери за прогнозиране на най-добрия план за лечение. Както е описано с NIMH RDoC, 38 този подход позволява по-нюансирано разбиране на потенциалните резултати, към които може да се насочи лечението. Предишните усилия за разработване на биомаркери варират в степента, до която е включена фенотипна информация. За подтипиране на пациенти с потенциална значимост за индивидуализирано лечение ще е необходима по-голяма фенотипна информация.
ТЕКУЩИ СТРАТЕГИИ ЗА ИЗВЪРШВАНЕ НА ФЕНОТИПИРАНЕ
ЕКСПОЗИЦИИ ЗА ОКОЛНАТА СРЕДА КАТО ПОТЕНЦИАЛНА БИОЛОГИЧНО СЪСТАВЯЩА СТРАТИФИКАЦИЯ ПРОМЕНЛИВА: ASD „ENVIROME“
Въпреки че по-ранни доклади, базирани на проучвания на близнаци, предполагат, че разстройството от аутистичния спектър (ASD) има наследственост до 0.9, 111–115 скорошни доказателства предполагат, че чисто генетичният компонент в причината за ASD е малко по-малък, отколкото се смяташе досега. 116–118 Въпреки че нашето разбиране за причините за околната среда е далеч по-малко от това за генетичните причини, трябва да се вземе предвид и тяхното въздействие върху основните невронни системи, свързани с експресията на ASD. Тази област на изследване се увеличи през последните години, като няколко фактора на околната среда придобиха голямо значение. Тези редове на изследване предполагат хипотезата, че ASD „envirome“ взаимодейства със специфични подлежащи невронни системи (генетично обусловени) в развиващия се човешки мозък, за да допринесе за експресията на ASD.
Един такъв негенетично допринасящ фактор за ASD е дисрегулацията на имунната система, която често се описва при лица с ASD и членовете на техните семейства. 65 Най-вече се съобщава, че майките на деца с ASD съдържат антитела, реактивни на фетални мозъчни протеини, които липсват при майки на деца, които обикновено се развиват, или на деца със забавяне на развитието без ASD. 119–121 Наскоро бяха идентифицирани протеиновите целеви антигени на тези ASD-специфични майчини антитела; именно разпознаването на различни комбинации от тези протеини от майчините антитела придава специфичността на ASD, свързано с майчините антитела (MAR). 122 Реактивността на антителата към тези протеини е отбелязана при 23% от майките на деца с ASD, в сравнение с по-малко от 1% при жените с типично развиващи се деца, което представлява много по-висок дял на ASD от всеки отделен ген. Етиологичната значимост на тези антитела се подкрепя допълнително от многобройни проучвания с гризачи и нечовешки примати, при които инжектирането на тези специфични за ASD майчини антитела в бременни животни е довело до MAR-аутистично поведение при потомството. 123–127
Излагането на психосоциални стресови фактори 128 или тропически бури 129 в края на втория до началото на третия триместър също е свързано с повишена честота на ASD. Повишен риск е установен и при различни други излагания на стрес в епидемиологични проучвания от датската и шведската кохорти. 130 131 В едно проучване тази асоциация присъства специално, когато психиатричната история на майката е включена в анализа на данните. 132 Рискът от ASD, свързан с пренатален психосоциален стрес, изглежда е свързан с генетичната податливост на майката към по-голяма реактивност на стреса. 133 Освен това, в модел на гризачи, пренаталното излагане на стрес на потомство на майки, податливи на генетичен стрес, е довело до отклоняващо се социално поведение 134, което също е свързано със забавена миграция на GABAergic неврони по време на развитието. 135 Излагането на майката на стрес преди бременност и дори стрес в началото на живота е свързано с повишен риск от развитие на ASD при следващи бременности, според скорошни открития в данни от здравното проучване на медицинските сестри. 136 137
ФЕНОТИПИРАНЕ, БИОМАРКЕРИ И ИЗПИТВАНИЯ ЗА ЛЕЧЕНИЕ
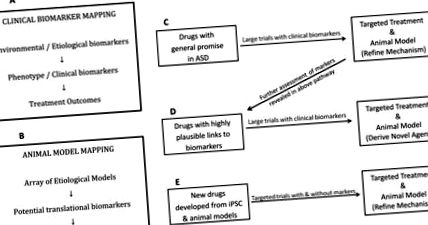
А. Настройка, обогатена с биомаркери за изпитания на ранен етап, за да се информират по-големи изпитания
Този процес би илюстрирал разумен модел, в който са насочени невронните системи, като същевременно е чувствителен към свързаното време за развитие. Един критичен въпрос е дали по-ранната намеса може да доведе до подобряване не само на симптомите по време на изпитването, но и до подобрена траектория на развитие. Също така е възможно лечението, което изглежда да е от полза по-рано, като например намалено поведение при приемане на лекарства, причиняващи седация, може да няма оптимални дългосрочни резултати. Поради това възрастта на участие и дългосрочното наблюдение може да са други ключови компоненти, които да се вземат предвид за включване в бъдещи клинични изпитвания.
Б. Причина/Картографиране на биомаркери, позволяващи разработването на нови съединения с животински модели, превеждащи се в клиничната обстановка по целеви начин
Информацията, получена от изследвания в богата на биомаркери среда, би информирала развитието и оценката на нови съединения в животински модели. За да се оптимизира този подход, трябва да се създаде карта на причините/биомаркери от големи клинични популации. Знанията от проучванията на ензима на ASD, както и развитието и когнитивната неврология трябва да модифицират картата на причината/биомаркера в подходящи възли. Гени, свързани с ASD, са били широко използвани при разработването на предклинични животински модели, включително мишки, плъхове, дрозофила и риба зебра. Впоследствие тези модели са използвани за оценка на рисковите гени за ASD и отговорите на нови лечения, с предимството, че резултатите от поведението, свързани с ASD, могат да бъдат изследвани. 175 Освен това животинските модели позволяват оценка на произтичащите от това поведенчески и физиологични ефекти, произведени от генетичните мутации и/или експериментални лечения, които не са възможни при хората.
Въпреки че терапевтичните лечения, базирани на проучвания върху животни, които използват генетично модифицирани животни по този начин, могат впоследствие да бъдат изследвани в клинична популация, може да бъде уверен само в реакция при пациенти с ASD, причинена от тази конкретна мутация (представляваща само малка част от общата население) и потенциално други с много подобен механизъм. По тази причина е разработен Предклиничният консорциум за терапия за аутизъм (PACT). PACT има за цел да използва селекция от генетично модифицирани модели на гризачи в стандартизиран паралелен метод за оценка на ефектите от потенциални нови фармакологични интервенции. 176
В. Как индуцираните плурипотентни стволови клетки могат да подпомогнат развитието на биомаркери?
Неотдавнашно проучване, използващо 3-D невронни култури (органоиди), получени от получени от пациента iPSCs с идиопатичен ASD, откри доказателства за свръхпродукция на инхибиторни неврони, повлияни от свръхекспресията на FOXG1. 180 Нокдаун на FOXG1 от RNAi в органоиди, получени от ASD, възстанови баланса между инхибиторно/възбуждащо производство на неврони, идентифицирайки FOXG1 като потенциална лекарствена цел. Необходима е бъдеща транслационна работа за тестване на терапевтичното въздействие на насочването към FOXG1 при идиопатична ASD.
Индуцираните плурипотентни стволови клетки предлагат предимството на мащабируемост пред животински модели. Ефектите на новите терапевтични средства могат да бъдат оценени по много ефективен начин с iPSC модели. 39,181–183 Освен това фактът, че това се основава на човешки мутации в човешката тъкан, предоставя допълнителни предимства при потенциално транслационно въздействие в сравнение с животински модели. Въпреки това, iPSCs са ограничени в способността си да изследват както негенетични причини, така и в случаите, при които патологията на ASD е резултат от ефекти, изискващи взаимодействието на множество нервни системи по време на специфични епохи на развитие. Съществуват и значителни технически предизвикателства, присъщи на изследванията на iPSC, включително предизвикателства при спецификацията и поддържането на типовете невронални клетки на мозъчната кора. Първоначалните разходи и достъпът до технология ограничават групите, които могат да предприемат мащабни проучвания на множество генетични причини за ASD в този момент за iPSC. Това ограничение може да стане по-малко проблематично, тъй като тези технологии стават по-евтини и по-широко достъпни.
БЪДЕЩЕТО. КАКВО ЩЕ НУЖНО ЗА ОТКРИВАНЕ НА БИОМАРКЕРИТЕ НА ASD?
Ценна информация е получена от по-големи епидемиологични проучвания по отношение на рисковите фактори на околната среда за ASD, като здравното проучване на медицинските сестри и датските и шведските кохорти, обсъдени в по-ранните раздели. Проучването за детски аутизъм от генетиката и околната среда (CHARGE) проследява големи проби от ASD и незасегнати деца по начин, контролиращ случая, за да се определи етиологичният принос от експозицията на околната среда, възпалителните маркери и генетичните фактори и техните взаимодействия при ASD (http: //beincharge.ucdavis.edu/), който вече разкри редица потенциални участници в околната среда, описани в по-ранните раздели. Освен това, проучвания като маркерите за риск от аутизъм при ранни признаци на бебета (MARBLES) (http://marbles.ucdavis.edu/) и надлъжно разследване на риска от ранния аутизъм (EARLI) (http://www.earlistudy.org /) ще предостави ценна информация за редица фактори чрез внимателно проследяване на последващата бременност на семейства с деца с аутизъм.
* Членове на MISSOURI AUTISM SUMMIT CONSORTIUM
Бележки под линия
Срещата в Университета на Мисури и Центъра Томпсън, от която е произведена тази статия, е финансирана от безвъзмездни средства от Mizzou Advantage, Програмата за уважавани посетители на Университета на Мисури, Института за клинична и транслационна наука на Университета в Мисури (iCATS) и Thompson Център за аутизъм и невроразвитие.
Разкриване: От приключването на статията, Даниел Смит зае позиция в Blackthorn Therapeutics. Останалите участници не декларират конфликт на интереси.
- Учените разкриват нови генетични мутации, свързани с разстройство от аутистичния спектър
- Рискови фактори за рак на простатата Медицина Джон Хопкинс
- Безалкохолна мастна чернодробна болест Carr Lab Perelman School of Medicine в Университета в
- Безалкохолна мастна чернодробна болест Вестник по естествена медицина
- Метаболитно разстройство или алалия или аутизъм -Doctors Lounge (TM)