Лидия И. Архир
1 Катедра по вътрешни болести, Университет по медицина и фармация „Григоре Т. Попа“, Яш, Румъния
2 Клинична болница „Сф. Спиридон ”, Яш, Румъния
Лора Михалаче
1 Катедра по вътрешни болести, Университет по медицина и фармация „Григоре Т. Попа“, Яш, Румъния
2 Клинична болница „Сф. Спиридон ”, Яш, Румъния
Михай Коваса
3 Катедра по основни медицински науки, Колеж по остеопатична медицина, Западен университет по здравни науки, Помона, Калифорния, САЩ
4 Департамент по здравеопазване и човешко развитие, Университет в Сучава, Сучава, Румъния
Резюме
Въведение
Адипозна термогенеза и адипокини
Има два вида мастна тъкан: бяла или кафява. При хората мазнините се състоят главно от бяла мастна тъкан (WAT), която е силно включена в хомеостазата и е способна да установи авто-, пара- и ендокринни начини за комуникация с други тъкани и органи. Мазнината, съставена от адипоцити/преадипоцити, съдържа също ендотелни клетки, мултипотенциални мезенхимни клетки, нервни клетки и имунни клетки, участващи в възпалителни и метаболитни/хормонални реакции. Той секретира цитокини, наречени адипокини (адипоцитокини), които влияят на възпалението, ангиогенезата и метаболитните процеси (14). Някои от тези адипокини се секретират предимно от адипоцитите (напр. Лептин, адипонектин, резистин, хемерин и висфатин), но много (напр. TNFα, IL-6 или MCP-1) се секретират и от други клетъчни типове (15 –18). Тъй като тези молекули могат да генерират сигнали на местно и периферно ниво, се смята, че те оказват влияние върху много метаболитни пътища, както и върху диференциацията на адипоцитите. Те също така служат като медиатори, свързващи възпалението и имунитета със затлъстяването и съпътстващите го заболявания/усложнения (19). Всъщност WAT може да бъде най-големият ендокринен орган, генериращ изобилие от хормони, фактори на растежа и комплемента и други молекули, включително рецептори за много от тези биологични агенти (20).
Ясно е обаче, че WAT основно съхранява триглицериди и мастни киселини (най-големият енергиен резерв) и се състои от клетки с единична (едноочна) липидна капчица и малко кръвоносни съдове, което води до неговия бяло-жълт вид. Съдържа ексцентрично ядро и много малък брой митохондрии. За сравнение, кафявата мастна тъкан е специализирана в енергийните разходи („изгаря калории“) (21). Състои се от много мултиокуларни липидни капчици и много голям брой съдържащи желязо митохондрии (21, 22). Митохондриалните мембрани на тази тъкан включват протеин, наречен разединяващ протеин 1 (UCP1), който изпомпва протони от митохондриалната матрица към митохондриалното междумембранно пространство (23). Активираният UCP1 не предизвиква синтез на АТФ, но води до отделяне на топлина, регулирайки телесната температура, особено при новородени (23, 24). НДНТ има положително влияние върху метаболитните процеси и увеличава общия разход на енергия, което води до намаляване на телесната маса (21). BAT произвежда специфични ендокринни фактори (фибробластен растежен фактор-21), както и отдалечени сигнали със системни последици (25). НДНТ може също да увеличи усвояването на кръвната глюкоза и липидите, подобрявайки техния метаболизъм, независимо от загубата на тегло.
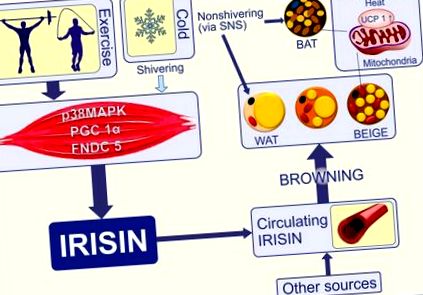
Известно е, че НДНТ е изобилна при гризачи и ниска при големи бозайници, като присъства при хората по време на вътрематочния живот и при кърмачетата в междускапуларните и околобъбречните региони, но дори тези малки количества постепенно изчезват (26). При възрастни НДНТ е остатъчна и без значителна физиологична активност (27). Неотдавнашното откритие на активна НДНТ при възрастни хора и документирането на няколко транскрипционни фактора, които регулират образуването на нови термогенни адипоцити, прави привлекателно увеличаването на този тип мастна тъкан и използването му като терапевтична цел (28). Подкожните мазнини могат да станат „кафяви“ при няколко дразнитела като студ, бета-адренергични агонисти или хормоноподобни стимули (29) (Фигура 1). Това зачервяване на мазнините включва индукция на UCP1mRNA и експресия на гени, които разделят дишането и производството на топлина. Доказано е при мишки, че е възможно намаляване на висцералната мастна тъкан, например с генетичната аблация на ретиналдехид дехидрогеназа 1 (RALDH1) (35), но този процес е много по-рядък от покафеняването на WAT. Откриването на индуцируеми бежови адипоцити разшири изследванията в тази област и има терапевтични обещания (36).
Студът инициира треперене в скелетните мускули и фаза без треперене, в която кафявата и бежовата мастна тъкан се активират, за да отделят топлина чрез UCP-1. Треперенето и упражненията насърчават термогенезата, медиирана от мастната тъкан, чрез секреция на иризин (30). Упражнението увеличава транскрипционния коактиватор PGC1-α и индуцира експресия на гена FNDC5. FNDC5 мембранният протеин се разцепва, за да освободи иризин в кръвта. Иризинът също се освобождава от адипоцитите, като по този начин се превръща в адипоцитокин (18). Други източници като мозък, панкреас, стомах, клетки на Купфер, език, ректум, сърце, тестис, синусоидални епителни клетки и зрителен нерв също освобождават иризин (31). Иризинът насърчава „потъмняване“ на зрели бели адипоцити в отговор на упражнения (32, 33). Кафявите и бежовите мастни тъкани увеличават енергийните разходи чрез отделяне на окислителния метаболизъм от производството на АТФ. Това е ключова функция на UCP1 (34). PGC-1α, активиран от пероксизомен пролифератор рецептор гама коактиватор 1 алфа; FNDC5, Fibronectin тип III, съдържащ домен протеин 5; WAT, бяла мастна тъкан; НЕТ, кафява мастна тъкан; БЕЖ, бежов адипоцит, брит („кафяво в бяло“) или индуцируема НДНТ; UCP1, разединяване на протеин-1; SNS, симпатикова нервна система.
Мускулна термогенеза и миокини
Произход на Irisin
Иризинът, открит за първи път при животни, а по-късно и при хора, е един от най-изследваните пептиди, предизвикани от упражнения през последните години (32) и се радва на все по-голяма популярност от старта си с лозунга „запали огъня ми“ (62). Иризинът принадлежи към класа на адипомиокините, тъй като действа както в мастната, така и в мускулната тъкан (адипокин и миокин) и е термогенен протеин, който насърчава енергийните разходи чрез кафяво от WAT (63). Иризинът разсейва енергията като топлина (64) и поради тази причина откритието му предизвика многобройни изследвания, насочени към разбиране на механизмите на енергийния метаболизъм (65). Неговото изолиране в мускулната тъкан, номенклатурата и първоначалната химическа характеристика са извършени от Bostrom et al. който показа, че иризинът е протеин със 112 аминокиселини и молекулно тегло 12 kDa (32). Името ирисин произхожда от древногръцката богиня Ирис (32), дъщеря на Таумас и Електра, която в гръцката митология е била богинята пратеник на добри новини от боговете до хората (66). Това име се оказа много подходящо, тъй като се отнася до основната функция на иризина, като химически пратеник, предаващ полезните ефекти от физическите упражнения върху мастната тъкан (зачервяване и термогенеза) и други органи, участващи в метаболизма.
Иризин и упражнения
Хомеостаза на иризин и глюкоза
Иризинът улеснява усвояването на глюкоза от скелетните мускули, подобрява метаболизма на чернодробната глюкоза и липидите, като има положителен ефект върху хиперлипидемията и хипергликемията, причинени от затлъстяване и метаболитен синдром (80), и следователно действа като инсулиносенсибилизиращ хормон (Фигура 2). Смята се, че иризинът влияе на органи и тъкани, участващи в диабет тип 2, като черния дроб и панкреаса, чрез намаляване на IR, въпреки че механизмите, чрез които той модулира функцията на панкреатичните островчета, все още не са известни (60). Предполага се, че иризинът може да подобри чернодробния метаболизъм чрез намаляване на ендоплазмения стрес на ретикулума (ER стрес) и че допринася за оцеляването и функцията на β-островните клетки (Фигура 2). Следователно иризинът може да повлияе положително на черния дроб и островчетата на панкреаса, като по този начин намалява риска от развитие на захарен диабет тип 2 (80).
Циркулиращият иризин произхожда главно от скелетни мускули по време на активност и от мастна тъкан. Иризинът действа локално, по автокринен/паракринен начин, а когато се пусне в обращение, действа по хормонален начин, медиирайки периферната активност (80). Иризинът има многоспектърни функции върху различни тъкани или органи, инхибира адипогенната диференциация, като същевременно насърчава остеогенната диференциация (59). Иризинът влияе върху функцията на скелетните мускули, панкреаса (81), черния дроб (82), мозъка (83) и костите (84, 85) засилва инсулиновата чувствителност, метаболизма, когницията и остеогенезата. Иризинът подобрява инсулиновата резистентност и диабет тип 2 чрез повишаване на чувствителността на инсулиновия рецептор в скелетните мускули и сърцето, чрез подобряване на чернодробния метаболизъм на глюкозата и липидите и чрез насърчаване на функциите на бета-клетките на панкреаса и покафеняване на бялата мастна тъкан (86). WAT, бяла мастна тъкан; BDNF, мозъчен невротрофичен фактор.
Участието на черния дроб в глюкозната хомеостаза е да се поддържа баланс между производството на чернодробна глюкоза и съхранението на глюкоза. Скоростта на глюконеогенезата се диктува предимно от нивата на транскрипция на ензимите на глюконеогенезата, фосфоенолпируват карбоксикиназата (Pepck) и глюкозо-6-фосфатазата (G6Pase). От друга страна, инхибирането на GSK-3 насърчава активността на гликоген синтазата, водеща до гликогенеза (87). Чернодробният липиден метаболизъм също играе съществена роля в хомеостазата на глюкозата. Когато приемът на въглехидрати надвишава капацитета за съхранение и окисляване, те се превръщат в мазнини чрез de novo липогенеза. Въпреки това, излишъкът на липиди в черния дроб причинява възпаление и IR (88). Значителни доказателства предполагат, че ER стресът, особено чернодробният ER, е тясно свързан с метаболитни заболявания, като насърчава производството на глюкоза в черния дроб, липогенезата и IR при затлъстяване и диабет (89). Активирането на чернодробния AMPK има антидиабетна роля в черния дроб чрез модулиране на метаболизма на глюкозата и мазнините, затихване на липогенезата и глюконеогенезата и насърчаване на липидната окисленост и гликолиза (90).
Иризин и затлъстяване
Въпреки че иризинът е известен предимно като миокин, той също се освобождава от мастната тъкан (18, 60), спечелвайки името си като адипокин и медиирайки полезните метаболитни ефекти от упражненията (101). При гризачите FNDC5/иризин се секретира предимно от адипоцитите на SAT и в по-малко количество от адипоцитите на висцералната мастна тъкан (ДДС) (18). При хората обаче експресията на FNDC5 е 100-200 пъти по-ниска при WAT, отколкото при мускулите, което показва незначителен принос на WAT към нивата на циркулиращия иризин (102). Приносът на мастната тъкан към циркулиращите нива на иризин е потвърден от молекулярни животински проучвания, доказващи, че секрецията на мастна тъкан допринася за циркулиращия FNDC5/иризин (18). Освен това мастната тъкан от човешки произход експресира и секретира FNDC5/иризин (103). Експериментите in vitro разкриват, че иризинът се произвежда в човешки преадипоцити и адипоцити и в адипоцити на 3T3-L1 (73). В резултат на това нивата на предшественика на иризин PGC1α са по-високи в мастната тъкан, отколкото мускулите след упражнение и това корелира с модела на секреция на иризин. Освен това, подобно на други адипокини, секрецията на иризин от SAT се влияе от нивата на циркулиращ иризин (18).
Противоречия относно секрецията и действието на иризин
Принос на автора
LA, LM и MC участваха в изготвянето, редактирането и писането на ръкописа, одобриха окончателната версия на ръкописа. LA проектира фигурите.
Изявление за конфликт на интереси
Авторите декларират, че изследването е проведено при липса на каквито и да било търговски или финансови отношения, които биха могли да се тълкуват като потенциален конфликт на интереси.
- Диетата с високо съдържание на захар и масло (HSB) предизвиква затлъстяване и метаболитен синдром с намаляване на регулаторните
- JCI - Чревен микробиом, затлъстяване и метаболитна дисфункция
- Насоки - Затлъстяване и метаболитни нарушения Хирургия на затлъстяването
- Високо съдържание на олеинова киселина фъстъчено масло и екстра върджин зехтин добавки отслабват метаболитния синдром
- Джеси Сантяно; t Болни! Псориазис и метаболитен синдром