Субекти
Резюме
Заден план
Анализът на транскриптом на коремна подкожна бяла мастна тъкан (sWAT) установи важни нарушения, свързани със затлъстяването. Въпреки това, връзката между sWAT транскриптома и дългосрочните бъдещи промени в телесното тегло остава неуловима.
Обективен
Да се изследват подписите на sWAT транскриптом преди и след дългосрочни промени в теглото и да се оцени тяхната прогнозна стойност за промени в телесното тегло.
Дизайн
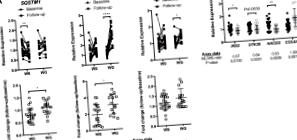
Общо 56 жени бяха проследени надлъжно и разделени на стабилни в теглото (WS, н = 25), наддаване на тегло (WG, н = 14) и отслабване (WL, н = 17) групи между изходното ниво и проследяването (13 ± 1 години). SWAT транскриптомът на гладно се анализира чрез генни микрочипове на изходно ниво и проследяване. Ключовите гени, свързани с промени в теглото, бяха валидирани с помощта на количествена PCR в реално време.
Резултати
Общо 285 стенограми показват разлика (FDR
Опции за достъп
Абонирайте се за Journal
Получете пълен достъп до дневник за 1 година
само 31,08 € на брой
Всички цени са нетни цени.
ДДС ще бъде добавен по-късно при плащане.
Наем или покупка на статия
Получете ограничен или пълен достъп до статии в ReadCube.
Всички цени са нетни цени.
Препратки
Flegal KM, Kit BK, Orpana H, Graubard BI. Свързване на смъртността от всички причини с наднорменото тегло и затлъстяването, използвайки стандартни категории индекс на телесна маса: систематичен преглед и мета-анализ. ДЖАМА. 2013; 309: 71–82.
Kitahara CM, Flint AJ, Berrington de Gonzalez A, Bernstein L, Brotzman M, MacInnis RJ, et al. Връзка между затлъстяването от клас III (ИТМ от 40–59 kg/m 2) и смъртността: обобщен анализ на 20 проспективни проучвания. PLoS Med. 2014; 11: e1001673.
Swinburn BA, Nyomba BL, Saad MF, Zurlo F, Raz I, Knowler WC, et al. Инсулинова резистентност, свързана с по-ниски нива на наддаване на тегло при индианците Пима. J Clin Invest. 1991; 88: 168–73.
Крило RR. Инсулиновата чувствителност като предиктор за възстановяване на теглото. Obes Res. 1997; 5: 24–9.
McLaughlin T, Abbasi F, Carantoni M, Schaaf P, Reaven G. Разликите в инсулиновата резистентност не предсказват загуба на тегло в отговор на хипокалорична диета при здрави жени със затлъстяване. J Clin Endocrinol Metab. 1999; 84: 578–81.
Rebelos E, Muscelli E, Natali A, Balkau B, Mingrone G, Piatti P, et al. Телесното тегло, а не инсулиновата чувствителност или секрецията, може да предскаже спонтанни промени в теглото при недиабетни и преддиабетни пациенти: проучването RISC. Диабет. 2011; 60: 1938–45.
Kong LC, Wuillemin P-H, Bastard J-P, Sokolovska N, Gougis S, Fellahi S, et al. Инсулиновата резистентност и възпалението предсказват кинетични промени в телесното тегло в отговор на диетична загуба на тегло и поддържане при лица с наднормено тегло и затлъстяване чрез използване на байесовски мрежов подход. Am J Clin Nutr. 2013; 98: 1385–94.
Anthanont P, д-р Йенсен. Базалният метаболизъм предсказва ли покачване на теглото? Am J Clin Nutr. 2016; 104: 959–63.
Piaggi P, Thearle MS, Bogardus C, Krakoff J. По-ниските енергийни разходи предсказват дългосрочно нарастване на теглото и мастната маса. J Clin Endocrinol Metab. 2013; 98: E703–7.
DeLany JP, Bray GA, Harsha DW, Volaufova J. Енергийните разходи и окисляването на субстрата предсказват промени в телесните мазнини при деца. Am J Clin Nutr. 2006; 84: 862–70.
Arner P, Bernard S, Salehpour M, Possnert G, Liebl J, Steier P, et al. Динамика на човешкия мастен обмен на липиди в здравето и метаболитните заболявания. Природата. 2011; 478: 110–3.
Tchoukalova YD, Koutsari C, Karpyak MV, Votruba SB, Wendland E, Jensen MD. Размер на подкожната адипоцит и разпределение на телесните мазнини. Am J Clin Nutr. 2008; 87: 56–63.
Spalding KL, Arner E, Westermark PO, Bernard S, Buchholz BA, Bergmann O, et al. Динамика на оборота на мастните клетки при хората. Природата. 2008; 453: 783–7.
Reilly SM, Saltiel AR. Адаптиране към затлъстяване с възпаление на мастната тъкан. Nat Rev Endocrinol. 2017; 13: 633–43.
Guilherme A, Virbasius JV, Puri V, чешки депутат. Адипоцитни дисфункции, свързващи затлъстяването с инсулинова резистентност и диабет тип 2. Nat Rev Mol Cell Biol. 2008; 9: 367–77.
Arner P, Andersson DP, Bäckdahl J, Dahlman I, Rydén M. Повишаването на теглото и нарушения метаболизъм на глюкозата при жените се прогнозират от неефективна липолиза на подкожната мастна клетка. Cell Metab. 2018; 28: 45–54.e3.
Clément K, Viguerie N, Poitou C, Carette C, Pelloux V, Curat CA, et al. Загубата на тегло регулира свързаните с възпалението гени в бялата мастна тъкан на затлъстели лица. FASEB J. 2004; 18: 1657–69.
Dahlman I, Linder K, Arvidsson Nordström E, Andersson I, Lidén J, Verdich C, et al. Промени в експресията на гена на мастната тъкан с диети с ограничена енергия при затлъстели жени. Am J Clin Nutr. 2005; 81: 1275–85.
Dahlman I, Forsgren M, Sjögren A, Nordström EA, Kaaman M, Näslund E, et al. Намаляване на регулацията на гените на електронна транспортна верига във висцералната мастна тъкан при диабет тип 2, независимо от затлъстяването и вероятно включващо тумор некротизиращ фактор-алфа. Диабет. 2006; 55: 1792–9.
Mutch DM, Temanni MR, Henegar C, Combes F, Pelloux V, Holst C, et al. Експресията на адипозен ген преди загуба на тегло може да диференцира и слабо да предскаже диетичните отговори. PLOS ONE. 2007; 2: e1344.
Márquez-Quiñones A, Mutch DM, Debard C, Wang P, Combes M, Roussel B, et al. Транскриптомът на мастната тъкан отразява вариациите между субекти с продължителна загуба на тегло и субекти, възвръщащи теглото си 6 месеца след ограничаване на калориите, независимо от приема на енергия. Am J Clin Nutr. 2010; 92: 975–84.
Mardinoglu A, Heiker JT, Gärtner D, Björnson E, Schön MR, Flehmig G, et al. Екстензивната загуба на тегло разкрива отчетливи промени в генната експресия в подкожната и висцералната мастна тъкан на човека. Sci Rep.2015; 5: 14841.
Armenise C, Lefebvre G, Carayol J, Bonnel S, Bolton J, Di Cara A, et al. Профилирането на транскриптом от мастна тъкан по време на нискокалорична диета разкрива предиктори за теглото и гликемичните резултати при затлъстели, недиабетни пациенти. Am J Clin Nutr. 2017; 106: 736–46.
Linné Y, Dahlman I, Hoffstedt J. бета1-адренорецепторен ген полиморфизъм предсказва дългосрочни промени в телесното тегло. Int J Obes. 2005; 29: 458–62.
Kolaczynski JW, Morales LM, Moore JH, Considine RV, Pietrzkowski Z, Noto PF, et al. Нова техника за биопсия на човешки коремни мазнини под местна упойка с лидокаин. Int J Obes Relat Metab Disord. 1994; 18: 161–6.
Chen J, Bardes EE, Aronow BJ, Jegga AG. ToppGene Suite за анализ на обогатяване на генни списъци и определяне на приоритет на генния кандидат. Нуклеинови киселини Res. 2009; 37 (издание на уеб сървъра): W305–11.
Capel F, Klimcáková E, Viguerie N, Roussel B, Vítková M, Kováciková M, et al. Макрофаги и адипоцити при затлъстяването при хора: експресия на гени в мастната тъкан и чувствителност към инсулин по време на ограничаване на калориите и стабилизиране на теглото. Диабет. 2009; 58: 1558–67.
Locke AE, Kahali B, Berndt SI, Justice AE, Pers TH, Day FR, et al. Генетичните изследвания на индекса на телесна маса дават нови идеи за биологията на затлъстяването. Природата. 2015; 518: 197–206.
Akiyama M, Okada Y, Kanai M, Takahashi A, Momozawa Y, Ikeda M, et al. Изследване за асоцииране в целия геном идентифицира 112 нови локуса за индекс на телесна маса в японската популация. Nat Genet. 2017; 49: 1458–67.
He Y, Hara H, Núñez G. Механизъм и регулиране на NLRP3 активиране на инфламазома. Тенденции Biochem Sci. 2016; 41: 1012–21.
Alligier M, Meugnier E, Debard C, Lambert-Porcheron S, Chanseaume E, Sothier M, et al. Ремоделиране на подкожната мастна тъкан по време на началната фаза на наддаване на тегло, предизвикано от прехранване при хора. J Clin Endocrinol Metab. 2012; 97: E183–92.
Wang Y, O’Connell JR, McArdle PF, Wade JB, Dorff SE, Shah SJ, et al. От корицата: Изследване за асоцииране на целия геном идентифицира STK39 като ген за чувствителност към хипертония. Proc Natl Acad Sci САЩ. 2009; 106: 226–31.
Torre-Villalvazo I, Cervantes-Pérez LG, Noriega LG, Jiménez JV, Uribe N, Chávez-Canales M, et al. Инактивирането на SPAK киназа намалява наддаването на телесно тегло при мишки, хранени с диета с високо съдържание на мазнини, като подобрява енергийните разходи и чувствителността към инсулин. Am J Physiol Endocrinol Metab. 2018; 314: E53–65.
Ikeda M, Kanao Y, Yamanaka M, Sakuraba H, Mizutani Y, Igarashi Y, et al. Характеризиране на четири бодливи 3-хидроксиацил-КоА дехидратази, участващи в синтеза на много дълговерижни мастни киселини. FEBS Lett. 2008; 582: 2435–40.
Khan T, Muise ES, Iyengar P, Wang ZV, Chandalia M, Abate N, et al. Метаболитна дисрегулация и фиброза на мастната тъкан: роля на колаген VI. Mol Cell Biol. 2009; 29: 1575–91.
Chen Y, Zhu J, Lum PY, Yang X, Pinto S, MacNeil DJ и др. Вариации в ДНК изясняват молекулярните мрежи, които причиняват заболяване. Природата. 2008; 452: 429–35.
Chang L, Adams RD, Saltiel AR. TC10-взаимодействащият протеин CIP4/2 е необходим за стимулирана от инсулин транслокация на Glut4 в адипоцити на 3T3L1. Proc Natl Acad Sci САЩ. 2002; 99: 12835–40.
Fan R, Toubal A, Goñi S, Drareni K, Huang Z, Alzaid F, et al. Загубата на корепресора GPS2 сенсибилизира активирането на макрофагите при метаболитен стрес, предизвикан от затлъстяване и диабет тип 2. Nat Med. 2016; 22: 780–91.
Cuffe H, Liu M, Key C-CC, Boudyguina E, Sawyer JK, Weckerle A, et al. Целевото заличаване на адипоцит Abca1 (ATP-Binding Cassette Transporter A1) уврежда затлъстяването, предизвикано от диетата. Arterioscler Thromb Vasc Biol. 2018; 38: 733–43.
Frisdal E, Le Goff W. Adipose ABCG1: Потенциална терапевтична цел при затлъстяване? Адипоцит. 2015; 4: 315–8.
Wei H, Tarling EJ, McMillen TS, Tang C, LeBoeuf RC. ABCG1 регулира нивата на холестерола на макрофагите в мастната тъкан на мишката и съотношението на клетките M1 към M2 при затлъстяване и калорични ограничения. J Lipid Res. 2015; 56: 2337–47.
Dahlman I, Rydén M, Brodin D, Grallert H, Strawbridge RJ, Arner P. Многобройни гени в локусите, свързани с разпределението на телесните мазнини, са свързани с мастната функция. Диабет. 2016; 65: 433–7.
Murphy J, Moullec G, Santosa S. Фактори, свързани с намаляване на размера на адипоцитите след интервенции за отслабване при наднормено тегло и затлъстяване: систематичен преглед и метарегресия Metab Clin Exp. 2017 г .; 67: 31–40.
Dikic I, Elazar Z. Механизъм и медицински последици от автофагията на бозайници. Nat Rev Mol Cell Biol. 2018; 19: 349–64.
Zhang Y, Sowers JR, Ren J. Насочване към автофагия при затлъстяване: от патофизиология до управление. Nat Rev Endocrinol. 2018; 14: 356–76.
Kovsan J, Blüher M, Tarnovscki T, Klöting N, Kirshtein B, Madar L, et al. Променена автофагия в човешките мастни тъкани при затлъстяване. J Clin Endocrinol Metab. 2011; 96: E268–77.
Jansen HJ, van Essen P, Koenen T, Joosten LAB, Netea MG, Tack CJ, et al. Аутофагичната активност се регулира нагоре в мастната тъкан на затлъстели индивиди и модулира проинфламаторната експресия на цитокини. Ендокринология. 2012; 153: 5866–74.
Kosacka J, Kern M, Klöting N, Paeschke S, Rudich A, Haim Y, et al. Автофагия в мастната тъкан на пациенти със затлъстяване и диабет тип 2. Ендокринол на Mol Cell. 2015; 409: 21–32.
Shigunov P, Sotelo-Silveira J, Kuligovski C, de Aguiar AM, Rebelatto CK, Moutinho JA, et al. PUMILIO-2 участва в положителната регулация на клетъчната пролиферация в стволови клетки, получени от човешки мастни клетки. Стволови клетки Dev. 2012; 21: 217–27.
Sun K, Tordjman J, Clément K, Scherer PE. Фиброза и дисфункция на мастната тъкан. Cell Metab. 2013; 18: 470–7.
Благодарности
Работата, представена в тази статия, се подкрепя от гранта на Фондация Novo Nordisk NNF18OC0033896, гранта на Шведската фондация за диабет DIA2016-095, Шведския съвет за научни изследвания, стратегическите изследвания, открити в областта на диабета и регионалния окръжен съвет, и съвместното предприятие на ЕС/EFPIA за иновативни лекарства (EMIF безвъзмездна помощ 115372).
Информация за автора
Принадлежности
Катедра по биология и хранене, Karolinska Institutet, 141 83, Стокхолм, Швеция
Келвин Х. М. Куок
Катедра по медицина (H7), Huddinge, Karolinska Institutet, 141 86, Стокхолм, Швеция
Mikael Rydén, Daniel P. Andersson, Peter Arner & Ingrid Dahlman
Лаборатории CLARINS, Понтуаз, Франция
Галски Beauchef, Christelle Guere & Katell Vie
Катедра по медицина, Solna, Karolinska Institutet, 171 76, Стокхолм, Швеция
Катедра по клинични науки, интервенции и технологии, Karolinska Institutet, 181 86, Стокхолм, Швеция
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Автора за кореспонденция
Етични декларации
Конфликт на интереси
Авторите декларират, че нямат конфликт на интереси.
Допълнителна информация
Бележка на издателя: Springer Nature остава неутрален по отношение на юрисдикционните претенции в публикувани карти и институционални принадлежности.
- Регулиране на експресията на генния часовник в човешката мастна тъкан чрез загуба на тегло International
- Регулиране на експресията на генния часовник в човешката мастна тъкан чрез загуба на тегло - PubMed
- Намаляването на телесното тегло с рутин е свързано с увеличаване на кафявата мастна тъкан
- Положителни утвърждения за отслабване - проявете тялото на вашите мечти
- Стероиди за отслабване - Топ 4 режещи стероиди за постно тяло! 2020 г.