Основен съвет: В този преглед е представена промяната на парадигмата по отношение на развитието на фитопрепарати и антиоксиданти след изчерпателно описание на по-нова информация, свързана с патогенезата на панкреатита. Обсъждат се няколко животински модела по отношение на тяхната роля в усилията за разработване на ефективни стратегии срещу панкреатит. Впоследствие се преглеждат по-нови терапевтични възможности с акцент върху хранителните вещества и фитопрепаратите. По-нататъшната дискусия също се фокусира върху обещанието за проучвания, оценяващи ефектите на антиоксидантите/фитопрепаратите при панкреатит, разочароващия характер на превеждането на тези агенти в клинични условия и очакваните постижения в научните изследвания, които могат да подкрепят използването на антиоксидантни фитопрепарати при лечението на панкреатит.
- Цитат: Парк JM, Lee S, Chung MK, Kwon SH, Kim EH, Ko KH, Kwon CI, Hahm KB. Антиоксидантни фитопрепарати за подобряване на панкреатита при животински модели: Отговор от природата. Свят J Gastroenterol 2014; 20 (44): 16570-16581
- URL:https://www.wjgnet.com/1007-9327/full/v20/i44/16570.htm
- DOI:https://dx.doi.org/10.3748/wjg.v20.i44.16570
AP е възпалително разстройство, тъй като възпалението не само засяга патогенезата, но също така определя хода на заболяването от увреждане на панкреатичните ацинарни клетки и смърт до започване на SIRS [8]. Тъй като прекомерният SIRS достига кулминация в основната причина за заболеваемост и смъртност, свързана с AP, увреждане на отдалечени органи (MODS), е важно да се идентифицират молекулите и факторите, участващи в този процес. Фосфолипаза А2 (PLA2), фактор на туморна некроза-α (TNF-α), интерлевкин (IL) -1β, IL-6, IL-8, CINC/GRO-α, MCP-1, фактор за активиране на тромбоцитите (PAF), IL -10, CD40L, C5a, ICAM-1, MIP1-α, CCL5 (RANTES), вещество P и сероводород (H2S) са показали, че играят критична роля [9]. Системните ефекти на AP са подобни на тези при други състояния като септицемия, тежки изгаряния и травма. Например, AP в тежката си форма се усложнява от MODS, най-важното от белодробни усложнения, които включват хипоксия, синдром на остър респираторен дистрес, ателектаза и плеврален излив [10] .
| Остър панкреатит |
| Церулейн ± липополизахарид (LPS) или етанол |
| Инфузия на жлъчен солен канал |
| Запушване на канал ± секретагоги |
| Диета [холин-дефицитен етионин с добавка (CDE)] |
| Цитокини |
| Коксаки вирус група В (CVB) |
| Хроничен панкреатит |
| Церулейн (многократно дозиране) |
| Алкохол |
| Инфузия на канали като тринитробензен сулфонова киселина или натриев таурохолат или дибутилтин дихлорид |
| Запушване на канал |
| Генетични; Cox-2, CFTR, IKK2, LXRb, PERK, TGF-β1 |
| Имунологични |
| Диета (CDE) |
| CVB |
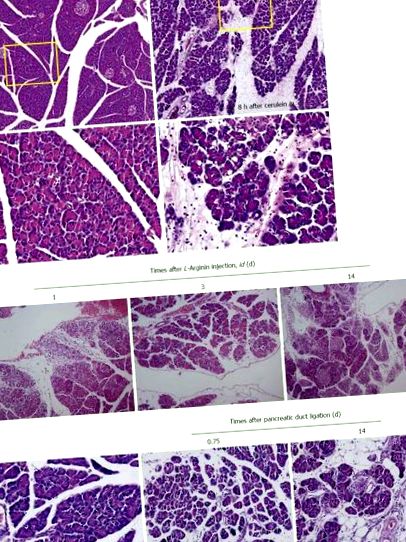
AP може да се предизвика чрез лигиране на дисталния жлъчен канал на нивото на дванадесетопръстника, което причинява ранното развитие на AP, обструктивна жълтеница и холангит при животните. Моделът за лигиране на канал е разработен в опит да прилича на клинични състояния, включително образуване на камъни в жлъчката, нарушения на подвижността на сфинктера, отоци и стриктури в папилата, тумори на папилата и паразити, засягащи крайния билиопанкреатичен канал. Обаче хирургичното лигиране на панкреатичния канал само обикновено причинява само лека до умерена степен на панкреатит и не успява да предизвика SAP. Вместо това повечето лабораторни животни развиват хронични лезии в панкреаса, характеризиращи се с атрофия и апоптоза на ацинарна и дуктална тъкан без значителна некроза или възпаление. Човешкият CP се характеризира с необратима фиброза, докато панкреатичната фиброза при животински модели е обратима (Фигура 1С). Мияучи и др [49] сравнява CP с фиброза при три различни животински модела, модела на дибутилтин дихлорид, плъхове WBN/Kob и плъхове PDL, и установява, че има дисбаланс между синтеза и разграждането на извънклетъчните матрични молекули или степента на стимулация за определен период може да доведе до фиброза на панкреаса.
Тъй като CP се определя като непрекъснато или рецидивиращо възпалително заболяване на панкреаса, характеризиращо се с прогресивни и необратими морфологични промени, панкреатит, последван от перилобуларна и интралобуларна фиброза на паренхима, калцификации в паренхима, както и образуване на псевдокисти [49]. Следователно, животните модели на CP не се различават от моделите на AP, но трябва да преодолеят острия фатален статус според моделите, приемайки хронична PDL, повтаряща се свръхстимулация с церулеан, хронично хранене с алкохол и хронична грижа за L-аргинин или CDE модел на диета. Както се вижда на Фигура 2С, необратимата фиброза и панкреатична недостатъчност след многократни остри пристъпи на панкреатично некро-възпаление [34] се придружават.
Тъй като екзокринната панкреатична недостатъчност е свързана с промени в GI интралуминалното рН, нарушения на подвижността, бактериален свръхрастеж и променен секрет на панкреатичната жлеза, абсорбцията на лекарства при пациенти с CP може да бъде повлияна от степента на тежест на CP [57]. Освен това общото здравословно състояние на пациентите с ХП често е доста лошо, тъй като повечето пациенти с ХП ограничават приема на храна поради болката, причинена от храненето, а в някои случаи приемът на храна може да бъде повече или по-малко заместен с алкохол, тютюн и кафе. Панкреатичната фиброза обаче е характерна черта на хроничното увреждане на панкреаса, което е резултат от дисбаланса между синтеза и разграждането на извънклетъчните протеини. Тъй като звездните клетки са ключови клетки, замесени в индуцирането на TGF-β на колагени, нашите предишни проучвания потвърждават, че антиоксидантните или антиоксидантните фитопрепарати подобряват прогресията на фиброзиращия панкреатит чрез потискащи действия върху звездните клетки на панкреаса.
P- Рецензент: Masamune A, Wronski M S- Редактор: Gou SX L- Редактор: A E- Редактор: Ma S
- Кучешки панкреатит Cy-Fair Animal Hospital
- 1 таблетка за панкреатит cron
- 10 най-добри храни за кучета при панкреатит (декември 2020 г.) - Отзиви; Top Picks Doggie Designer
- Алергии в кучета VCA Animal Hospital
- Информация за породата; Ветеринарни лекари в Fairfield, CA Barney и Russum Animal Clinic