Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Департамент по въпросите на ветераните на САЩ, Здравна система на Сейнт Луис, отдел John Cochran, Сейнт Луис, Мисури
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Адресирайте кореспонденцията и заявките за повторно отпечатване до:
Никълъс О. Дейвидсън, д.м.н., д.ик.н.
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет
660 S Euclid Ave, Сейнт Луис, МО 63110
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Тези автори допринесоха еднакво за тази работа. Потърсете още статии от този автор
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Американско министерство по въпросите на ветераните, Здравна система на Сейнт Луис, отдел Джон Кокран, Сейнт Луис, Мисури
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури
Адресирайте кореспонденцията и заявките за повторно отпечатване до:
Никълъс О. Дейвидсън, д.м.н., д.ик.н.
Отдел по гастроентерология, Медицински факултет на Вашингтонския университет
660 S Euclid Ave, Сейнт Луис, МО 63110
Резюме
Съкращения
Синдромът на раздразненото черво (IBS), дефиниран клинично от хронична коремна болка и променени навици на червата без установима органична причина, засяга до 15% от възрастното население. 1 Въпреки че висцералната свръхчувствителност 2 и анормалната подвижност на червата 3 са основни аномалии, няколко други фактора участват в генерирането на симптоми при IBS, включително генетична чувствителност, 4 промени във фекалната микробиота, 5 бактериален свръхрастеж, 6 чревни възпаления, 7 хранителна непоносимост (включително въглехидратна малабсорбция, ) 8 и чувствителност към глутен. 9 В допълнение, при подгрупа пациенти със синдром на раздразнените черва с диария (IBS-D), патофизиологията може да включва излишно доставяне на жлъчни киселини (BAs) в лумена на дебелото черво, което води до нетна секреция на течности и електролити. 10, 11
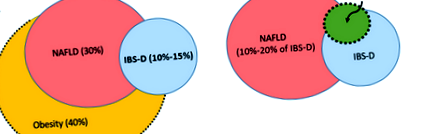
Нарастващата глобална епидемия от затлъстяване фокусира вниманието върху свързаните с това съпътстващи заболявания, включително NAFLD. Съществува значително припокриване в преобладаването на затлъстяването и NAFLD сред населението (фиг. 1А). 17 Новите проучвания обаче също сочат към припокриване между затлъстяването и IBS-D (фиг. 1А). 18 Други проучвания показват по-високо разпространение на NAFLD при пациенти с BAD, 19 и все пак друга работа показва повишени симптоми на диария при подгрупа пациенти с NAFLD (фиг. 1). Тези фактори, известни патофизиологични връзки между променен метаболизъм на БА и диария, заедно с доказателства, свързващи отклоняваща се ВА сигнализация с нарушена метаболитна хомеостаза, 21 повишиха информираността за споделените патофизиологични пътища в подгрупи пациенти с БАД и НАБЛН. Тази асоциация се подсилва от нововъзникващи данни, демонстриращи припокриване на фенотипове, свързващи затлъстяването, NAFLD, IBS-D и BAD (фиг. 1B) и от констатациите с терапевтични агенти, насочени към BAM както при BAD, така и при NAFLD. Тук правим преглед на аспектите на патофизиологията на ВА и хомеостатичната сигнализация, със специален акцент върху това как нарушенията в избрани сигнални пътища могат да допринесат за клиничните прояви, свързващи фенотипите на затлъстяването и свързаните с BAD.
Физиология на BA метаболизъм и нарушения в BAD
Първичните BA претърпяват конюгация чрез цитозолни и пероксизомни BA трансферази към глицин и таурин (в съотношение приблизително 70:30) и след това се изнасят през каналикуларната мембрана чрез помпа за износ на жлъчна сол/аденозин трифосфат свързваща подсемейство B член 11 (Abcb11) (Фиг. 2) и се съхранява в жлъчния мехур, заедно с фосфолипидите и холестерола. 26 След хранене, свиването на жлъчния мехур се предизвиква от секрецията на холецистокинин от дванадесетопръстника l клетки, 26 насърчаване на липидна емулгиране, липолиза и храносмилане на храносмилането. Активна абсорбция на BA се появява в терминалния илеум чрез апикален зависим от натрий транспортер на жлъчна сол (ASBT), семейство носител на разтворено вещество 10 член 2 (Slc10a2) (Фиг. 2). В рамките на илеалния ентероцит BAs свързват фарнезоидния X рецептор (FXR) 26, който след това насърчава хетеродимеризацията с ретиноидния X рецептор (RXR), активирайки FXR/RXR комплекса. Освен това, BA, които не се свързват с FXR и избягват метаболизма на първо преминаване от черния дроб, оказват периферни ефекти върху мастната и мускулната тъкан, сигнализирайки чрез Takeda G, свързан с протеин рецептор 5, за насърчаване на енергийните разходи. 27
Активирането на този хетеромерен комплекс FXR/RXR (фиг. 2) от своя страна транскрипционно нагоре регулира експресията както на малкия хетеродимерен партньор на транскрипционния корепресор (SHP) (до регулиране надолу Slc10a2), така и на илеалния ентерокин FGF15/19 (FGF15 е мишият ортолог). Активирането на FXR/RXR също транскрипционно нагоре регулира експресията на базолатералния илеален ентероцит БА износител на органичен транспортен разтвор (Ost) α/β, който насърчава секрецията на BA в порталната вена за рециркулация в черния дроб (фиг. 2). Илеалните BA се транспортират от илеалния BA-свързващ протеин и се секретират във порталната вена чрез Ostα/β (както по-рано) и впоследствие се транспортират в хепатоцита от чернодробния натриево-таурохолатен ко-транспортиращ полипептид (NTCP), Slc10a1 (фиг. 2 ). 28
Абсорбцията и рециклирането на Ileal BA е изключително ефективно, като BA се подлага на ентерохепатален цикъл поне 10 пъти дневно и само 5% от луминалните BA достигат дебелото черво. В дебелото черво първично конюгираните BA претърпяват микробна деконюгация, епимеризация и дехидроксилиране във вторичен Bas 'DCA, урсодезоксихолева киселина (UDCA) и LCA, някои от които се реабсорбират и рециркулират обратно в черния дроб, където се подлагат и реконюгация и секреция заедно с първичната БА. 22 BAs на дебелото черво влияят върху секрецията на течности чрез увеличаване на клетъчния калций и аденозин цикличен аденозин монофосфат, който от своя страна регулира секрецията на епителния хлорид/бикарбонат, като по този начин създава активен механизъм за секреция на течности и електролити и съответно диария (фиг. 2). 36
Развитие и полезност на биомаркери при клинична оценка на BAD
Поради повишената информираност за различните патофизиологични механизми, лежащи в основата на IBS-D, се препоръчва тестване за потвърждаване на диагнозата BAD по време на емпирична секвестрантна терапия на BA. Насоките на Канадската асоциация по гастроентерология за клинична практика препоръчват потвърждаващо тестване със 75 SeHCAT или C4 при започване на емпирична BA секвестрантна терапия. 47 Лица с окончателна диагноза BAD са показали, че имат степен на отговор над 70% на секвестрантната терапия на BA, за разлика от тези с отрицателно тестване за BAD със само 25% отговор на терапията. 48 Освен това потвърждаващото тестване за BAD е вероятно рентабилно и намалява необходимостта от прекомерна диагностична оценка при тази подгрупа пациенти. 49
Клинични изпитвания на агенти, модифициращи метаболизма на BA при BAD и IBS
Холестираминът е BA секвестрант, който намалява диарията при всички видове БАД. В няколко серии случаи 71% до 93% от пациентите са отговорили на холестирамин. 50-52 При IBS-D, 96% са съобщени, че отговарят на емпирична терапия с холестирамин, като дозовият отговор се основава на тежестта на BAM (по-добър отговор при по-тежък BAM). 12 Colestipol е алтернативен секвестрант на BA, който е проучен при лечението на BAD, 11 и colesevelam, още един секвестрант, подобрена диария при 83% от пациентите с BAD, 53 с тенденция към забавяне на 24-часовото транзитно време на дебелото черво. 54
Както бе споменато по-горе, OCA е мощен синтетичен FXR агонист, който е проучен при ограничени пациенти с BAD. Този агент подобрява клиничните симптоми с намаляване на седмичния брой на изпражненията и средната форма на изпражнения при пациенти с първична BAD и пациенти с вторична BAD с кратки резекции на илеята (55
Инхибитор на илеалния БА транспорт, елобиксибат, също е изследван при преобладаващи запек разстройства и е локално действащ инхибитор на ASBT. Блокадата на илеалния БА транспорт води до повишена концентрация на БА в дясното дебело черво и секреторни и двигателни ефекти, които благоприятстват запека. Вторичен ефект е повишеният серумен C4, който корелира с транзита на дебелото черво и формата на изпражненията. 56
Променени сигнали за BA и FGF19 при метаболизма на чернодробните триглицериди и NAFLD
Важна физиологична роля на FGF19 се предполага от предсказуемото следпрандиално повишаване на нивата на циркулация, специфични за съдържанието на мазнини в диетата, 57 предполагащо роля на ентерокин за интегриране на хомеостатичната метаболитна регулация в допълнение към регулирането на синтеза на BA.
| Ерен 68 | Биопсия | 91 (възрастни) | 130 (NAFLD) | 69 | Биопсия | 21 (възрастни) | 57 (NASH) | 0,114 |
| 101 (SS) | ||||||||
| 116 (контроли) | ||||||||
| Шройдер 66 | Ултразвук | 20 (възрастни) | 180 (NAFLD) | 0.94 | ||||
| 260 (контроли) | ||||||||
| Фридрих 67 | Ултразвук | 26 (възрастни) | 116 (затлъстяване NAFLD) | 0,01 | ||||
| 128 (с наднормено тегло) | ||||||||
| 178 (контроли) | ||||||||
| Nobili 70 | Биопсия | 33 (педиатрична) | 55 (NASH) | 60 | Биопсия | 84 (педиатрична) | 41 (NASH) | 60 Хипотезата, че дефицитът на FGF19 води до влошаване на чернодробната стеатоза, се подкрепя допълнително от рандомизирано проучване с FXR антагонист, UDCA, при пациенти със затлъстяване, подложени на операция на стомашен байпас на Roux-en-Y. 71 Пациенти със затлъстяване, предварително лекувани в продължение на 3 седмици с UDCA, показват по-ниски серумни концентрации на FGF19 и повишена тежест на чернодробна стеатоза, както е установено при интраоперативна чернодробна биопсия. |
В обобщение, данните за хора поддържат връзка между ниските серумни нива на FGF19 и чернодробната стеатоза. Най-правдоподобното биологично обяснение на тази връзка е, че дефицитът на FGF19 предхожда развитието на стеатоза, тъй като този дефицит намалява окисляването на чернодробните триглицериди, като същевременно се увеличава de novo липогенеза. И все пак, обръщането на причинно-следствената връзка (т.е. чернодробната стеатоза води до нисък FGF19) остава възможна; това обаче е в противоречие с проучвания, които показват значително повишени нива на FGF19 при пациенти с алтернативна етиология на чернодробно заболяване, като алкохолен хепатит и холестаза. 72
Роля на FGF15 в модели на мишка на NAFLD
| Шумахер 75 | Високо съдържание на мазнини срещу чау | FGF15 KO | Няма разлика в степента на стеатоза |
| Шмит 74 | 1% холестерол срещу чау | Селективен (илеален или чернодробен) FXR KO | Диета с 1% холестерол (но не и чау) при илеални FXR-KO мишки предразполага към чернодробна стеатоза |
| Чен 76 | Тетрациклин | FGFR4 извънклетъчен домейн | FGFR4 антагонизмът предотвратява микровезикуларната чернодробна стеатоза |
| Фу 73 | Високо съдържание на мазнини срещу чау при ob/ob мишки | Трансгенна експресия FGF19 | Повишеният серумен FGF19 предпазва от NAFLD |
| Хуанг 63 | Високо съдържание на мазнини срещу чау | FGFR4 KO | FGFR4 KO мишки, хранени с високомаслена диета, бяха защитени срещу чернодробна стеатоза въпреки повишената дислипидемия |
Клинични изпитвания на агенти, модифициращи сигнализирането през оста FGF19 в NAFLD
Клиничната употреба на рекомбинантен FGF19 първоначално се възприема като ограничена, като се имат предвид опасения с потенциална хепатокарциногенност, причинена от сигнализиране на FGFR4/KLB рецептор чрез сигналния преобразувател и активатора на транскрипция 3 (STAT3). 79 Въпреки това, NGM282, биоинженериран мутант вариант на FGF19, не подава сигнал през STAT3 и е доказано, че е ефективен при обръщане на стеатоза, възпаление и фиброза и е защитен срещу хепатоцелуларен рак при модел на мишка, хранена с високо съдържание на мазнини/високо съдържание на мазнини фруктозна диета. 80 Проучването при хора от фаза 2, използващо парентерално инжектиране на NGM282, успешно постигна своята основна крайна точка за по-малко от 5% загуба на чернодробна мазнина, измерена чрез фракция на мастна протонна плътност с магнитен резонанс при 74% и 78% от лекуваните с 3 mg и 6 mg, съответно (в сравнение с само 9% при плацебо). 81 Тези наблюдавани промени са свързани със значително намаляване на плазмените нива на C4, което предполага, че механизмът на действие включва променен синтез на BA. Лечението с NGM282 също доведе до повишен серумен холестерол с ниска плътност (LDL), главно при големи LDL частици. 81
По подобен начин мощният FXR лиганд, OCA, значително увеличава секрецията на FGF19. 82
В заключение, изглежда, че патогенезата на BAD и NAFLD споделя припокриващи се механизми и пътища (Таблица 3). Чрез сроден FGFR4/KLB рецептор в черния дроб, активността на FGF19 не само регулира BA хомеостазата, но също така играе ключова роля в липидния метаболизъм и инсулиновата чувствителност. По този начин ниските серумни нива на FGF19 са замесени в патогенезата на BAD при IBS-D, както и NAFLD, и следователно парадигмите на лечението, които влияят на хомеостазата на FGF19, показват полза в малки проучвания и при двете групи нарушения. Бъдещите проучвания допълнително ще изяснят включените механизми и пътища и се очаква да дадат нови терапевтични цели и специфични фармакологични агенти, които могат да бъдат полезни за лечение на отличителни подгрупи на пациенти с BAD и NAFLD.
- Най-добрата храна за кучета за киселинен рефлукс - нашите 5 най-добри отзива за 2020 г.
- 3 начина за спиране на диарията при деца - wikiHow мама
- Преглед на алкалната диета 2020 - Rip-Off или си струва да опитате Ето защо
- Всичко за пълнолунието в Овен 30 септември 2020 г. - CityWomen®; Ко
- Алкалната и киселинна диета е опростена - билки Мин