Гладуването е ... хората остават без достатъчно храна, докато гладът е особено вирулентна проява на [глад], причиняващ широко разпространена смърт.
Свързани термини:
- Аминокиселина
- Глюкоза
- Ензим
- Протеин
- Инсулин
- Мутация
- Автофагия
- Автофагозома
Изтеглете като PDF
За тази страница
Глад
Резюме
Фаталният глад е рядка причина за смърт в индустриализираните страни, но може да има голямо медицинско значение, ако смъртта е резултат от умишлено спиране на храна, особено от кърмачета. Значението на глада в клинично, съдебно и медико-правно отношение зависи от степента на недохранване или метаболитни нарушения, които от своя страна зависят от тежестта и продължителността на глада и дали е свързано с обострящи фактори като заболяване. Обикновено диагнозата смърт в резултат на глад е проста диагноза prima facie. Трябва обаче да се изключат основните заболявания като причини за отслабване и съпътстващи заболявания. В следващата глава ще бъде разгледано значението на глада, нормалните хранителни нужди, свързаното с болести недохранване, степента на глад, находките от аутопсията и по-нататъшните разследвания, които са важни в медико-юридически контекст. В случаите на глад при деца са от особено значение няколко класификации на протеиново-енергийното недохранване, разработени за страните от третия свят.
Глад
Резюме
Гладуването е процес, който започва след храносмилане и се удължава, докато храната отново бъде погълната; терминът често се използва взаимозаменяемо с гладуване, което предполага доброволно спиране на приема на храна. Основни метаболитни адаптации се случват за справяне с глада, най-забележителното превключване в използваното гориво. Всички бозайници, включително хората, имат относително малко въглехидратни резерви; 70-килограмов мъж има приблизително 900 kcal въглехидрати, съхранявани като гликоген в скелетните мускули и черния дроб, но има 141 000 kcal триглицериди в мастната тъкан. Мозъкът и червените кръвни клетки използват глюкозата като гориво (мозъкът използва приблизително 600 kcal d -1). Глюкозата, която се синтезира (глюконеогенеза) по време на глад, използва аминокиселини като източник на въглерод. За да се сведе до минимум загубата на чиста телесна маса по време на глад, трябва да се осъществи голяма адаптация, която да позволи използването на мастни киселини и техния окислителен продукт, кетонни тела, като основни източници на гориво. Тази статия описва подробно метаболитните адаптации, които се случват по време на глад и използваните методи за оценка на тези промени.
Глад
Мартин Колмайер, в Хранителен метаболизъм, 2003
Оборот на протеини
Докато значителни количества телесни мазнини могат да бъдат загубени по време на глад, основната опасност идва от разграждането на протеините. Очевидното общо загуба на мускули е зловеща характеристика, която сочи към паралелната загуба на функционални протеини в сърцето, черния дроб, бъбреците и други тъкани.
Около 150 g незаменими аминокиселини и подобно количество несъществени аминокиселини са необходими дневно за синтеза на протеини при здрав мъж със средно тегло (Munro, 1975). Голяма част от това може да се получи от разграждането на телесните протеини.
Когато приемът на енергия престане да бъде достатъчен при предварително добре подхранван човек и еднодневното снабдяване с гликоген се изразходва, клетъчните свободни аминокиселини, редовният белтъчен оборот и увеличеното мобилизиране на малък пул протеини с особено бърз оборот („ лабилен протеин ') може да покрие нуждите от глюкоза през първите часове на гладно. Главната зависимост на мозъка от постоянното снабдяване с глюкоза прави глюконеогенезата от аминокиселини толкова важна.
Увеличаването на секрецията на глюкагон в отговор на спадащите нива на глюкоза в кръвта насърчава мобилизирането на протеини в скелетните мускули и други тъкани. Повечето от хидролизираните протеини достигат до кръвта като аланин и глутамин. Черният дроб и бъбреците могат да използват тези несъществени аминокиселини за глюконкогенеза и да изпратят глюкозата отново в обращение за използване от мозъка, мускулите и други глюкозозависими тъкани. Черният дроб също секретира глутамин в кръвта като азот и носител на гориво за други тъкани (Watford et al., 2002). Терминът аланинов цикъл намеква за използването на аланин като совалка за пренос на азот и въглерод между мускулите и черния дроб. Повишеното разграждане на тъканните протеини и окисляването на освободените аминокиселини е очевидно от удвояването на производството на урея през първите дни на гладуването (Giesecke et al., 1989). Хормоните (адреналин, кортизол) и цитокини (напр. Интерлевкин 6), които се увеличават в циркулацията след травматичен стрес и инфекция, бързо привличат вътреклетъчни свободни аминокиселини (Hammarqvist et al., 2001) и ускоряват белтъчния катаболизъм (Smeets et al., 1995).
Ако гладът продължи, нуждите на телесните мазнини могат да задоволят все по-голям дял от енергията. Дори мозъкът се адаптира все повече към употребата на метаболитите на мастните киселини ацетоацетат и β-хидроксибутират. Предполага се обаче, че тъканният протеин трябва да бъде мобилизиран за попълване на междинните съединения на цикъла на Кребс а-кетоглутарат и оксалоацетат (Owen et al., 1998). Необичайно големите нужди от глюкоза на човешкия мозък, които могат да представляват до половината от общото потребление на енергия на детето, причиняват постоянно изтичане на междинните продукти от цикъла на Кребс. Глицеролът от мобилизирани триглицериди може да отговори на нуждите от синтез на глюкоза на други бозайници с малък мозък, но при хората това не е достатъчно. Независимо от това, затлъстелите хора губят тъканни протеини по време на глад само наполовина по-бързо от слабите (Elia et al., 1999). Наличието на глицерол от мазнини може да има значение.
Продължителното гладуване променя активността на ключовите ензими на метаболизма на протеините и аминокиселините (Young и Marchini, 1990). Като цяло има спад в активността на ензимите, участващи в необратимо разграждане, и увеличаване на ензимите за рециклиране и използване на аминокиселини.
В резултат на гладуването окисляването на аминокиселини от белтъчния оборот пада до по-малко от 10% (Tomkins et al., 1983). Дейностите на аминокиселинните дехидрогенази в мускулите и на урейния цикъл в черния дроб и бъбреците намаляват. При липса на прием на диети, поемането на амоняк от порталната кръв значително надвишава усвояването на аспартат. Последицата е, че чернодробните протеини трябва да бъдат мобилизирани, за да се осигури аспартат за детоксикацията на амоняка като урея (Brosnan et al., 2001).
Том 2
Кетоза от глад
Гладът ще генерира умерена кетоацидоза при нормални индивиди. 282 По време на първоначалните 10–14 часа на гладно нивата на глюкоза се поддържат предимно чрез гликогенолиза. След изчерпване на запасите от гликоген, глюконеогенезата става основният източник на глюкоза. Чернодробните енергийни нужди се поддържат чрез окисляване на мастните киселини. Ускорената липолиза и окисляването на чернодробните мастни киселини водят до кетоацидоза, както беше обсъдено по-рано. След 1–2 седмици концентрацията на кетокиселини в кръвта се стабилизира при около 5–6 mEq/литър и [HCO 3 -] p пада до 18–20 mEq/литър. По-фулминантната кетоацидоза се прекъсва в резултат на индуцирано от кетокиселини освобождаване на инсулин от островните клетки на панкреаса. 237 Въпреки продължаващото гладуване, произтичащото повишаване на нивата на инсулин притъпява липолизата. С продължаването на глада нивата на глюкагон и катехоламин също намаляват към нормалните граници и това също забавя генерирането на кетокиселини. Въпреки това бременните жени и малките деца са особено уязвими към по-тежка кетоацидоза по време на глад. При такива пациенти пероралното хранене често е невъзможно поради анорексия, повръщане и коремна болка.
Метаболитна хомеостаза
Протеинов катаболизъм по време на глад
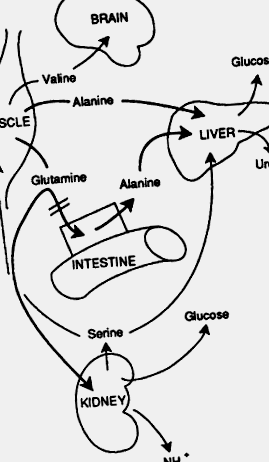
ФИГУРА 22-24. Постабсорбционен метаболизъм на аминокиселини и киселинно-алкален метаболитен превключвател. В ранната постабсорбционна фаза черният дроб е основният източник на плазмена глюкоза, образувана от аланин, доставена от мускулите или червата. Основният азотен продукт е урея. С напредването на глада необходимостта от киселинно-алкален баланс води до намалено усвояване на глутамин от спланхничното легло и увеличено поемане от бъбреците. В бъбреците глутаминът произвежда амониев йон като противоион за β-хидроксибутират и ацетоацетат. Въглеродната верига на глутамин се използва в глюконеогенезата. Ако гладът прогресира, необходимостта от киселинно-алкален баланс води до намалено усвояване на глутамин от спланхничното легло и увеличено поемане от бъбреците. Аминокиселините с разклонена верига служат като основен субстрат за мускулния метаболизъм. По-късно при гладуване някои от аминокиселините с разклонена верига, особено валин, се освобождават от мускулите и могат да бъдат използвани от мозъка като източник на енергия.
ФИГУРА 22-25. Източници на производство на глюкоза по време на глад.
[Възпроизведено с разрешение от F. J. Cahill, Физиология на инсулина при човека: Диабет 20, 783 (1971).]
Системи за поведение на хормони, които не са от бозайници
2.31.3.1 Стрес от глад
Гладуването е екологично значим стрес, тъй като наличието на храна е динамичен аспект на повечето среди. Следователно може да се предположи, че придружаващите поведенчески и физиологични реакции на лишаването от храна са подложени на значителен селективен натиск и че механизмите, залегнали в основата на реакциите на глад, могат да бъдат сходни при широк кръг от организми. При насекомите най-често използваният показател за определяне на реакциите на глад е продължителността на живота и по същество има два фактора, които определят колко дълго един организъм може да оцелее при глад. Първият е размерът на енергийните запаси (т.е. резервоара за гориво), а вторият е как се използва тази енергия (т.е. мили на галон).
Енергийният капацитет може да бъде повлиян от предишната история на хранене, както и от относителната ефективност на трансформацията на хранителни вещества в складирани резерви. Използването на енергия също се влияе от множество различни биологични фактори, включително метаболитни нужди, превръщането на запасите в налична енергийна валута и относителната ефективност на използване (окислителна способност) от активните тъкани. Преразпределението на енергийните изисквания е критичен аспект на подхранването на реакциите на стрес и такива отговори отразяват биологичните приоритети за облекчаване на хомеостатичните предизвикателства.
При дрозофилата, както и при много други метазони, гладът предизвиква хиперактивно поведение. Тази промяна в движението е от общо адаптивно значение, тъй като улеснява отстраняването на организма от източника на стрес или, в конкретния случай на глад, насърчава поведението за търсене на храна. Очевидно гладът също води до изчерпване на енергийните запаси, което се влошава от повишените нива на активност и съпътстващото по-високо метаболитно търсене. Ясно е, че повишената активност води до загуба на енергийни резерви, но може да е и обратното - тоест, че количеството на движението в крайна сметка се контролира от наличността на енергия. Ако случаят е такъв, може да се предположи, че периферните тъкани предават сензорна информация на централните области, които контролират локомоторното поведение. Алтернативно, гладуването може да предизвика независими промени в мобилизацията на енергия и движението.
Анализът на селекцията също така дава представа за основните генетични компоненти, които могат лесно да бъдат изследвани чрез количествени локуси на признаци (QTL) или анализ на микрочипове. Анализът на транскриптите на животни, подложени на условия на глад, показва общо намаляване на изобилието от транскрипти на гени, функциониращи в имунитет (Harbison et al., 2005). В подкрепа на тези резултати паразитиралите дрозофили са свръхчувствителни към стрес от глад и изсушаване (Hoang, 2001). Това предполага, че неспособността за отклоняване на енергиите далеч от имунните функции влияе неблагоприятно върху оцеляването при тези условия. Това се подкрепя и от наблюдението, че хроничното стимулиране на имунната система при дрозофила намалява продължителността на живота (Libert et al., 2006). Аналогично, анализът на микрочиповете показва повишена експресия в различни транскрипти, функциониращи в рамките на метаболитните процеси на мобилизация на енергия (Harbison et al., 2005). Тези резултати подкрепят централната роля на енергийните запаси и употреби като критична цел на модифицирането, предизвикано от глад.
- Нефролитиаза - общ преглед на ScienceDirect теми
- Нефросклероза - общ преглед на ScienceDirect теми
- Skinfold - общ преглед на ScienceDirect теми
- Натриев баланс - общ преглед на ScienceDirect теми
- Покой за разход на енергия - общ преглед на ScienceDirect теми