Резюме
1. Въведение
Постенето нараства популярността през новото хилядолетие. Голяма част от новооткрития ентусиазъм се дължи на нарастващото обществено схващане, че гладуването може да бъде от полза за много аспекти на човешкото здраве. Въпреки предполагаемите ползи за здравето от гладуването, той остава донякъде чужд на конвенционалната медицинска практика, въпреки че тази ситуация не е съвсем нова; постенето в исторически план е изпадало и излиза от мода във връзката му с медицината. Както Марк Твен може да е казал, „Историята не се повтаря, но се римува.“
За да се разбере защо и как гладуването може да бъде приложимо като терапия за редица неврологични заболявания, е полезно да се изследва гладуването както в еволюционен, така и в механистичен контекст. По този начин постепенно трябва да стане ясно, че подходите на базата на гладно и лекарства не трябва да се изключват взаимно; те могат да се комбинират и такъв подход всъщност може да е идеален. В ерата на нарастващите разходи за здравеопазване и нарастващото разпространение на инвалидизиращи неврологични разстройства, въздействието на самоосигуряваща се, безплатна, ефективна терапия заедно с конвенционалните медицински подходи би било значително и положително.
На този фон се обсъждат определението, произходът, механизмите и различните режими на гладуване, последвано от обобщение на доказателствата, подкрепящи гладуването при профилактиката и лечението на различни неврологични разстройства, последвано от дискурс за най-често срещаните нежелани реакции ефекти и заблуди, свързани с гладуването.
2. Какво е гладно?
„Гладуване“ може да се определи като доброволно въздържане от храна и напитки за определени, повтарящи се периоди от време, като периодите на гладно обикновено варират от 12 часа до три седмици при хората [1,2,3,4]. Гладуването най-често се противопоставя на храненето ad libitum („по желание“), което се характеризира с три или повече хранения на ден в съвременните общества и - в комбинация със заседнал начин на живот - може да увеличи риска на човек от развитие на хронично неврологично заболяване [ 5]. Гладуването не трябва да се бърка с глад, състояние на хронична хранителна недостатъчност, което не е нито доброволно, нито контролирано и което може да завърши с органна недостатъчност и смърт.
2.1. Пост: Произход
По време на еволюцията организмите, способни да понасят среда, лишена от хранителни вещества, продължително време притежават важно предимство за оцеляване пред тези, които не могат да го направят. Еволюционният селективен натиск за преживяване на стреса, свързан с нискоенергийната среда, е породил редица метаболитни механизми, предизвикани от гладуване, които са запазени при хора милиони, ако не и милиарди години [6].
2.1.1. Дочовешки еволюционни произходи на гладуването
Много едноклетъчни и прости многоклетъчни организми променят метаболизма си по време на недостиг на хранителни вещества, чиято цел е да се запазят ресурсите, да се минимизират щетите и да се увеличи дълголетието. Например, когато мутантните бактерии от Escherichia coli се прехвърлят от богат на хранителни вещества бульон в среда без калории, те се подлагат на поредица от метаболитни промени, които им позволяват да оцелеят четири пъти по-дълго от бактериите от див тип [7] и когато дрожди Saccharomyces cerevisiae се сменят от растежна среда с вода, тя навлиза в стационарна фаза, която увеличава толерантността си към стрес и удвоява живота си [8,9]. Подобни отговори са наблюдавани и при прости многоклетъчни организми, лишени от хранителни вещества, като нематода Caenorhabditis elegans, която преминава в метаболитно „състояние на дауер“, което води до значително увеличаване на продължителността на живота [10].
Отвъд тези по-прости форми на живот, редица сложни многоклетъчни организми, като бели дробове, змиорки, жаби, змии и членестоноги, също са развили изключителна устойчивост на недостиг на хранителни вещества, отчасти поради намалената скорост на метаболизма в покой и нивата на активност [11]. Въпреки това, вместо да влязат в латентна фаза, някои сложни организми всъщност повишават нивата си на когнитивна и физическа активност, когато пости, подобрявайки способността си да търсят и придобиват храна. Например гризачите при режим на гладно показват намаляване на размера на повечето органи, освен мозъка (и половите жлези) [12], което води до поддържане или подобряване на когнитивната и физическата работоспособност [13,14]. В друг пример, пленни лъвове, преминали от конвенционален дневен график на хранене към режим „дефиле и бързо“, състоящ се само от три хранения на седмица, са показали намаляване на неадаптивното, стереотипно поведение, като темпото и увеличаване на адаптивните, ловни- свързани поведения, като подушване и дебнене [15].
2.1.2. Пост в човешката история
Подобно на много от организмите, които са ги предшествали в еволюцията, хората преди земеделието са издържали редовни периоди на недостиг на храна [16]. Хората са събирачи на ловци от два милиона години; само сравнително кратко преди 12 000 години настъпи преходът към земеделие [17]. По този начин хората след земеделието може да не са имали достатъчно време, за да се адаптират напълно към непрекъснатото снабдяване с храна, осигурено от земеделието, което отчасти може да обясни по-късното въвеждане на доброволни практики на гладуване от повечето цивилизации на земята [18]. Древните римляни например вярвали, че яденето на повече от едно голямо хранене на ден е нездравословно [19]. Повечето световни религии, включително християнството и исляма, също включиха редовен пост в своите религиозни практики [20].
В по-съвременните времена потенциалните ползи за здравето от гладуването са били периодично разпознавани и забравени. Американският лекар Едуард Дюи възприема донякъде радикална гледна точка на гладуването през 1800 г., вярвайки, че на практика всички болести произтичат от прекомерното хранене [21]. През 1900 г. немският лекар Ото Бухингер, първият човек, който стриктно документира полезните ефекти на гладуването при много човешки заболявания, пише, че „Гладуването без съмнение е най-ефективният биологичен метод за лечение“ [22]. Валтер Лонго, роден в Италия биогеронтолог и изследовател на гладно през 2000-те години, наскоро предположи, че гладуването избирателно активира множество „програми за дълголетие“, които могат да доведат не само до удължена продължителност на живота, но и до удължена продължителност на здравето [23]. Любопитното е, че въпреки тези и други застъпници на гладно, установеният режим на хранене в повечето съвременни общества остава три или повече хранения на ден, модел, който е свързан с нарастващо в световен мащаб затлъстяване, диабет тип 2 и различни инвалидизиращи неврологични разстройства [ 24,25].
2.2. Пост: Механизми
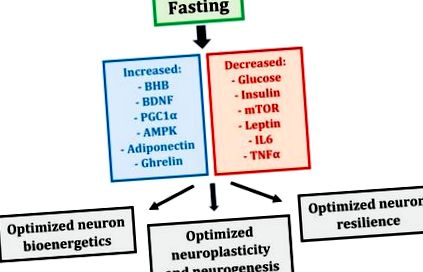
Гладуването предизвиква координирана промяна на много метаболитни и транскрипционни механизми, които могат да повлияят на невроните (Фигура 1). Колективно тези промени създават изменено метаболитно състояние на цялото тяло, което оптимизира невроновата биоенергетика, пластичността и устойчивостта на стрес, завършвайки с поддържано или дори подобрено когнитивно представяне [5].
Индуцирани на гладно метаболитни и транскрипционни механизми и техните ефекти върху невроните (BHB - бета-хидроксибутират; BDNF - невротрофичен фактор, получен от мозъка; PGC1α - активиран от пероксизома пролифератор γ коактиватор 1α; AMPK - AMP-активирана протеин киназа; mTOR - цел за бозайници) на рапамицин; IL6 — интерлевкин 6; TNFα - фактор на туморна некроза α).
2.2.1. Пост: цяло тяло, променено метаболитно състояние
След 12–36 часа на гладно човешкото тяло навлиза във физиологично състояние на кетоза, характеризиращо се с ниски нива на глюкоза в кръвта, изчерпани запаси от чернодробен гликоген и чернодробно производство на кетонни тела, получени от мазнини, или кетони, които служат като основен енергиен източник за мозъка [26]. Черният дроб е основното място на кетогенезата, но мозъчните астроцити също генерират кетони [27,28]. В рамките на няколко дни след започване на кетоните кетоните се превръщат в предпочитан източник на гориво за мозъка, осигурявайки до 70% от енергийните му нужди [29]. Кетоните представляват по-ефективен източник на енергия за единица кислород в мускулите [30,31] и евентуално в мозъка [32], като подобряват биоенергетиката на невроните и когнитивната ефективност; например, беше показано, че гризачите, подложени на кетонен естер в продължение на пет дни, показват подобрено пространствено обучение и памет [33].
И все пак кетоните са нещо повече от източник на енергия за невроните; първичният кетон в кръвта, бета-хидроксибутират (BHB), също изпълнява важни сигнални функции [5,26]. В хипокампалните и кортикалните неврони BHB играе жизненоважна сигнална роля, като индуцира транскрипцията на мозъчно-получен невротрофичен фактор (BDNF) чрез инхибиране на хистонови деацетилази, ензими, които потискат експресията на BDNF [34]. BDNF е основен регулатор на невронната функция; стимулира биогенезата на митохондриите, поддържа синаптичната структура, стимулира производството и оцеляването на нови хипокампални неврони и повишава устойчивостта на невроните към наранявания и заболявания [35].
В допълнение към BHB и BDNF, гладуването индуцира експресията на главен регулатор на митохондриите, транскрипционен фактор, активиран от пролифератор пероксизомен рецептор γ коактиватор 1α (PGC1α) [5,36]. PGC1α е централен индуктор на биогенезата на митохондриите, увеличавайки биомасата на митохондриите, което от своя страна подобрява биоенергетиката на невроните и дава възможност за синаптична пластичност. PGC1α също модулира състава и функцията на митохондриите; например, мускулните митохондрии, изолирани от трансгенни мишки, които ектопично експресират PGC1α, показват повишен дихателен капацитет в сравнение с контролите от див тип [37]. По този начин PGC1α не само стимулира биогенезата на митохондриите, но и стимулира образуването на митохондрии с променени присъщи свойства; и двете имат положителен ефект върху биоенергетиката на невроните.
Гладуването показва мощни ефекти върху метаболизма на глюкозата и инсулиновата сигнализация [1,6]. При хората гладуването в продължение на три до пет дни намалява нивата на глюкозата в кръвта с 30% –40% и инхибира гликолизата [38,39,40]. Гладуването в алтернативни дни в продължение на три седмици намалява нивата на инсулин с 50% –60% на гладно [41]. Като цяло, три до пет дни гладуване при хора също води до 60% спад на инсулиноподобния растежен фактор (IGF-1), основният растежен фактор при бозайниците, пет до десеткратно увеличение на IGF -1 свързващ протеин (IGFBP1), един от основните му свързващи протеини, и дву до трикратно увеличение на растежния хормон (GH), който се повишава, за да запази мускулната маса [39,42,43]. Следователно гладуването предотвратява развитието на хроничен, прекомерен и потенциално нерегулиран метаболизъм на глюкозата, като същевременно запазва чувствителността към инсулин и сигнализирането на растежния фактор, като всичко това може да бъде от полза за невроновите биоенергетици.
Постенето оказва също силно влияние върху процесите на синтез и разграждане на клетките [44,45]. Балансът на клетъчния синтез спрямо разграждането се регулира от съответните дейности на два главни регулатора на метаболизма, мишена на рапамицин (mTOR) и AMP-активирана протеин киназа (AMPK) [44]. При условия с високо съдържание на хранителни вещества (особено аминокиселини), mTOR стимулира синтеза на протеини и растежа на клетките; за разлика от това, когато клетъчните енергийни резерви са ниски, AMPK понижава регулирането на mTOR, за да сведе до минимум консумацията на енергия и да стимулира автофагията, вътреклетъчен път на разграждане, който изчиства неправилно сгънатите протеини и увредените органели, рециклира хранителните вещества и подпомага производството на енергия [45]. Постенето потиска mTOR и повишава AMPK, като по този начин ограничава консумацията и растежа на хранителни вещества в полза на автофагията и оцеляването; въпреки че mTOR и AMPK са изследвани предимно в мускулните клетки, последните данни сочат, че тези два антагонистични главни метаболитни регулатора могат също да медиират отговорите на гладно в невроните [5].
Постенето влияе върху метаболизма на мазнините, като променя хормоналните дейности на лептина, адипонектина и грелина [1,5,46]. Лептинът е свързан с провъзпалително състояние, докато адипонектинът е свързан с повишена инсулинова чувствителност и потиснато възпаление [47]. Грелинът също е свързан с повишена инсулинова чувствителност [48]; освен това грелинът може да стимулира хипокампалната синаптична пластичност и неврогенезата [49]. Гладуването намалява лептина, но увеличава адипонектина и грелина, промени, които вероятно са полезни за биоенергетиката на невроните и поддържането на нервните пътища.
И накрая, гладуването потиска възпалението, намалявайки експресията на провъзпалителни цитокини като интерлевкин 6 (IL6) и фактор на туморна некроза α (TNFα) [50,51]. Тъй като възпалителните процеси са в основата на много различни неврологични разстройства [52], способността на гладно да потиска нервното и системното възпаление може да подобри оцеляването на невроните при тези разстройства.
2.2.2. Пост: повече от ограничение на калориите
Ограничението на калориите се отнася до хронично 20% -40% намаляване на приема на калории, като честотата на хранене се поддържа [1]. Повече от век изследвания показват, че ограничаването на калориите намалява хроничните заболявания и удължава продължителността на живота при различни видове [53]. Тъй като ограничаването на калориите и гладуването споделят много подобни механизми и гладуването често води до намаляване на приема на калории с течение на времето, често се повдига въпросът дали потенциалните ползи от гладуването се дължат само на намаления прием на калории, за разлика от някакъв конкретен ефект от гладуване.
Няколко проучвания върху животни и хора показват, че гладуването може да донесе ползи за метаболизма на клетките (включително невроните) извън ограничението на калориите. Доказано е, че някои мишки, които са гладували през други дни, могат да ядат два пъти повече в деня на хранене, така че нетният им седмичен прием на калории остава подобен на мишките, хранени ad libitum; въпреки липсата на цялостно ограничаване на калориите, първите все още показват полезни метаболитни ефекти в сравнение с вторите, включително подобрени нива на глюкоза и инсулинова активност, както и повишена невронна резистентност към невротоксин, каинова киселина [54]. Проучвания, включващи хора с наднормено тегло и затлъстяване, които не са страдали от диабет, показват по-големи подобрения в чувствителността към инсулин при гладуващи индивиди в сравнение с техните негладни, съпоставени с калории [55,56]. Наскоро петседмично рандомизирано кръстосано проучване при мъже с преддиабет сравнява режим на гладно, съдържащ достатъчен общ прием на калории за предотвратяване на загуба на тегло, спрямо контролна група с редовен график на хранене; въпреки че и двете групи са били съпоставени за прием на калории, групата на гладно е показала по-големи подобрения в чувствителността към инсулин и други мерки за метаболитно здраве [57].
Най-очевидното обяснение на предполагаемия, специфичен за гладуването ефект върху метаболитното здраве може да се крие във фундаменталната разлика между гладуването и ограничаването на калориите - времето. По-конкретно, гладуването се прилага периодично, докато ограничаването на калориите е непрекъснато. След 12–36 часа на гладно се забелязва метаболитен преход или „превключване“ от използване на въглехидрати и глюкоза към мастни киселини и кетони като основни клетъчни източници на гориво [5]. По време на гладно състоянието превключвателят е „включен“, теоретично регулирайки автофагията и пътищата за оцеляване в невроните, докато по време на хранене превключвателят е „изключен“, подчертавайки пътищата за преустройство и растеж. По този начин, за разлика от ограничаването на калориите, гладуването се възползва от всяко последователно биоенергийно предизвикателство, като „подготвя сцената“ за относително свободна от стрес фаза на възстановяване на клетките; с други думи, превключването - прекъсването - може да осигури предимството за метаболизма на невроните. Всъщност, хронифицирането може да бъде вредно, независимо от храненото или на гладно метаболитно състояние - например, острото активиране на mTOR стимулира мускулната хипертрофия, докато хроничното активиране води до атрофия [58,59,60], а периодичното активиране на AMPK засилва невропластичността, но трайно активиране на AMPK уврежда го [61].
2.3. Пост: режими
Три параметъра характеризират режима на гладно - интензивността на ограничаването на храната и напитките, честотата на периодите на гладуване и продължителността на периодите на гладуване (Таблица 1). „Идеалният“ режим на гладуване зависи от индивидуалния начин на живот и поносимостта.
маса 1
Режими на гладно при хора (по интензивност, честота и продължителност).
- Пълна статия Асоциация на ИТМ и инсулин на гладно с рискови фактори за сърдечно-съдови заболявания в
- Особености на медикаментозната терапия на синдрома на болката при пациенти с терминален стадий на бъбречно заболяване
- Ендоскопска оценка на язвена болест по време на Рамадан гладуване
- Оценка на HuoXueHuaYu терапия за безалкохолни мастни чернодробни заболявания систематичен преглед и
- Диетични навици и неврологични особености на пациентите с болестта на Паркинсон Последици за практиката