Отдел по медицинска онкология, клиника Майо, Рочестър, MN 55905, Съединени американски щати
* Автор-кореспондент: Joleen Hubbard
Отдел по медицинска онкология, клиника Майо, Рочестър, MN 55905, Съединени американски щати.
Тел: 5072848318
Факс: 5075386133
Електронна поща: [имейл защитен]
Дата на получаване: 25 август 2016 г .; Приета дата: 31 август 2016 г .; Дата на публикуване: 06 септември 2016 г.
Цитат: Esplin BL, Hubbard J. Изолирани церебеларни метастази като първоначална проява на десния рак на дебелото черво: доклад за случая и преглед на настоящите стратегии за управление. Colorec Cancer 2016, 2: 3.
Въведение
55-годишна жена без значителна минала медицинска история, представена на местния си лекар с двуседмична история на некоординация на дясната ръка и прогресивна нестабилност на походката Тя няма фамилна анамнеза за злокачествено заболяване и отрича загуба на тегло, промяна на апетита, гадене, умора, коремна болка, слабост, треска, студени тръпки или нощно изпотяване.
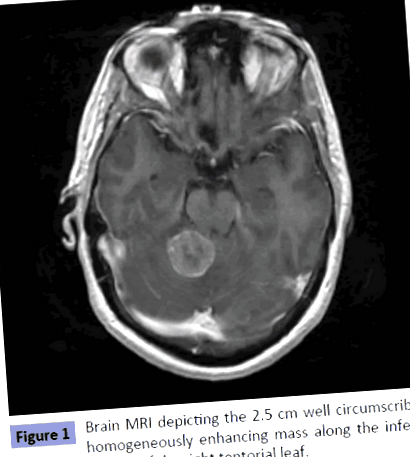
ЯМР на мозъка й разкрива екстраксиален появяващ се мозъчен тумор (Фигура 1), който показва характеристики на менингиом. Пълната кръвна картина разкрива лека нормоцитна анемия с хемоглобин от 11,0 mg/dl и химичен панел с йонизиран калций е нормален. Приложени са предоперативни стероиди и масата е резецирана със задоволителен следоперативен курс и разрешаване на неврологичните симптоми. Патологията разкри метастатичен слабо диференциран карцином. Имунохистохимичните петна бяха положителни за AE1/AE3, CDX2, CK7, CK20 и CAM5, в съответствие с не-невроналния, стомашно-чревния произход.
Фигура 1: Мозъчен резонанс на мозъка, изобразяващ 2,5 cm добре ограничена, хомогенно повишаваща маса по долната повърхност на десния тенториален лист.
Последваща КТ на гърдите, корема и таза разкрива 4,6 × 4,2 × 2,7 cm централно некротична маса по медиалния аспект на цекума и възходящото дебело черво, касаеща първично злокачествено заболяване на дебелото черво. Интересното е, че не са наблюдавани метастази в черния дроб, белите дробове или костите (Фигура 2). Последвалата колоноскопия разкри лезия във възходящото дебело черво и биопсията потвърди междинен аденокарцином. Никога не е била подлагана на скринингова колоноскопия преди поставянето на диагнозата.
Фигура 2: Представително изображение от коремната КТ на пациента, демонстриращо централнонекротичната десностранна маса на дебелото черво. На този КТ не са отбелязани рентгенографски доказателства за чернодробни или белодробни лезии.
След краниотомия тя претърпя лъчева терапия с цял мозък, последвана от десностранна хеми-колектомия. Патологичната оценка разкрива инвазия в околоколоновата мастна тъкан с 7/22 мезентериални лимфни възли, положителни за аденокарцином, в съответствие с pT3N2bM1 стадий IV заболяване. Тя претърпя 12 цикъла на адювантно модифицирана FOLFOX6 химиотерапия без усложнения.
Тринадесет месеца по-късно бяха открити множество 1,5-сантиметрови чернодробни лезии върху наблюдение на КТ корем. Биопсия и мутационен анализ разкриха KRAS див тип метастатичен колоректален рак. Тя е подновена за лечение с FOLFOX6 + бевацизумаб, но развива значителна реакция по време на втората инфузия на оксалиплатин, което води до преминаване към FOLFIRI + бевацизумаб. Наблюдавано е прогресиране на чернодробните метастази след 2 цикъла от този режим, което води до заместване на бевацизумаб с цетуксимаб и продължаване на FOLFIRI. След 7 месеца отговор на заболяването с FOLFIRI + цетуксимаб, CT корем разкри прогресия на чернодробно заболяване. Терапията е преминала към регорафениб. По време на подаването тя е завършила 2 месеца от това лечение 30 месеца след първоначалната диагноза.
Дискусия
| # Пациенти | 17 | 35 | 126 | 29 | 48 |
| Средна възраст, години | 59 | 63 | 62 | 58 | 63 |
| Съотношение мъже: жени | 3.2 | NR | 1.8 | 3.8 | 1.1 |
| Честота на BM в CRC,% | 1.6 | NR | 1.6 | 1.3 | NR |
| Място на първичен тумор,% | |||||
| Възходящ + напречен | 0 | NR | 24 | NR | 40 |
| Низходящ + сигмоиден | 29 | NR | 13 | NR | 12 |
| Ректум | 71 | NR | 63 | 59 | 48 |
| BM характеристики,% | |||||
| Единична | NR | 49 | 40 | 31 | 63 |
| Многократни | 76 | 51 | 60 | 69 | 37 |
| Само надясно | NR | NR | 74 | 48 | 54 |
| Само инфраторсион | 29 | NR | 18. | 6 | 23. |
| Едновременен срещнат сайт,% | |||||
| Бял дроб | 76 | NR | 72 | 69 | 64 |
| Черен дроб | 47 | NR | 33 | 24 | 50 |
| Бели дробове + черен дроб | NR | NR | NR | NR | NR |
| Костен | 23. | NR | 21. | 6.8 | NR |
| Нито един | 12 | 34 | 8 | 21. | 10 |
| Средна преживяемост след BM, месеци (диапазон) | |||||
| Обща средна преживяемост | 4,5 (NR) | 5 | 5,4 (3,9-6,9) | 7,4 (NR) | 4 (1-13) |
| Само хирургия | 5,2 * (NR) | NR | 11,5 ** (0,2-22,7) | 5.1 (NR) | 3 (NR) |
| WBRT | 4,5 (NR) | 3 (1-8) | 4 (1,4-6,5) | 7,9 (NR) | 4 (NR) |
| SRS | 5,2 * (NR) | NR | 9,5 (4,7-14,2) | 7 (NR) | NR |
| Хирургия + радиация | NR | 9 * (2-24) | 11,5 ** (0,2-22,7) | 11.4 *** (NR) | 13 (NR) |
| Подкрепящи грижи | 3,7 (NR) | NR | 1,5 (1,1-1,9) | 1.6 (NR) | 2 (NR) |
| Химиотерапия след BM | NR | NR | 12,7 (9,5-16,0) | NR | NR NR |
* Пациентите, получили „операция или радиохирургия“, са обединени в една и съща група за анализ.
** Пациентите, получили "операция +/- WBRT", бяха обединени в същата група за анализ.
*** Пациентите са получили операция плюс WBRT или SRS.
Маса 1: Характеристики на тумора от избрани проучвания с BM в mCRC, с препратки. BM: Метастази в мозъка; NR: не се съобщава; WBRT: Цялостна лъчева терапия; SRS: Стереотаксична радиохирургия.
Прогнозата обикновено е лоша при пациенти с мозъчни метастази в mCRC, със средна обща преживяемост в диапазона от 5 месеца (диапазон 4,5-7,4 месеца, маса 1). Неврохирургичната резекция на мозъчни метастази, последвана от цялостна мозъчна лъчетерапия (WBRT), може да подобри преживяемостта с приблизително 6 месеца при пациенти с mCRC, в сравнение или с операция, или само с лъчение [3-7,10-13]. Резултатите от оцеляването с различни подходи към мозъчните метастази в CRC са изброени в маса 1. Показано е, че инфентенториалните метастази са лош прогностичен фактор в сравнение с супратенториалните метастази (5,1 срещу 9,1 месеца). Изглежда, че други фактори като пол и брой метастази не оказват влияние върху общото оцеляване след неврохирургична резекция на метастази в мозъка [14].
Съществуват ограничени данни за това кои системни агенти са оптимални при лечението на първа линия за CRC мозъчни метастази [4,15-17]. Стандартните опции включват оксалиплатин или иринотекан, комбинирани с 5-флуоруцил/левковорин плюс биологичен агент, насочен към съдовия ендотелен растежен фактор (VEGF) или епидермален растежен фактор (EGFR). За тези с рак на дивия тип RAS не са докладвани данни за ефективността на панитумумаб или цетуксимаб при мозъчни метастази в CRC. Честотата на KRAS мутации сред пациенти с CRC мозъчни метастази е докладвана при 56%, малко по-висока от честотата на KRAS мутации, съобщени за mCRC като цяло (40%) [18]. Тъй като пациентите с KRAS мутации не са кандидати за лечение с EGFR антагонисти цетуксимаб или панитумумаб, тези терапии могат да играят по-малка роля при пациент с CRC мозъчни метастази [19].
Бевацизумаб, хуманизирано моноклонално антитяло с активност срещу съдов ендотелен растежен фактор А, е одобрен като терапия от първа и втора линия при mCRC в комбинация с цитотоксична химиотерапия. Въпреки това, полезността на този агент за лечение на мозъчни метастази остава неясна, тъй като ранният случай на вътремозъчен кръвоизлив след приложение на бевацизумаб доведе до изключване на пациенти с BM от практически всички следващи клинични проучвания [20-23]. Важно е, че в доклад за случай от 2008 г. това усложнение не се наблюдава при пациент с mCRC и известни метастази в мозъка, когато бевацизумаб е добавен към спасяваща терапия на базата на 5-FU [20]. Текущите проучвания с глиоми и рак на гърдата дават подобни резултати, които могат да подновят ентусиазма за по-строго клинично изследване на бевацизумаб и други целеви агенти при лечението на мозъчни метастази при mCRC [23-25].
Представяме необичаен случай на изолирани симптоматични инфрантенториални метастази в мозъка като първоначално представяне на праволинеен mCRC при иначе здрава 55-годишна жена. Въпреки обикновено лошата прогноза, свързана с инфраторсните метастази в мозъка при mCRC, тя е жива и продължава палиативна терапия 30 месеца след диагнозата. Този случай допълнително подчертава предимството на комбинираното лечение с едномодално лечение за мозъчни метастази при mCRC. Ролята на биологичните агенти при лечението на мозъчни метастази остава неясна, което налага по-нататъшно проучване при тази популация пациенти.
- Метастатичен рак Какво е метастази
- Чернодробни признаци, симптоми и усложнения
- Нарушена регенерация Роля за мускулната микросреда при ракова кахексия
- Черният дроб контролира загубата на рак - ScienceDaily
- Юли 2020 г .; s Новолуние в рак - как влияе на зодията ви