Вторник, 21 януари 2020 г.
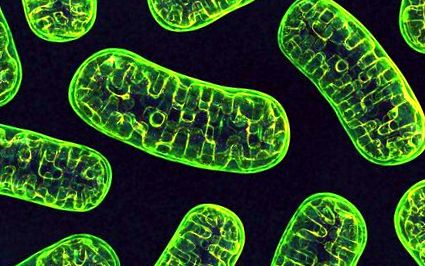
Митохондриите на нашите клетки, произвеждащи енергия (на снимката по-горе), имат силна сигурност, за да се уверят, че вредните вещества не могат да попречат на тяхната решаваща функция. Ново изследване на IRP открива как токсичен протеин, свързан с невродегенеративни заболявания, заобикаля тези защитни сили, за да увреди митохондриите в невроните.
Като фен на дългодействащия анимационен сериал „Симпсъните“, станах свидетел на бъркотията на Омир Симпсън, която предизвика няколко близки срива в атомната електроцентрала, където работи. Сериозни проблеми могат да възникнат в такива съоръжения, когато грешният човек получи достъп до тях, а същото важи и за енергийните митохондрии, които захранват нашите клетки. Ново изследване на IRP разкри как протеин, за който е известно, че уврежда невроните, навлиза в митохондриите, за да предизвика хаос, убиващ клетките. 1
Болестта на Паркинсон, инвалидизиращо неврологично състояние, което причинява сериозни проблеми с движението, е второто най-често срещано невродегенеративно разстройство в САЩ. Болестта е свързана с необичайно натрупване на протеин, наречен алфа-синуклеин, който се произвежда естествено в невроните. Предишни проучвания показват, че когато алфа-синуклеин се натрупва в клетките, той по някакъв начин се придвижва вътре в митохондриите и пречи на способността им да произвеждат енергийните клетки, необходими за оцеляването. Въпреки това точката за достъп алфа-синуклеин, използвана за влизане в митохондриите, отдавна е загадка.
Указание за този пъзел се появи преди няколко години, когато френска фармацевтична компания откри, че лекарството, наречено олезоксим, предпазва митохондриите от токсичните ефекти на излишния алфа-синуклеин. 2 Учените на компанията също установиха, че олеоксимът се свързва с протеин, открит на външната повърхност на митохондриите, наречен зависим от напрежението анионен канал, или VDAC 3, който действа като шлюз, позволяващ на определени молекули да се придвижват в и извън митохондриите.
Тези наблюдения заинтригуват Татяна Ростовцева, доктор по медицина, асоцииран учен в лабораторията на старши изследовател на IRP Сергей Безруков, доктор на науките, тъй като проучванията в нейната лаборатория показват, че алфа-синуклеинът също взаимодейства с VDAC. 4 Следователно д-р Ростовцева и постдокторант в нейната лаборатория, д-р Амандин Ровини, имат за цел да определят дали VDAC участва в способността на олезоксима да защитава митохондриите от алфа-синуклеин.
„Мислете за VDAC като за голяма пора във външната мембрана на митохондриите“, обяснява д-р Ростовцева. „Това е като контролен пункт. Повечето вещества, които митохондриите обработват или произвеждат, не могат да преминат външната мембрана без VDAC. "
Д-р Ростовцева (втора отляво), д-р Ровини (четвърта отдясно) и техните колеги в лабораторията на д-р Безруков
Работата с членове на собствената им лаборатория и изследователи на болестта на Паркинсон в лабораторията на старши изследовател на IRP, д-р Марк Куксън, д-р Ростовцева и д-р Ровини в крайна сметка доказа, че тяхната представа е вярна. Екипът започна с индуциране на свръхпроизводство на алфа-синуклеин в тип клетки, които обикновено се използват за изследване на невроналната функция. В съответствие с минали проучвания, те откриха, че излишъкът от алфа-синуклеин убива тези клетки и че лечението с олеоксим драстично намалява степента на клетъчна смърт, като поддържа митохондриите здрави. Екипът на IRP също потвърди, че когато клетките свръхпродуцират алфа-синуклеин, се открива много повече алфа-синуклеин в техните митохондрии и в непосредствена близост до VDAC на външната повърхност на митохондриите. Лечението с олеоксим обаче значително намалява количеството алфа-синуклеин, разположено близо до VDAC, както и количеството на протеина вътре в митохондриите.
След това, за да проучат дали VDAC е необходим, за да може алфа-синуклеинът да навлезе в митохондриите, учените драстично намалиха количеството на VDAC в клетките, които свръхпроизводиха алфа-синуклеин. Без VDAC те откриха, че алфа-синуклеинът не може да се натрупва в митохондриите, доказвайки за първи път в клетъчен модел, че VDAC е шлюзът, през който алфа-синуклеин навлиза в митохондриите. Освен това, допълнителни проучвания предоставят доказателства, че олеоксимът предпазва митохондриите от алфа-синуклеин, като възпрепятства способността на алфа-синуклеина да преминава през VDAC.
„Това е много нов механизъм, който ние предлагаме“, казва д-р Ростовцева. „Мисля, че това обяснява много неща и вероятно също не е уникално за алфа-синуклеин или олезоксим. VDAC е основно място на митохондриите, засегнато при много невродегенеративни заболявания, а олеоксимът е само едно от редицата невропротективни и противоракови лекарства, които взаимодействат с VDAC, така че този механизъм може да бъде приложим и за лекарства, различни от олезоксима. "
Например може да се окаже, че лекарствата против рак често причиняват форма на увреждане на нервите, наречена невропатия, тъй като подобно на алфа-синуклеин, те увреждат митохондриите, преминавайки през VDAC. Ако се установи, че случаят е такъв, изследвания като д-р Ростовцева могат да насочат към потенциални методи за намаляване на този страничен ефект. Откритията на нейния екип също могат да имат важни последици за лечението на многобройни неврологични заболявания, които, подобно на Паркинсон, са резултат от смъртта на неврони, включително ALS и болестта на Хънтингтън.
„Независимо дали използваме олезоксим или не за лечение на тези заболявания, проучвания като нашето ни показват къде да се фокусираме“, казва д-р Ростовцева. „VDAC не представлява особен интерес, защото е просто дупка, но от моя гледна точка VDAC и други протеини във външната мембрана на митохондриите са пренебрегнати. Ако нашата хипотеза е вярна, това означава, че трябва да фокусираме изследователската общност върху разглеждането на VDAC като фармакологична цел за лекарства. "
Абонирайте се за нашия седмичен бюлетин, за да бъдете в крак с последните пробиви в програмата за вътрешни изследвания на NIH.
[1] Молекулярен механизъм на медиирана от олезоксим невропротекция чрез насочване на взаимодействието на α-синуклеин с митохондриален VDAC. Rovini A, Gurnev PA, Beilina A, Queralt-Martín M, Rosencrans W, Cookson MR, Bezrukov SM, Rostovtseva TK. Cell Mol Life Sci. 2019 ноември 23. doi: 10.1007/s00018-019-03386-w.
[2] Защитна роля на олезоксима срещу индуциран от див тип а-синуклеин токсичност в човешки невронално диференцирани SHSY-5Y клетки. Gouarné C, Tracz J, Paoli MG, Deluca V, Seimandi M, Tardif G, Xilouri M, Stefanis L, Bordet T, Pruss RM. Br J Pharmacol. 2015 януари; 172 (1): 235-45. doi: 10.1111/bph.12939.
[3] Олезоксим (TRO19622): ново, насочено към митохондриите невропротективно съединение. Bordet T, Berna P, Abitbol J, Pruss RM. Фармацевтични продукти (Базел). 2010 февруари; 3 (2): 345-368. doi: 10.3390/ph3020345
- Royal canin ветеринарна диета избран протеин за възрастни pr суха храна за котки Превод на изследвания в
- Заглушаването на мастните протеини подобрява затлъстяването и кръвната захар - ScienceDaily
- NORI PROTOCOL Институт за хранителна онкология
- Диета Северна звезда - Безопасна и ефективна течна диета с високо протеинова програма за отслабване
- Метаболитна адаптация към диета с ниско съдържание на въглехидрати и протеини („Традиционна“) в Австралия