Изабел Комино
1 Departamento de Microbiología y Parasitología, Facultad de Farmacia, Universidad de Sevilla, c/Profesor García González 2, 41012 Севиля, Испания; Имейли: se.su@onimoci (I.C.); se.su@oneroml (M.L.M.); se.su@cra (A.R.)
Мария де Лурд Морено
1 Departamento de Microbiología y Parasitología, Facultad de Farmacia, Universidad de Sevilla, c/Profesor García González 2, 41012 Севиля, Испания; Имейли: se.su@onimoci (I.C.); se.su@oneroml (M.L.M.); se.su@cra (A.R.)
Ана Реал
1 Departamento de Microbiología y Parasitología, Facultad de Farmacia, Universidad de Sevilla, c/Profesor García González 2, 41012 Севиля, Испания; Имейли: se.su@onimoci (I.C.); se.su@oneroml (M.L.M.); se.su@cra (A.R.)
Алфонсо Родригес-Ерера
2 Instituto Hispalense de Pediatría, c/Guadalbullón 2, 41013 Севиля, Испания; Имейл: moc.airtaidepphi@zeugirdorosnofla
Франсиско Баро
3 Instituto de Agricultura Sostenible (C.S.I.C.), Alameda del Obispo s/n, 14004 Кордоба, Испания; Имейл: se.cisc.sai@orrabf
Каролина Соуза
1 Departamento de Microbiología y Parasitología, Facultad de Farmacia, Universidad de Sevilla, c/Profesor García González 2, 41012 Севиля, Испания; Имейли: se.su@onimoci (I.C.); se.su@oneroml (M.L.M.); se.su@cra (A.R.)
Резюме
Строгата безглутенова диета (GFD) е единственото налично в момента терапевтично лечение за пациенти с целиакия, автоимунно разстройство на тънките черва, свързано с трайна непоносимост към глутеновите протеини. Пълното елиминиране на глутеновите протеини, съдържащи се в зърнените култури, от диетата е ключът към управлението на цьолиакия. Това обаче поражда многобройни социални и икономически последици поради повсеместното присъствие на глутен в храните. Изследванията, представени в този преглед, се фокусират върху текущото състояние на алтернативните зърнени култури и псевдозърнени култури и техните производни, получени чрез естествен отбор, програми за размножаване и трансгенна или ензимна технология, потенциално толерирани от целиакия. Накрая описваме няколко стратегии за детоксикация на хранителния глутен. Те включват ензимно разцепване на глиадинов фрагмент от пролил ендопептидази (PEP) от различни организми, разграждане на токсични пептиди чрез покълване на зърнени ензими и трансамидиране на зърнени брашна. Тази информация може да се използва за търсене и разработване на зърнени култури с хлебните и хранителни качества на токсичните зърнени култури, но които не влошават това състояние.
1. Въведение
Целиакия е синдром на хранителна непоносимост, който, въпреки че е недостатъчно диагностициран, е едно от най-честите хронични стомашно-чревни разстройства. Развива се при генетично предразположени индивиди, при които неидентифицирани фактори на околната среда (инфекции, промени в микробната флора и др.) Могат да предизвикат непоносимост към глутен, съдържащ се в пшеница, ечемик, ръж и овес [1,2]. Глутенът е сложна смес от протеини, наречени проламини. Тази протеинова фракция има специфично наименование: пшеничните проламини се наричат глиадини и глутенини, ечемичните проламини са хордеини, ръжните проламини са секалин, а тези от овес са авенини. Обща характеристика на тези протеини е наличието на множество остатъци от пролин и глутамин, което ги прави устойчиви на стомашно-чревно храносмилане и по-изложени на дезаминиране от тъканната трансглутаминаза.
Идентифицирани са няколко епитопа, отговорни за токсичността на глутена, въз основа на способността им да стимулират пролиферацията на Т-клетки, реагиращи на глутен в биопсии на тънките черва, получени от целиакия. Като се има предвид само пшеницата, в базата данни с имунни епитопи (IEDB) [3] могат да бъдат намерени 190 Т-клетъчни стимулиращи епитопи, свързани с цьолиакия. От тях 94 епитопи са разположени в гени на α-глиадин, 74 в гени на γ-глиадин, 12 в гени на ω-глиадин, 8 в гени за глутенин с ниско молекулно тегло (LMW) и 2 в гени с високо молекулно тегло (HMW).
Най-приетият модел за обяснение на имунопатогенезата на цьолиакия е двусигналният модел, характеризиращ се с първи вроден имунен отговор и последващ вторичен адаптивен отговор, който ще стимулира хистологична лезия, характеризираща се с масивна интраепителна инфилтрация на лимфоцити, хиперплазия на криптите и вилозна атрофия [2]. Поглъщането на тези протеини води до възпаление, атрофия и хиперплазия на тънкочревните крипти на пациента с целиакия. Това заболяване обаче засяга не само червата, но е системно заболяване, което може да причини нараняване на кожата, черния дроб, ставите, мозъка, сърцето и други органи.
Целиакия преминава в ремисия, когато пациентите се поставят на диета за изключване на глутен и пациентите рецидивират, когато глутенът се въведе отново в диетата [1,2]. Спазването на GFD е трудно и засяга качеството на живот на пациентите, но строгата диета е от решаващо значение за намаляване на заболеваемостта и смъртността [4].
Глутенът има много специални характеристики, които благоприятстват използването му в различни хранителни продукти. Тъй като по време на производството на нишесте се генерира голямо количество глутен, той има относително ниска цена. Това може да се окаже проблематично за хората на GFD, тъй като глутеновите протеини могат да бъдат намерени в неочаквани източници като месо, риба или млечни продукти. Това е причината, поради която активно се търсят алтернативни подходи към GFD [5], които включват търсене и разработване на нови зърнени култури или глутен без или с ниско имуногенно съдържание. В тази статия ще разгледаме текущото състояние на алтернативните зърнени култури и техните производни, получени чрез естествен подбор, развъдни програми и трансгенна или ензиматична технология, които могат да бъдат толерирани от пациенти с цьолиакия.
2. Естествени сортове зърнени и псевдозърнени култури, подходящи за пациенти с целиакия
2.1. Пшеница и ечемик
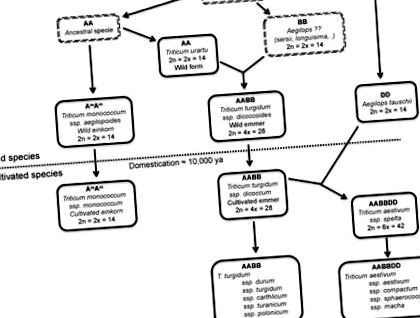
Култивираната пшеница е генетично много сложна поради произхода си от прародините диплоидни видове чрез процес на естествена хибридизация и последваща полиплоидизация. Двата вида пшеница със земеделско значение, макаронената пшеница и хлебната пшеница, са тетраплоидни (два генома, AABB) и хексаплоидни (три генома, AABBDD), съответно (Фигура 1). Тетраплоидите са възникнали в природата чрез спонтанна хибридизация на два диплоидни вида, всеки донорен геном А и В, между 0,5 и 2 милиона години. Хлябната пшеница (AABBDD) произхожда от полетата преди около 8000 години чрез спонтанна хибридизация между твърда пшеница (AABB) и Aegilops tauschii, диплоидният донор на генома D (Фигура 1).
Диаграма, показваща еволюционните връзки между видовете пшеница и сродните видове Aegilops. Пунктираната линия разделя дивите и опитомените видове пшеница. Предците или неизвестните видове са заобиколени от двойно пунктиран правоъгълник. Посочени са нивото на плоидност и броят на хромозомите. Номенклатура според ван Слагерен [8].
Един вид пшеница, Triticum aestivum, се използва предимно в съвременния индустриализиран свят, поради увеличеното производство на протеини, както и издръжливостта си в по-студен климат. Установено е също така, че протеините, които са най-имуногенни за цьолиакия, се намират във глиадиновата фракция на T. aestivum. Съществуват обаче почти 20 други вида пшеница, които или не се отглеждат от съвременните общества, или се отглеждат в избрани региони на света [6]. С толкова голям брой налични видове пшеница, значително количество изследвания са фокусирани върху изследването на различни видове и сортове пшеница като алтернатива на строга GFD за пациенти с целиакия [7].
Бяха извършени някои подходи за отстраняване на целиакия токсични протеини в ечемика. Двойно нулеви хибридни растения, до голяма степен лишени от В- и С-хордеини, са произведени чрез конвенционално кръстосване [16]. Ечемикът е диплоид и за разлика от ситуацията при хлебната пшеница, генетиката на хордеините е относително ясна. Има четири протеинови семейства на хордеини: В-, С-, D- и γ-хордеини, като В- и С-хордеините заедно представляват над 90% от ечемичните хордеини. Изолирането на двойно нулеви ечемични линии на хордеин от хибриди на Risø 56 и Risø 1508 е довело до линия, която не натрупва B- или C-хордеин и има само 3% от див тип хордеин, заедно с 20-кратно намаляване на реактивността в T -клетъчни анализи [16,17]. В допълнение, проведени проучвания показват, че някои линии за малцуване (Hordeum vulgare) са по-малко имуногенни в сравнение с дивите линии (Hordeum chilense) [18]. Тези открития биха могли да повишат перспективата за отглеждане на видове ечемик с ниски нива на вреден глутен и атрактивната цел за разработване на нетоксични сортове ечемик с потенциална употреба в производството на напитки, така консумирани по целия свят, както и бирите. Нищо обаче не е известно за вариабилността в целиакичната токсичност на други видове или разновидности на токсични зърнени култури като ръж.
2.2. Овес
Култивираният овес са хексаплоидни зърнени култури, принадлежащи към рода Avena L., който се среща в цял свят в почти всички селскостопански среди [19]. Напоследък овесът получава все по-голям интерес като човешка храна, главно защото зърнените култури могат да бъдат подходящи за консумация от пациенти с целиакия. Предлагат се няколко сорта овес. Той е богат източник на протеини, съдържа редица важни минерали, липиди, β-глюкан, полизахарид със смесени връзки, който формира важна част от диетичните фибри на овес, а също така съдържа различни други фитоконституенти като авенантрамиди, индол алкалоид - грамин, флавоноиди, флавонолигнани, тритерпеноидни сапонини, стерини и токоли. Традиционно овесът се използва отдавна и се счита за стимулант, спазмолитик, антитумор, диуретик и невротоник. Овесът има различни фармакологични дейности като антиоксидант, противовъзпалително, антидиабетно, антихолестеролемично и др. [20].
Сравнението на различните проучвания се усложнява от различните планове на изследването, различните условия, използвани при тестването, броя на участниците, включени във всяко изследване, и докладването на контрола на чистотата на овесения материал, използван в клиничните изпитвания. Друг релевантен фактор при различните дизайни е липсата на информация за използвания сорт овес. Silano et al. [25] изследва имуногенния ефект на авенините от четири сортове овес, използвайки периферни лимфоцити от пациенти с CD. Всички тествани сортове овес (Lampton, Astra, Ava и Nave) от тези изследователи са имуногенни с разлики в способността им да предизвикат отговор. Друго проучване обаче потвърждава, че Avena genziana и Avena potenza не показват in vitro дейности, свързани с CD патогенезата [26].
Съобщава се за полезността на G12 антителата за идентифициране на потенциално токсични сортове овес за пациенти с целиакия [27]. Тази констатация позволи класифицирането на сортовете овес в три групи въз основа на степента им на афинитет към G12 антителата: силно призната група, една с умерено разпознаване и такава без реактивност [27]. Тези резултати бяха потвърдени от MALDI-TOF, SDS-PAGE и Western blot, като показаха, че броят, относителната интензивност на върховете и протеиновият профил, получени за деветте сорта овес, се различават един от друг. Потенциалната имунотоксичност на различните видове овес се определя от Т-клетъчна пролиферация и освобождаване на интерферон γ. Реактивността, която Т-клетките, изолирани от пациенти с целиакия, проявяват с три сорта овес (по един от всяка от класифицираните групи) корелира директно с реактивността на moAb G12. Разнообразието, наблюдавано в реактивността спрямо различните сортове овес, предполага вариации в състава на авенина и следователно в количеството имунотоксични епитопи, подобни на 33-мерните, присъстващи в тези сортове. Това дава рационално обяснение защо само някои овес предизвикват имунологичен отговор.
В сравнение с пшеничните глиадини, авенините са малко проучени и броят на пълните гени на авенин, присъстващи в момента в базите данни, е ограничен и от няколко генотипа, така че вариабилността на гените на авенин в овеса не е добре представена. Наскоро е известно, че подобно на пшеницата, овесените зърна имат както мономерни, така и полимерни авенини [28]. Установена е пряка връзка между имуногенността на различните сортове овес и наличието на специфични пептиди с по-висока/ниска потенциална имунотоксичност, което може да обясни защо някои сортове овес са токсични за пациенти с целиакия, а други не [28]. Включването на някои сортове овес в хранителните продукти не само може да подобри хранителните качества, но също така може да осигури лечение на различни заболявания и би било приветствано от пациентите с цьолиакия.
2.3. Други зърнени и псевдозърнени култури
Добре известно е, че високата хранителна стойност на зърнените храни, съдържащи глутен, и вискоеластичната мрежа, генерирана от глутена, което позволява отлична аерирана структура в хранителните продукти. За разлика от тях, безглутеновите продукти на зърнена основа могат да бъдат богати на въглехидрати и мазнини и имат недостиг на макронутриенти и микроелементи. В резултат на това дългосрочното придържане към GFD може да предизвика недостиг на хранителни вещества. Предлагат се различни протеини като алтернатива както за ролята на полимера, така и за увеличаване на хранителната стойност на продуктите без глутен. Включването на други съставки/хранителни вещества като 3-омега липиди, специфични протеини и др. Е алтернатива за подобряване на хранителния състав на продукти без глутен.
Прави впечатление, че много зърнени култури (членове на семейство треви), които са тясно свързани с пшеницата, ръжта и ечемика, се считат за токсични въз основа на таксономията. Освен това, някои изследвания, фокусирани върху протеиновата хомология в зърната, подкрепят молекулярни доказателства [28,29]. Въпреки това, член, принадлежащ към други племена, които изглежда са свързани с царевица, се считат за безопасни (Фигура 2) и могат да служат като заместители и да осигурят брашна за готвене и печене за чувствителни към целиакия и глутен индивиди. Има изследвания на протеини в подкрепа на това заключение, въпреки че проучванията не са достатъчно пълни, за да предоставят повече от насоки.
- Ефектът на безглутенова диета върху аланин аминотрансфераза (ALT) при пациенти с целиакия
- Какво означава диета без глутен за пациентите с ХБН Национална бъбречна фондация
- Безглутеновата диета; Химия
- Тестовете за серумна трансглутаминаза и ендомизиални антитела не откриват повечето пациенти с целиакия
- Безглутеновата диетична прищявка или необходимостта от диабет