Инженерна наука, 2019, 8, 19-24
Публикувано онлайн: 04 април 2019 г.
Получено на 25 февруари 2019 г., Прието на 03 април 2019 г.
Бърза редукция на 4-нитрофенол, използвайки желатинов хидрогел, съдържащ сребърни наночастици
Mazhar Ul-Islam 1 *, Jawad Ali 2, Waliullah Khan 3, Adnan Haider 4, Nasrullah Shah 3, Md. Wasi Ahmad 1, Muhammad Wajid Ullah 5 * и Guang Yang 5 *
1 Департамент по химическо инженерство, Технически колеж, Университет Dhofar, Салала, Султанат Оман
2 Катедра по химия, Балочистански университет по ИТ, инженерни и управленски науки, Квета, Белуджистан, Пакистан
3 Катедра по химия, Университет Абдул Уали Хан, Мардан, Мардан, Пакистан
4 Катедра по химия, Университет за наука и технологии Кохат, Кохат, Хайбер Пахтунхва, Пакистан
5 Катедра по биомедицинско инженерство, Huazhong University of Science and Technology, Wuhan 430074, Китай
* Кореспонденция: Mazhar Ul-Islam ([имейл защитен])
Резюме:
Настоящото проучване отчита синтеза на желатинов хидрогел, съдържащ сребърни наночастици (AgNPs) и ролята му на катализатор. Порест желатинов хидрогел с размер на порите 15-100 nm се приготвя чрез охлаждане на неговия горещ разтвор до стайна температура с глутаралдехид като омрежител. Желатиновият хидрогел се потапя в 1 mM разтвор на сребърен нитрат за 24 часа чрез ex-situ импрегниране. Импрегнирането на AgNPs беше потвърдено чрез сканираща електронна микроскопия с полеви емисии (FE-SEM), която показа равномерно разпръскване на наночастици на повърхността на хидрогела и частично импрегниране в матрицата. Термогравиметричният анализ (TGA) показа импрегнирането на 9 тегловни% AgNPs в хидрогелния композит, което също допринесе за подобрените му топлинни свойства. Анализът с рентгенова дифракция (XRD) потвърждава аморфната природа на желатина и добавянето на AgNP. AgNPs/желатинов хидрогел ефективно редуцира 4-нитрофенола чрез натриев тетрахидроборат при константа на скоростта на реакцията от 0,498 min -1. Приготвените AgNPs/желатинов хидрогел могат да се използват като катализатор за други подобни видове реакции.
Съдържание
Ключови думи: Желатин; Хидрогел; Сребърни наночастици; Катализатор.
1. Въведение
Желатинът е известен на човечеството от 16-ти век. Понастоящем се използва за различни приложения във фармацевтичната, хранителната, биомедицинската и фотографската индустрия; следователно се произвежда в голям мащаб. Общата химическа структура на желатина е дадена на схема 1. Неговата химическа структура съдържа множество –NH2, NH и други кислородсъдържащи функционални групи, които взаимодействат с различни метални йони и наночастици за различни функционални приложения. 1–3 Желатинът се използва най-вече под формата на хидрогел, който представлява набъбнала омрежена мрежа от полимерни вериги. Неговите хидрогелове могат да побират до 95% тегловно вода. Няколко проучвания съобщават за използването на хидрогелове или хидрогел-образуващи полимерни покрития като хитозан, бактериална целулоза и карбоксиметил целулоза върху друг субстрат за използване на хостинг на каталитични метални наночастици. 4-8 В допълнение, желатиновите хидрогелове също са изследвани за проучванията за адсорбция и биосъвместимост. 9–11
В момента пречистването на отпадъчните води придобива все по-голям интерес, тъй като ежедневните дейности, извършвани от индустриите, замърсяват съседните водни тела 7,32, което пряко засяга живия организъм, зависим от тези водни тела. Например текстилната промишленост изхвърля токсични реактивни багрила в близките потоци. По същия начин фармацевтичната промишленост изхвърля токсични органични съединения във водните потоци като ароматни съединения. Тези съединения не само влияят на водните организми, но и налагат неблагоприятни ефекти върху местността. Следователно премахването им е от първостепенно значение, както предлагат природозащитниците. Сред различните техники, използвани за тяхното отстраняване, каталитичната трансформация на тези съединения в по-малко токсични съединения са едно от възможните решения на този проблем. За да се намалят разходите за каталитичния процес, е силно желателно да се възстанови катализаторът и да се използва повторно в друга партида.
Настоящото проучване имаше за цел да произведе импрегнирани с желатинов хидрогел сребърни наночастици чрез омрежване на глутаралдехид за приложение в катализа за редукция на 4-нитрофенол с натриев тетрахидроборат. Този произведен желатин/сребърен нанокомпозит беше оценен за неговите характеристики чрез катализиране на редукцията на 4-нитрофенол (4-NP) до 4-аминофенол (4-NP) във воден разтвор. Разработеният материал може да намери потенциални приложения като катализатор при разграждането на различни органични материали от промишлените отпадъци.
2. Експериментален раздел
2.1 Материали
Различните химически реактиви, използвани в настоящото проучване, включително желатинов прах, натриев тетрахидроборат, сребърен нитрат и 4-нитрофенол, са закупени от реномиран доставчик на химикали и са използвани без допълнителна обработка. Във всички експерименти се използва дейонизирана и дестилирана вода.
2.2 Приготвяне на желатинови хидрогелове
Двата различни хидрогела на желатина се приготвят в дейонизирана дестилирана вода. Накратко, 10 тегл.% Желатин се разтваря в дестилирана вода чрез нагряване при 60 ° С при непрекъснато разбъркване. След пълно разтваряне се добавя подходящо количество разтвор на глутаралдехид и се разбърква в продължение на 10 минути. Разтворът се охлажда до стайна температура, която в крайна сметка се превръща в хидрогел. Този хидрогел е използван в каталитичните изследвания. Подобна процедура беше приета за приготвяне на 3 тегл.% Разтвор. Този хидрогел се използва за изобразяване на наночастици.
2.3 Приготвяне на синтез на наночастици сребро и потапяне в желатинов хидрогел
За синтез на сребърни наночастици в желатинов хидрогел е използван метод на химична редукция. За приготвяне на сребърни наночастици в желатиновия хидрогел се използва 1 mM разтвор на сребърен нитрат. Обикновено 5 g хидрогел, приготвен по гореспоменатия метод, се потапят в 50 ml разтвор на сребърен нитрат за 5 h. След абсорбирането на йони на среброто хидрогелът се поставя във прясно приготвен 15 mM разтвор на натриев тетрахидроборат. Хидрогелът става тъмнокафяв веднага след потапяне в разтвор на редуциращ агент. Този хидрогел многократно се измива с дейонизирана дестилирана вода, за да се отстранят нереагиралите сребърни йони и наночастици от повърхността му.
2.4. Характеризиране
Морфологичните особености на лиофилизирания желатинов хидрогел и наличието на сребърни наночастици в неговата матрица бяха наблюдавани чрез сканиращ електронен микроскоп на полеви емисии (Hitachi S-4800 & EDX-350 (Horiba) FE-SEM (Токио, Япония). Преди наблюдение чрез FE-SEM, пробите бяха покрити с осмична киселина (OsO4) с VD HPC-ISW осмиево покритие (Токио, Япония). Рентгеновият анализ беше извършен с помощта на рентгенов дифрактометър (X'Pert-APD Philips, Холандия) с X- генератор на лъчи (3 kW) и анод (LFF Cu). Излъчването е CuK-α при 1,54Å, напрежението и токът на рентгеновия генератор са съответно 40 kV и 30 mA, а ъгълът на сканиране варира от 20 до 80 °. Термогравиметричният анализ (TGA) се извършва с помощта на термогравиметричен/диференциален термичен анализатор (Seiko Instruments Inc.). Обикновено в експеримента се използва проба от 5 до 10 mg (лиофилизирана). Пробата се нагрява при скорост на нагряване от 10 ° C на минута в запечатан керамичен държач за проби до 800 ° C в инертна атмосфера. За каталитичните експерименти беше използван UV-видим спектрофотометър (Thermo Scientific). За анализ, разтворът в кварцова кювета се поставя в държача за проби с еталонна кювета, съдържаща вода, за измервания.
2.5 Тестване на катализатора в реакция на редукция на модел
За да се изследва ролята на желатиновия хидрогел, съдържащ наночастици Ag като катализатор, той се смесва на малки парченца (под 1 mm) чрез многократно прилагане и освобождаване на натиска върху палеца върху него. Приготвя се 4-нитрофенол (4-NP) в дейонизиран дестилиран воден разтвор с концентрация 1,4 × 10 -4 М. След това се взимат 40 ml 4-NP разтвор в бехерова чаша, съдържаща 0,35 g желатинов хидрогел, поддържан Ag наночастици и се задържа в продължение на 3 минути. Редукционната реакция се инициира чрез добавяне на 0,5 g натриев тетрахидроборат в чашата. Към този момент приблизително 3 ml разтвор от мензура се подлагат на измервания с UV видима абсорбционна спектроскопия при постоянен интервал от време.
3. Резултати и дискусия
Химичната структура на желатиновите и Ag наночастици, импрегнирани желатинови влакна, е илюстрирана на схема 1. Разтварянето на две различни концентрации на желатин във вода разкрива, че желатинът с по-ниска концентрация е лесно разтворен в гореща вода при 60 ° C и образува бистър разтвор. Добавянето на омрежител улеснява процеса на образуване на гел и разтворът се превръща в хидрогел при охлаждане до стайна температура. Наночастиците Ag са включени в хидрогела чрез ex-situ импрегниране, където хидрогелът абсорбира сребърни йони от разтвор на сребърен нитрат заедно с процеса на синтез. По-нататъшното третиране на хидрогел с натриев тетрахидроборат намалява абсорбираните йони до Ag NPs в желатиновия хидрогел. Ag NPs, прикрепени към желатиновите влакна на повърхността, както и в матрицата.
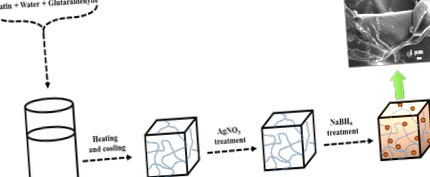
Схема 1 Илюстрация на (а) химична структура на желатин (б) образуване на неговия хидрогел, съдържащ импрегнирани Ag NPs и техния процес на приготвяне.
3.1 Морфологични особености на AgNPs/желатинов хидрогел
Фиг. 1 FE-SEM изображения на приготвения хидрогелен материал: (а) чист хидрогел при ниско и (б) при голямо увеличение и (в) AgNPs импрегниран желатинов хидрогел.
3.2 Термогравиметричен и рентгенов дифракционен анализ на AgNPs/желатинов хидрогел
Фиг. 2 показва TGA кривите на лиофилизиран чист желатин и AgNPs/желатинов хидрогел. TGA кривата показва три различни региона за отслабване. Първоначалната загуба на тегло, варираща около 7 до 8% и в двете проби, може да се отдаде на загубата на водни молекули. След това се наблюдава силна загуба на тегло в температурния прозорец от 220 ° C до 400 ° C в чиста желатинова проба, което може да се отдаде на разграждането на желатиновите полимерни вериги в пробата. След 455 ° С няма промяна в теглото и се получава краен остатък от 10%. В пробата AgNPs/желатин основната загуба на тегло започва при 260 ° С и продължава, докато се получи постоянно тегло от 19%. Разликата между теглото на желатина и AgNPs/желатина е около 9%. Тези наблюдения показват, че вградените наночастици леко повишават термичната стабилност на хидрогела. Освен това, TGA анализът дава доказателства за наличие на 9 тегловни% AgNPs в композитния хидрогел. Резултатите от TGA са приблизителни за количеството наночастици Ag в хидрогела. Подобен метод за сближаване на металните наночастици е докладван от няколко други проучвания. 4,15,33
Фиг. 2 TGA термограми от чист желатин и AgNPs/желатинови хидрогелове.
Фигура 3 представя моделите на XRD на лиофилизирани проби от желатин и AgNP/желатинов хидрогел. Желатинът е известен аморфен полимер; следователно не наблюдавахме никакъв дифракционен пик в XRD кривата на желатина, освен аморфен хало при 2-тета от 20 °. За разлика от това, XRD кривата на AgNPs/желатин показва няколко дифракционни пика, които могат да се отдадат на присъствието на Ag наночастици в хидрогела с кубична фазова кристална структура, както беше съобщено по-рано 15. Размерът на наночастиците се изчислява чрез уравнението на Scherrer, което се оценява на 22 nm.
Фиг. 3 Рентгенов дифракционен анализ на чистия желатин и AgNPs/желатинови хидрогелове.
3.3 Каталитични свойства на AgNPs/желатинов хидрогел
маса 1 Сравнение на AgNPs в каталитичната ефективност на желатинов хидрогел с други катализатори за намаляване на 4-NP.
- Композитни скелета, съдържащи копринен фиброин, желатин и хидроксиапатит за костна тъкан
- Дмитрий Медведев Бързи факти
- Можете ли да отслабнете, като разхождате жената от паунда - гнездото
- Диета за отслабване при спешни случаи, Acv Отслабване Fast -Camp Комо
- Gotoly Спортно облекло за отслабване за жени Бързо загряващо изгаряне на мазнини от тренировка Фитнес
