Ентералното хранене се отнася до всеки метод на хранене, който включва вливане на храна в стомашно-чревния тракт, като нормално хранене, хранене чрез назогастрална или назоентериална тръба или хранене в гастростома или ентеростомия (например така наречения PEG, перкутанна ендоскопска гастростомия ).
Свързани термини:
Изтеглете като PDF
За тази страница
Ентерално хранене
Въведение
Ентералното хранене включва директен достъп до стомашно-чревния тракт с тръба - тоест има телесна инвазия. Въпреки че обикновено се счита за еквивалентно на хранене, ентералното хранене се различава от простото хранене:
Ентералното хранене заобикаля нормалните хранителни механизми на обонянието, вкуса, дъвченето и преглъщането, както и цефалната фаза на храносмилането.
Ентералните формули обикновено са фиксирани, дефинирани и непроменени, за разлика от голямото разнообразие от хранителни вещества в храната.
Ентералното хранене е неволно или неволно и често се дава непрекъснато, за разлика от периодичния и доброволен прием на орална храна.
Ентералното хранене е свързано с рискове и усложнения.
Тази статия ще се фокусира върху епруветките и достъпа до стомашно-чревния тракт, видовете ентерални формули, индикациите, усложненията и взаимодействията между лекарства и формули.
Ентерално хранене
Андрю Р. Дейвис, Антъни Дж. Хенеси, в Cphical Care Nephrology (Трето издание), 2019
Потенциални рискове, свързани с ентералното хранене
Ентералното хранене обикновено се доставя в стомаха с назогастрална сонда, 27–29 и в много случаи това води до задоволително доставяне на хранене. Въпреки това, стомашната моторика (особено изпразването на стомаха) и абсорбцията са нарушени при критично заболяване, 30–32 и това може да доведе до ентерална непоносимост към хранене. 33
Съобщава се, че непоносимост към ентерално хранене се наблюдава при 31% до 46% от пациентите със стомашно хранене 33,34 и обикновено се проявява с големи стомашни остатъчни обеми и повръщане. 27,33,35 Това води до голям брой пациенти, които не постигат очакваните си изисквания за доставка на енергия 36 и изглежда, че излагат пациентите на по-висок риск от пневмония и вероятно смъртност. 33 Това често се влошава при критично болни пациенти, когато им се отказва ентералното хранене за диагностични и терапевтични процедури.
Управлението на потенциалната непоносимост към ентерално хранене чрез забавяне на започването на назогастрално хранене е нелогично, тъй като това ще намали шанса пациентът да отговори на енергийните изисквания, може да влоши чревната пропускливост 37 и може да доведе до увеличени инфекциозни усложнения и продължителност на престоя в болницата. 4 Следователно има много по-голяма обосновка за по-проактивни стратегии, като например използването на основана на доказателства насока за хранене, която включва използването на промоционални лекарства и хранене в тънките черва, когато пациентите развият характеристики на непоносимост. 5
Ентерално хранене
Метаболитни усложнения
Ентералното хранене води до много по-малко метаболитни усложнения, отколкото парентералното хранене. Най-честото метаболитно усложнение на ентералното хранене вероятно е хипергликемия, особено при пациенти с вече съществуваща непоносимост към глюкоза. Това може да се постигне чрез по-строг контрол на диабета. Хипергликемията рядко налага намаляване на храненето.
Формулите за хранене с тръби с висока енергийна плътност или съдържание на протеини не съдържат достатъчно вода, за да могат някои пациенти да се справят с натоварването с разтворени бъбреци. Пациентите, получаващи тези формули, които не са в състояние да регулират доброволно нуждите си от течности и нямат достатъчен интравенозен прием на течности, могат да станат дехидратирани, хиперосмоларни и хипергликемични. Осмоларността на формулата не е свързана с тези проблеми, тъй като въглехидратите (основният осмотичен компонент) се метаболизират и не допринасят за натоварването на бъбречното разтворено вещество, освен когато възникне гликозурия. Състоянието на течности и нивата на глюкоза в кръвта на пациентите в риск трябва да бъдат внимателно наблюдавани.
Ентерално хранене
D.L. Вайцберг, Р.С. Torrinhas, в Encyclopedia of Food and Health, 2016
Формулиране
EN може да се прилага периодично или непрекъснато. Изборът на път за прилагане на ЕН и видът на инфузията, която ще се въздейства, ще повлияят върху дизайна на формулировката му. Това включва също определяне на общия период за прилагане на диетата, обема за вливане, скоростта на вливане, ако ще се използва гравитационно капково и под каква форма ще бъде осигурен (инфузионна помпа или чрез болус). Таблица 2 очертава програмирането на EN според позиционирането на захранващата тръба в пред- или постпилорно местоположение.
Таблица 2. Програмиране на EN според позиционирането на тръбата за подаване
| Стомах | Позволява доставяне на голям обем | Хиперосмоларните разтвори се понасят, но колкото по-висока е осмолалността на разтвора, толкова по-бавно се изпразва стомаха | Зависи от общия обем/ден и толерантността на пациента. Може да се използва по-ниско фракциониране (четири до шест пъти на ден) и по-голям обем във всяка доставка | Около 120 капки в минута (или време (мин) = общ обем (ml)/6) от началото на терапията |
| Постпилорна | По време на периодично подаване, обемът не трябва да надвишава 300 ml h - 1 при адаптирани пациенти | По-добра толерантност за формулировки с по-малко от 550 mOsm l - 1; капенето на хиперосмоларни разтвори трябва да се контролира стриктно чрез използване на инфузионна помпа | Непрекъснато или периодично фракциониране, обикновено между шест и осем доставки на ден на всеки 3 часа | Начална фаза: 60 капки/мин (или време (мин) = общ обем (мл)/3); „Адаптирана“ фаза: 120 капки в минута (или време (мин) = общ обем (ml)/6) |
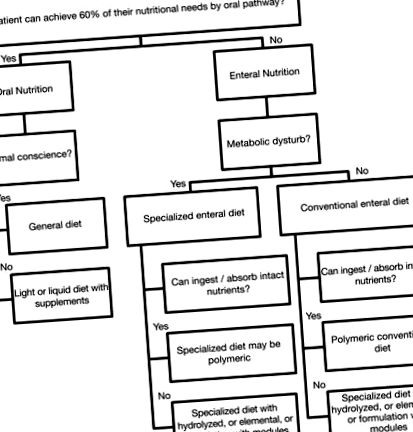
Ентералните формулировки трябва да бъдат хранително пълноценни, когато се използват като изключително хранене или като добавка към пациенти с нормално перорално поглъщане; или хранително непълни, когато се използват само като добавка към храненето. Оценката на храносмилателната и абсорбционната способност на пациента трябва да се извърши за по-добър избор на ентерална формула ( Схема 2 ).
Схема 2. Планиране за избор на ентерални диети.
Няколко ентерални формулировки се основават на прясна храна, преработена храна или както прясна, така и преработена храна. Следователно хранителните вещества, съдържащи EN, обикновено са същите съставки на нормалната диета, консумирана по орален път, включително въглехидрати (40–60% от общите енергийни нужди), протеини (14–20% от общите енергийни нужди), мазнини (15–30% енергийни нужди) и фибри (40–20 gl - 1). Трябва да се имат предвид различни фактори, за да се улесни изборът на най-подходящата ентерална формулировка за пациенти с индикация EN, като калорийна плътност, осмоларност и осмолалитет, път на приложение, източник и сложност на хранителните вещества и заболяване.
EN калоричната плътност (kcal ml - 1) трябва да се основава на общите калорични нужди на пациента спрямо обема на ентералните диети, които трябва да се прилагат на ден. Ентералните диети с по-висока енергийна плътност имат по-малко количество вода, което може да варира от 690 до 860 ml l - 1 диета. Категоризацията на ентералните формули, според нейната енергийна плътност, е показана в Таблица 3 .
Таблица 3. Категоризиране на ентералните формули според енергийната му плътност
| Много ниско | 1.5 | Рязко хиперкалоричен |
Доставката на витамини и минерали варира в зависимост от специфичните нужди на пациентите и тяхното заболяване. В специфичните хранителни нужди трябва да оцените индикацията за допълнителни добавки с микроелементи, дори когато съставът сам по себе си постига стойностите, препоръчани от Препоръчителната диетична добавка (RDA). Клиничната хранителна оценка на пациента трябва да включва обективни и/или субективни показатели, за да се идентифицира възможно най-рано всеки риск от специфичен дефицит на микроелементи, за да бъде незабавно коригиран и/или предотвратен.
Някои специализирани и много специфични формулировки за конкретна клинична ситуация (напр. Бъбречна недостатъчност) са недостатъчни за някои доставки на витамини и минерали. Следователно, EN диетичното планиране отчита необходимостта от добавяне или не на тези микроелементи. При продължителна употреба на непълно ентерално хранене трябва да се посочат допълнителните витамини и минерали.
При пациенти със синдроми на малабсорбция изследвайте възможния дефицит на мастноразтворими витамини (A, D, E и K), за да го коригирате скоро. Липсват конкретни препоръки за витамини и минерали за критично болни пациенти. Въпреки това, при такова състояние нуждите от антиоксидантни хранителни вещества се увеличават поради оксидативния стрес и се препоръчва да се добавят витамини А, С и Е, цинк и селен.
EN осмоларността (mmol l - 1 разтвор) и осмоларността (mOsm kg - 1 вода) са свързани с неговата храносмилателна толерантност. Въпреки че стомахът понася диети с по-висока осмолалност, по-дисталните части на стомашно-чревния тракт реагират по-добре на формулировки на изосмолари. Следователно, хиперосмоларните диети, инфузирани чрез гастростомия или назогастрална сонда за хранене, имат по-добра храносмилателна толерантност в сравнение с приложението чрез постпилорни или йеюнални сонди.
Хранителните вещества, които най-много влияят на осмоларността на разтвора, са прости въглехидрати (моно- и дизахариди), които имат по-голям осмотичен ефект от въглехидратите с по-високо молекулно тегло (нишесте); минерали и електролити, поради свойството на дисоциацията му на по-малки частици (например натрий, калий и хлорид); хидролизирани протеини; кристални аминокиселини; както и средноверижните триглицериди, тъй като те са по-разтворими от дълговерижните триглицериди. Колкото повече хидролизатни компоненти съдържат състава, толкова по-висока е неговата осмолалност.
Ентералните диети не трябва да надвишават стойността на натоварването на бъбреците с разтворени вещества, поносимо от бъбреците (800–1200 mOsm, при нормална ситуация). Натоварването с разтворени бъбреци може да бъде изчислено чрез добавяне на 1 mOsm за всеки mEq натрий/калий/хлорид и 5,7 mOsm (възрастни) или 4 mOsm (деца) за всеки грам протеин от неговата формула. Специално внимание трябва да се обърне на критични клинични ситуации, като сепсис, следоперативна, политравма и тежко изгаряне, където урината става много гъста, с висока осмолалност (около 500–1000 mOsm kg - 1), дори при подходяща хидратация.
Важното е, че влиянието на осмоларността на лекарството обикновено се пренебрегва. Средната осмоларност на течните лекарства, прилагани през устата или чрез епруветка за хранене, варира от 450 до 10 950 mOsm kg - 1 вода. Някои прояви на стомашно-чревна непоносимост могат да бъдат свързани с лекарството, въпреки че често се приписва на ентерална формулировка.
В специфични клинични ситуации може да има изисквания за промяна във видовете използвани хранителни вещества; количеството и/или формата трябва да бъдат представени. В такива случаи хранителната терапия става по-специализирана. Тези адаптации включват промени от обикновен източник на хранителни вещества, използвани до неговите физикохимични и структурни модификации. По този начин, специализираните формулировки за ентерално приложение могат да осигурят различни източници на витамини, минерали, въглехидрати, липиди и протеини и тези хранителни вещества могат да бъдат представени изцяло или хидролизирани (изцяло или частично) структура.
Някои специализирани формулировки на EN са част от имунонутрицията. Имунонутрицията е хранителна интервенция, която изследва конкретната активност на различни хранителни вещества за облекчаване на възпалението и модулиране на имунната система, в която са включени омега-3 мастните киселини, аргинин, глутамин, нуклеотиди и антиоксиданти. Понастоящем има консенсус, че периоперативното имунонутриция може да бъде от полза за елективни хирургични пациенти, особено за тези с недохранване, подложени на големи стомашно-чревни операции. При тези пациенти приложението на ентерални диети, съдържащи n-3 PUFA, нуклеотиди и аргинин, допринася за намаляване на следоперативните инфекциозни и неинфекциозни усложнения и трябва да се започне 5-7 дни предварително (500–1000 ml на ден - 1) и да се поддържа в следоперативния период.
Въпреки че ползата от използването на тази ентерална формула, комбинираща различни хранителни вещества с имуномодулиращи функции, е добре установена при хирургични пациенти, липсват данни за потвърждаване или насочване на ефективното и безопасно използване на ентерални диети, съдържащи изолирани имунонутриенти в различни клинични популации, включително аргинин и глутамин. При хемодинамично стабилно състояние аргининът може да предложи имунологични и метаболитни ползи, но участието му в синтеза на азотен оксид може да представлява потенциален риск за септично болни. Ентералният глутамин трябва да се има предвид за лечение на пациенти с изгаряния и жертви на травми, но няма достатъчно доказателства за употребата му при критично болни пациенти с отказ на множество системи.
Други хранителни вещества, които могат да съставят специализирани EN формулировки, включват аминокиселини с разклонена верига (BCAA). BCAA осигуряват основно гориво за скелетните мускули по време на стрес и сепсис. Следователно, левцин, изолевцин и валин могат да бъдат добавени към специализирани формули на EN като допълнителни метаболитни източници, за да отговорят на метаболитните нужди на скелетните мускули по време на хиперметаболитни състояния.
ВЪНШНО ХРАНЕНЕ
Гастростомично хранене
Пациентите, които се нуждаят от дългосрочно или постоянно ентерално хранене, трябва да бъдат обмислени за поставяне на епруветка за гастростомия или бутон за гастростомия (по-малък уред, който е почти изравнен с кожата). Техниката на перкутанна ендоскопска гастростомия (PEG) е добре установена процедура за осигуряване на ентерална хранителна подкрепа. Въпреки че хранителната гастростомия може да бъде поставена хирургично, PEGs се сравняват благоприятно, с по-ниска заболеваемост и цена; хирургичната гастростомия изисква лапаротомия и обща анестезия, докато ПЕГ се извършва под местна упойка с помощта на оптичен ендоскоп. Предлагат се набор от PEG комплекти за кърмачета, деца и възрастни. Храненето на йеюностомия може да се разглежда като средство за осигуряване на ранна следоперативна хранителна подкрепа при избрани пациенти и може да се използва за краткосрочна или дългосрочна подкрепа.
Ентерално хранене
Изследвания на наркотици
Систематични прегледи
Изключително ентерално хранене при деца с болест на Crohn’s
4.1 Типичен ексклузивен протокол за ентерално хранене
EEN включва използването на изключителен период от течна диета за период до 8 седмици, с изключване на нормалната диета през този период. 15,35 Потенциалната роля на EEN възниква от описателни проучвания преди повече от 4 десетилетия: тези доклади и серии от случаи илюстрират подобрен възпалителен статус при възрастни пациенти, управлявани с хранителна намеса. 36–40 Рандомизирано контролирано проучване, сравняващо EEN и кортикостероиди (CS) при възрастни с активен CD: в това ирландско проучване EEN и CS се извършват по подобен начин. 41 Въпреки че многобройни последващи проучвания показват ползи от EEN при възрастни, много по-нови доклади показват, че EEN е по-ефективен при деца. 18,42
Хранене при критично болни пациенти
5 Кога трябва да се започне EN при критично болни пациенти?
Ранният ЕН обикновено се определя като започване на ентерално хранене в рамките на 48 часа от приема на интензивно отделение. Много RCT са сравнявали ранния EN с забавения прием на хранителни вещества при критично болни пациенти, получаващи механична вентилация, и когато тези резултати са били обобщени, ранният EN е бил свързан с тенденция към намаляване на смъртността и значително намаляване на инфекциозните усложнения. Ранното стартиране на EN изглежда не влияе върху продължителността на механичната вентилация или продължителността на престоя на интензивното отделение. Наличието на чревни звуци и преминаването на плоскост не са необходими преди институцията по EN.
Хранителна поддръжка: Възрастни, Ентерално
Определение
Ентералното хранене е метод за осигуряване на хранителни вещества директно в стомашно-чревния тракт, когато човек не може да приема храна през устата. Използва се при пациенти, които имат адекватна функционална стомашно-чревна система и могат да усвояват и абсорбират храна, но при които приемът през устата е недостатъчен за поддържане или възстановяване на оптимален хранителен статус. Известно също като хранене с тръба, ентералното хранене (EN) доставя хранителни вещества директно в стомаха или червата чрез тънка гъвкава тръба. Прилага се през назогастрална сонда, поставена през носа, или през кожата, поставена в стомаха (гастростомия) или тънките черва (йеюностомия). EN обикновено се счита за по-безопасен и предпочитаният метод за осигуряване на хранителна подкрепа над парентералното хранене. В тази статия се разглежда използването на ентерално хранене.
Подкрепа за храненето на възрастен пациент с рак
HEIDI J. СРЕБЪРНО,. GORDON L. JENSEN, в Nutritional Oncology (Второ издание), 2006
Показания
EN обикновено се предоставя на пациенти с рак на главата, шията и горната част на стомашно-чревния тракт в остри, общностни и дългосрочни грижи, когато пациентите не могат да дъвчат, преглъщат, усвояват и/или абсорбират адекватно, за да отговорят на нуждите от хранителни вещества. Една от основните причини EN да се предпочита пред PN е, че EN е по-физиологичен; EN поддържа бариерната функция на лигавицата на червата и предотвратява ендогенната чревна бактериална транслокация. Например, Jiang et al. (2003) рандомизира 40 пациенти с рак на стомаха или дебелото черво в група EN или PN след резекция на тумора. Пациентите са получавали изокалорични и изонитрогенни формули, инициирани 3 дни следоперативно. Чревната пропускливост е измерена чрез екскреция на лактулоза и манитол с урината след приложение на постоперативните дни 1, 7 и 12. Съотношението лактулоза/манитол е значително по-ниско в групата на EN на 7 и 12 ден, което показва повишена цялост на лигавицата на червата.
В проучване, проведено от Bozzetti et al. (2001), 317 пациенти с рак на стомашно-чревния тракт от 10 институции в Италия са разпределени на случаен принцип за изокалорични и изонитрогенни EN или PN разтвори за 1 седмица след операцията. Пациентите с ЕН са имали значително по-малко общи и инфекциозни усложнения. Освен това средната продължителност на болничния престой за групата с EN е била почти наполовина по-малка от тази на групата с PN (съответно 5,7 ± 2,9 срещу 10,4 ± 4,5 болнични дни).
Също така е общоприето, че EN е по-рентабилен от PN (ASPEN, 2002). Само няколко проучвания обаче сравняват разходите за EN с PN и единственото, проведено изключително с пациенти с рак, е гореспоменатото проучване на Braga et al. (2001). Подобно на други проучвания, основният фокус на тези изследователи беше да сравнят разходите за EN и PN решение. Брага и сътр. (2001) изчислява, че използването на EN вместо PN би спестило $ 65 на ден. В ретроспективно сравнение на разходите, свързани с домашния EN (HEN) с домашния PN (HPN) въз основа на таксите за Medicare през 1996 г., Reddy and Malone (1998) установяват, че средните годишни разходи на пациент за EN решения ($ 9535 ± 13,980) са около една пета от цената на PN решения ($ 55,193 ± 30,596). И все пак, всички разходи както за EN, така и за PN могат да бъдат по-големи от съобщените, тъй като биха обхванали други разходи като поставяне на захранващата тръба или катетър, заем за инфузионна помпа, комплект за администриране и превръзка, както и разходи за проследяване грижи, включително спешен кабинет, посещение на лекарски кабинет или клиника, домашни медицински сестри и други професионални терапевтични грижи, медикаментозна терапия, лабораторни такси и болнични реадмисии.
- Целулит - общ преглед на ScienceDirect теми
- Царевичен глутен - общ преглед на ScienceDirect теми
- Century Egg - общ преглед на ScienceDirect теми
- Фосфомицин - общ преглед на ScienceDirect теми
- Хранителна добавка - общ преглед на ScienceDirect теми