Катедра по молекулярна ендокринология и метаболизъм, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Катедра по молекулярна ендокринология и метаболизъм, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Катедра по молекулярна ендокринология и метаболизъм, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Катедра по молекулярна ендокринология и метаболизъм, Токийски медицински и дентален университет, Bunkyo-ku, Токио 113-8510, Япония
Катедра по молекулярна ендокринология и метаболизъм, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Катедра по молекулярна ендокринология и метаболизъм, Токийски медицински и дентален университет, Bunkyo-ku, Токио 113-8510, Японски център за медицинско обслужване и връзки, Tokyo Medical and Dental University, Bunkyo-ku, Tokyo 113-8510, Япония
Катедра по превантивна медицина и метаболизъм, Висше училище по медицински и дентални науки, Токийски медицински и дентален университет, Bunkyo-ku, Токио 113-8510, Япония, Катедра по диабет, ендокринология и хематология, Медицински център Dokkyo Medical University Saitama Medical Center, Koshigaya, Saitama 343 -8555, Япония
Отдел по медицинска генетика, Медицинска болница на Медицинския и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Отдел по медицинска генетика, Медицинска болница на Токийския медицински и зъболекарски университет, Bunkyo-ku, Токио 113-8510, Япония
Катедра по педиатрия и биология на развитието, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Катедра по педиатрия и биология на развитието, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Център за медицинска генетика, Медицински факултет на университета Keio, Shinjuku-ku, Токио 160-0016, Япония
Катедра по ендокринология, хематология и геронтология, Медицински факултет, Университет Чиба, Чиба, Чиба 260-0856, Япония
Катедра по ендокринология, хематология и геронтология, Медицински факултет, Университет Чиба, Чиба, Чиба 260-0856, Япония
Катедра по молекулярна ендокринология и метаболизъм, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
Катедра по молекулярна ендокринология и метаболизъм, Медицински и дентален университет в Токио, Bunkyo-ku, Токио 113-8510, Япония
2020 年 67 巻 2 号 стр. 211-218
- Публикувано: 2020 г. Получено: 2019/06/05 Издадено на J-STAGE: 2020/02/28 Прието: 2019/10/15 [Предварително публикуване] Издадено: 2019/11/08 Преработено: -
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> 1]. Тези пациенти показват или почти пълна, или частична липса на мастна тъкан. Има четири вида липодистрофия; вродена генерализирана липодистрофия ( CGL), фамилна частична липодистрофия (FPLD), придобита генерализирана липодистрофия (AGL) и придобита частична липодистрофия (APL) [2 Brown RJ, Arujo-Vilar D, Cheung PT, Dunger D, Garg A, et al. (2016) Диагнозата и управление на синдроми на липодистрофия: насоки за практиката на много общества. J Clin Endocrinol Metab 101: 4500–4511.
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> 2]. Наследяването на CGL е автозомно рецесивно, докато FPLD е автозомно доминиращо, а AGL и APL са по-чести сред жените. Пациенти с генерализирана липодистрофия имат лептинов дефицит, вторичен до почти пълна загуба на мастна тъкан, което е свързано с тежка форма на метаболитни нарушения, характеризиращи се с дислипидемия, затлъстяване на черния дроб, инсулинова резистентност и диабет.
Мутации в A/C ламинат (LMNA) генът причинява прогероидни синдроми, които често придружават генерализирана липодистрофия. Те са известни като автозомно доминиращ синдром на прогерия на Hutchinson-Gilford (HGPS) [3 Hennekam RC (2006) Синдром на прогерия Hutchinson-Gilford: преглед на фенотипа. Am J Med Genet A 140: 2603–2624.
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> 5]. Разпространението е изключително ниско и няма очевидна полова разлика.
Наскоро Хусейн и др. съобщава за някои случаи на APS с de novo хетерозиготен LMNA c.29C> T; p.T10I мутация. Тези пациенти имат клинични характеристики, различни от другите видове APS, които включват тежки метаболитни нарушения като захарен диабет, дислипидемия и безалкохолно мастно чернодробно заболяване. Следователно те наричат този нов синдром като генерализиран прогероиден синдром, свързан с липодистрофия (GLPS) [6 Hussain I, Patni N, Ueda M, Sorkina E, Valerio CM, et al. (2018) Нов генерализиран прогероиден синдром, свързан с липодистрофия, дължащ се на повтарящи се хетерозиготни LMNA p.T10I мутация. J Clin Endocrinol Metab 103: 1005–1014.
Заместителната терапия с метрелептин драстично подобрява инсулиновата резистентност и дислипидемия при пациенти с генерализирана липодистрофия [7 Oral EA, Simha V, Ruiz E, Andewelt A, Premkumar A, et al. (2002) Лептинова заместителна терапия за липодистрофия. N Engl J Med 346: 570–578.
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> 8]. Ефектите на метрелептин върху тестостерона, както и неговото въздействие върху скелетната мускулна маса, остават неясни. случай на GLPS с метаболитни аномалии и опишете промените в апетита, хормоните и телесния състав веднага след (малко след това, две седмици след това и т.н.) и също така една година след започване на лечението с метрелептин.
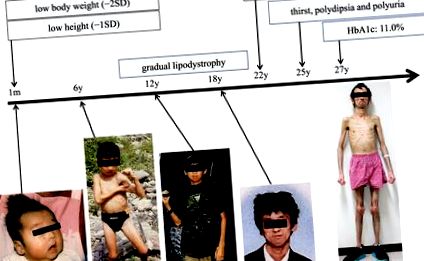
28-годишен японец беше приет в нашата болница заради липодистрофия. Той имаше нормален ръст (51,5 см) и тегло (3296 г) при раждането. Умерено забавяне на физическия растеж се наблюдава още на едномесечна възраст, но по това време не се наблюдават видими психични или хормонални нарушения (Фиг. 1 Времеви ход на растежа и клинични находки за настоящия случай.
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> 2). Генерализираната липодистрофия стана явна около началото на пубертета, но медицински преглед, когато беше на около 20 години, не показа метаболитни аномалии. От 25-годишна възраст той развива повишена жажда, полидипсия и полиурия и посещава общата клиника по вътрешни болести на 28-годишна възраст. Последващите прегледи разкриват, че той вече е развил хипергликемия и дислипидемия (HbA1c: 9,7–10,1%, HOMA -IR: 5.64, TG: 281–783 mg/dL). До този момент той нямаше значителна минала медицинска история, няма известна фамилна анамнеза и не е имал кръвни връзки в роднините си (Фиг. 3 Семейно родословие на настоящия случай.
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> Фиг. 3). Неговата височина, телесно тегло и индекс на телесна маса бяха 153,6 cm, 28,3 kg и 11,9 kg/m 2, Той имаше нисък ръст, птичи фации с клюн на носа, претрупване на зъбите поради микрогнатия, частично посивяване и загуба на коса и висок глас, всички от които са типични характеристики на APS. Нямаше значителна кожа аномалии и съвместни контрактури.Лабораторни данни за прием (на гладно)
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> Таблица 1 показва лабораторните данни за прием (на гладно). Неговият гликиран хемоглобин (HbA1c) е 11,0%. Серумна аспартатна трансаминаза (AST ), нивата на аланин аминотрансфераза (ALT) и γ-глутамилтрансфераза (γ-GTP) са съответно 40, 81 и 65 IU/L, което показва умерена чернодробна дисфункция. Серумните нива на триглицеридите (TG) са 158 mg/dL. нива на лептин (2,2 ng/ml, нормални: 2,4–25,0) и намалени нива на общия тестостерон в серума (1,90 ng/ml). Неговите вторични сексуални характеристики са нормални. Липса на срамни или аксиларни косми, намалено либидо и дисфункция на ерекцията или еякулацията не е налице. Ултрасонографията на корем показва мастен черен дроб, а магнитно-резонансната томография показва липсата както на подкожна, така и на висцерална телесна мазнина (Фиг. 4T-1, претеглена магнитно-резонансна томография, показваща липсата както на подкожна, така и на висцерална маст.
"data-html =" true "data-position =" bottom "data-toggle =" tooltip "> Фиг. 5), което показва, че е имал GLPS. Извършено е и цялостно секвениране на родителите на родителите му и не е открита мутация. Електрокардиограма и е извършена ултракардиография, тъй като пациентите с GLPS често страдат от сърдечно-съдови заболявания, но нито едно изследване не разкрива сърдечни аномалии. Подходящата диетична терапия след хоспитализация веднага подобрява значително кръвната му глюкоза, но изглежда трудно да продължи диетичната терапия извън болницата поради хиперфагия започва инжектиране на метрелептин [1,2 mg (0,04 mg/kg)/ден]. Малко след заместването на метрелептин той усеща намалени усещания за глад преди хранене и подобрено усещане за ситост след. На 13-ия ден от лечението значително подобрение в дневните вариации на са наблюдавани нива на серумна глюкоза, триглицериди, инсулин и плазмен глюкагон (Фиг. 6 Дневни вариации на (A) глюкоза, (B) инсулин, (C) глюкагон и (D) триглицерид e нива непосредствено преди и 12 дни след започване на лечението с метрелептин. E: Площ под кривата на нивата на глюкоза, инсулин, глюкагон и триглицериди.
"data-html =" true "data-Position =" bottom "data-toggle =" tooltip "> Фиг. 6). Освен това се наблюдават повишени нива на серумен тестостерон (4.15 ng/ml). От друга страна, серумното лутеинизиране нивата на хормона (LH) са леко повишени, от 1,5 mIU/ml до 1,6 mIU/ml. След 1 година монотерапия с инжектиране на метрелептин неговият HbA1c е 5,3%, серумните нива на TG са 86 mg/dL, серумните нива на AST са 20 IU/L и серумните нива на ALT са 12 IU/L, което показва, че метаболитните му профили са подобрени чрез монотерапия с лептин. Серумното ниво на тестостерон (3,73 ng/ml) остава повишено, а нивата на LH се повишават (2,7 mIU/ml) след 1 година от лечение с метрелептин.Освен това, леко увеличение на индекса на скелетната мускулатура, от 3,42 до 3,45 kg/m 2, се наблюдава според рентгеновата абсорбциометрия с двойна енергия (индекс на скелетните мускули; ASM/височина 2, нормално:> 6,87. ASM; апендикулярна скелетна мускулна маса, сумата от мускулните маси на четирите крайника).
Времеви ход на растежа и клинични находки за настоящия случай.
Диаграма на растежа на пациента от раждането до 18-годишна възраст. Затворените червени кръгове показват височината (горния панел), а затворените червени квадратчета показват телесното тегло (долния панел).
- Случай на камъни от стагхорн в бъбрек с илеален уретер, лекуван чрез перкутанна нефролитотомия
- Синдром на автопивоварната Определение, симптоми и др
- Агресивна аневризмална костна киста във връзка с полиостозна фиброзна дисплазия Доклад за случай -
- 10 диетични съвета за синдром на раздразнените черва (IBS) Carlisle Digestive
- 36-годишен мъж, страдащ от панкреатит и история на скорошно начало на случая с орлистат