Тексаски институт за черния дроб, Сан Антонио, Тексас
University of Texas Health San Antonio, San Antonio, TX
Naim Alkhouri, M.D., Texas Liver Institute, 607 Camden Street, San Antonio, TX 78215. E-mail: [email protected] Потърсете още статии от този автор
Тексаски институт за черния дроб, Сан Антонио, Тексас
Тексаски институт за черния дроб, Сан Антонио, Тексас
University of Texas Health San Antonio, San Antonio, TX
Naim Alkhouri, MD, Texas Liver Institute, 607 Camden Street, San Antonio, TX 78215. E-mail: [email protected] Потърсете още статии от този автор
Тексаски институт за черния дроб, Сан Антонио, Тексас
Потенциален конфликт на интереси: N.A. получи финансиране за изследвания от Intercept Pharmaceuticals, Allergan и Gilead Sciences. Той е в бюрото за лектори на Intercept Pharmaceuticals и Gilead Sciences.
Резюме
Гледайте видео презентация на тази статия
Съкращения
Безалкохолната мастна чернодробна болест (NAFLD) е най-честата причина за чернодробно заболяване в западните страни, като засяга приблизително 20% до 30% от хората в САЩ. 1, 2 NAFLD има хистологичен спектър, който варира от относително доброкачествения неалкохолен мастен черен дроб (NAFL), до агресивната форма на неалкохолен стеатохепатит (NASH), до NASH с напреднала фиброза/цироза, водеща до чернодробно чернодробно заболяване. 2, 3
Тъй като няма одобрено от САЩ Агенция по храните и лекарствата (FDA) лечение за NAFLD, за пациентите се препоръчват промени в начина на живот. В проспективно проучване върху ефектите от загубата на тегло върху NAFLD, загубата на тегло ≥10% води до регресия на фиброзата при 45% от пациентите и отзвучаване на NASH при 90% от пациентите. 4 Въпреки това, в това проучване само 10% от пациентите са успели да отслабнат ≥10%, което показва спешната необходимост от разработване на нови фармакологични лечения извън модификациите на начина на живот.
Напоследък засиленото разбиране на патогенезата на болестта доведе до разработването на множество медицински терапии за NAFLD, насочени към различни пътища на заболяването. Този преглед ще обсъди четири лекарства, които са във фаза III рандомизирани контролирани проучвания (RCT): елафибранор, обетихолова киселина (OCA), ценикривирок (CVC) и селонсертиб (SEL). Важно е да се отбележи, че хистологичните крайни точки за всяко проучване от фаза III са малко по-различни, което изключва сравнението на резултатите от главата до главата. И накрая, ще се опитаме да предоставим на читателите нов начин на мислене, който сравнява спектъра на NAFLD с този на диабет тип 2 (T2D), за да стратифицира пациентите с NAFLD и да вземе решение за подходящия курс на лечение.
Агонист на активирания от пероксизом пролифератор рецептор
Рецепторите, активирани от пероксизомен пролифератор (PPAR), са активирани от лиганд транскрипционни фактори, които регулират метаболитните процеси. 2, 5 PPARα е повсеместно експресиран 5 и регулира липидния метаболизъм и енергийната хомеостаза в множество органи. 2 PPARδ се експресира в метаболитно активни тъкани, включително черния дроб, където играе роля за изместване на чернодробния метаболизъм към липидно окисление. 2, 5
Elafibranor е двоен агонист на PPARα/δ, който подобрява хомеостазата на глюкозата, увеличава метаболизма на инсулина и намалява възпалението. RCT от фаза IIb (NCT01694849/GOLDEN-505) оценява ефектите на елафибранор (120 mg/ден, 80 mg/ден или плацебо) в продължение на 52 седмици. 6 Основната крайна точка беше обръщането на NASH без влошаване на фиброзата; резултатите обаче не са статистически значими. След post hoc анализи с модифицирана дефиниция на първичния изход, по-голям дял от пациентите в групата с елафибранор (120 mg/ден) видяха резолюция на NASH в сравнение с тези в групата на плацебо (19% срещу 12%, P = 0,045). Актуализираната дефиниция на разделителната способност на NASH подчертава балонирането на хепатоцитите и определя влошаването на фиброзата като всяко едноетапно увеличение.
Фаза III RCT (NCT02704403/RESOLVE-IT) включва пациенти, за да се оцени ефекта на елафибранор (120 mg/ден или плацебо) върху хистологичното подобрение, определено като разделителна способност на NASH, без влошаване на фиброзата на 72 седмици с по-продължително проследяване за оценка неговите ефекти върху свързаната с черния дроб заболеваемост и смъртност.
Farnesoid X Receptor Agonist
Farnesoid X рецепторите (FXR) са транскрипционни фактори на ядрените рецептори, експресирани в черния дроб, които регулират инсулиновата чувствителност и участват в липидния метаболизъм. 7 Жлъчните киселини (BAs), естествени лиганди на FXR, 7 се синтезират в черния дроб и насърчават инсулиновата чувствителност и намаляват глюконеогенезата и циркулиращите триглицериди, когато са свързани с FXR. 8
OCA (6-етилхенодезоксихолевата киселина) е синтетичен BA и FXR активатор. 9 RCT от фаза IIb (NCT01265498/FLINT) оценява OCA (25 mg/ден или плацебо) в продължение на 72 седмици за лечение на хистологично доказан NASH. Основният резултат е подобрение на чернодробната хистология без влошаване на фиброзата. 9 Хистологичното подобрение е постигнато при 45% от пациентите в групата с OCA в сравнение с 21% от групата на плацебо (P = 0,0002); подобрение на фиброзата се наблюдава при 35% от групата с OCA в сравнение с 19% от плацебо (P = 0,004). Разделителната способност на NASH обаче не се различава в групата OCA (22%) и плацебо групата (13%) (P = 0,08). 9
Понастоящем RCT от фаза III (NCT02548351/REGENERATE) записва пациенти с доказан с биопсия NASH, за да оцени ефекта на OCA (10 mg/ден, 25 mg/ден или плацебо) в продължение на 72 седмици върху чернодробната хистология. Пациентите също ще бъдат проследявани в продължение на 6 години, за да се оценят тежки резултати като прогресия до цироза, нужда от чернодробна трансплантация и смърт.
Хемокин (C-C мотив) рецептор тип 2/5 антагонист
Възпалителният отговор на увреждане на хепатоцитите води до чернодробна фиброгенеза. Този отговор активира клетките на Kupffer (KCs) и чернодробните звездни клетки (HSC) в допълнение към набирането на макрофаги и моноцити. KCs, моноцитите и HSCs експресират хемокин (C-C мотив) рецепторни типове 2 (CCR2) и 5 (CCR5), които насърчават възпалителния отговор при чернодробно увреждане. 10
CVC, двоен антагонист на CCR2 и CCR5, демонстрира антифибротични ефекти в предклинични модели. Понастоящем RCT от фаза IIb (NCT02217475/CENTAUR) оценява ефектите на CVC (150 mg/ден или плацебо) върху лечението на NASH с чернодробна фиброза. Основната крайна точка е хистологичното подобрение без влошаване на фиброзата. 11 След 1 година лечение разликата в хистологичното подобрение не е била статистически значима между CVC групата и групата на плацебо, съответно 16% спрямо 19% (P = 0,52). Когато се анализира една от вторичните крайни точки - подобряване на фиброзата с поне един етап - поотделно, повече от CVC групата (20%) постигнаха подобрение на фиброзата в сравнение с плацебо групата (10%) (P = 0,02). 11.
RCT от фаза III включва пациенти с NASH за оценка на ефектите на CVC (150 mg/ден или плацебо) върху чернодробната фиброза (NCT03028740/AURORA).
Инхибитор на киназа 1, регулиращ сигнала за апоптоза
Регулиращата сигнала на апоптоза киназа 1 (ASK1) е член на семейството на активираната от митоген протеин киназа киназа киназа, която играе роля в реакциите на стрес. 12 Активирането на ASK1 от оксидативен стрес води до чернодробно възпаление, апоптоза на хепатоцитите и фиброза. 2
SEL (GS ‐ 4997) е селективен инхибитор на ASK1. Проведена е фаза II RCT (NCT02466516) за оценка на ефектите на SEL (6 или 18 mg/ден) самостоятелно или в комбинация със симтузумаб (125 mg/седмица) при пациенти с NASH и фиброза в продължение на 24 седмици. Симтузумаб, хуманизирано моноклонално антитяло, е посочен като неефективен при лечение на фиброза и се счита за плацебо. 13 Пациентите, лекувани със SEL, са имали повече подобрение на фиброзата; 43% от групата на 18 mg SEL и 30% от групата на 6 mg SEL се подобриха в сравнение с 20% от групата на симутумаб (плацебо).
Понастоящем две проучвания фаза III включват пациенти с NASH и свързваща фиброза (NCT03053050/STELLAR ‐ 3) и компенсирана цироза (NCT03053063/STELLAR-4), за да се оценят ефектите на SEL (6 mg/ден, 18 mg/ден или плацебо) с планиран междинен анализ на 48 седмици за оценка на хистологичното подобрение.
Предефиниране на спектъра на NAFLD: NAFLD е новият диабет тип 2
Дори с разработването на ефективни одобрени от FDA терапии за NAFLD, няколко проблема могат да забавят рутинната им употреба в клиничната практика. Основният въпрос е, че NAFLD е много често срещана и повечето пациенти имат относително по-малко прогресиращата форма, NAFL. Това кара много лекари от първичната помощ да вярват, че NAFLD не е сериозно заболяване, което изисква лечение. Идентифицирането на пациенти с NASH/напреднала фиброза все още изисква чернодробна биопсия, което не е осъществим вариант за заболяване, което засяга една трета от общото население в Съединените щати.
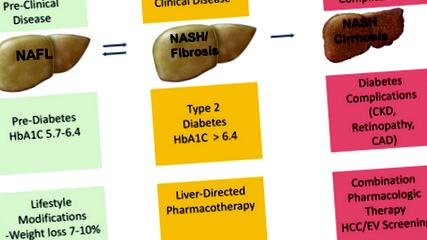
Ние вярваме, че бъдещото управление на спектъра NAFLD ще се развие по подобен модел на текущото управление на спектъра T2DM (фиг. 1). Бихме искали да сравним NAFL с преддиабет, който не е заболяване само по себе си, а рисков фактор за развитие на T2DM. Основата за управление както на NAFL, така и на преддиабет са модификациите на начина на живот. NASH се счита за движеща сила за развитието на чернодробна фиброза и евентуално цироза; следователно ние считаме NASH за сериозно заболяване, което налага агресивно медицинско управление с различни фармакологични агенти, подобни на това, което се изисква за пациенти с T2DM. И накрая, развитието на NASH цироза с усложнения на порталната хипертония показва увреждане на крайния орган на черния дроб. Това е подобно на развитието на инсулинозависим диабет и неговите макро-съдови и микроваскуларни усложнения и изисква най-агресивен подход към лечението.
Новите образни технологии вече позволяват диагностика на най-важното място при NAFLD и стадиране на чернодробна фиброза, което най-вероятно ще се превърне в новия „хемоглобин A1c“ (HbA1C) на хепатолога за рисково стратифициране на пациентите в различни категории на тежест на NAFLD.
Заключение
Тъй като разпространението и клиничната тежест на NAFLD се увеличава, необходимостта от одобрено от FDA лечение се засилва. В момента десетки лекарства са в клинични изпитвания, за да се идентифицира най-ефективното лечение. Терапиите се различават по своя механизъм на действие, като се фокусират върху метаболитни цели, противовъзпалителни ефекти или антифибротични ефекти. Elafibranor, OCA, CVC и SEL са четири от лекарствата, подложени на фаза III RCT (обобщени в таблица 1). Продължаващите изследователски усилия гарантират, че възможностите за лечение скоро ще станат достъпни.
| Елафибранор | PPARα/δ агонист | Да | Не | RESOLVE ‐ IT | 120 mg/ден | 72 седмици |
| OCA | FXR агонист | Не | Да | РЕГЕНЕРИРАЙТЕ | 10-25 mg/ден | 72 седмици |
| CVC | CCR2/CCR5 антагонист | Не | Да | ПОЛЯРНО СИЯНИЕ | 150 mg/ден | 52 седмици |
| SEL | ASK1 инхибитор | Не | Да А а Числово по-високи нива на подобрение на фиброзата, които не достигат статистическа значимост. Това беше доказателство за концепция, което не беше способно да открие хистологични промени в стадия на фиброза. | STELLAR 3 и 4 | 6 и 18 mg/ден | 48 седмици |
- а Числово по-високи нива на подобрение на фиброзата, които не достигат статистическа значимост. Това беше доказателство за концепция, което не беше способно да открие хистологични промени в стадия на фиброза.
- 1 Townsend SA, Newsome PN. Статия за преглед: нови лечения при безалкохолна мастна чернодробна болест . Aliment Pharmacol Ther 2017; 46: 494 - 507 .
Брой пъти цитирани според CrossRef: 17
- Chang-hua Zhang, Bu-gao Zhou, Jun-qing Sheng, Yang Chen, Ying-qian Cao, Chen Chen, Молекулярни механизми на чернодробна инсулинова резистентност при неалкохолно мастно чернодробно заболяване и потенциални стратегии за лечение, Фармакологични изследвания, 10.1016/j.phrs .2020.104984, (104984), (2020).
Оценка на терапевтичния потенциал на Cenicriviroc при лечението на неалкохолен стеатохепатит с фиброза: Кратък доклад за възникващи данни
- 12 стратегии за отстраняване на мастни чернодробни заболявания - пазари на начин на живот
- Асоциация на юношеското затлъстяване с неалкохолната мастна чернодробна болест и свързаните с нея рискови фактори в
- Основан на доказателства преглед на употребата на статини при пациенти с безалкохолна мастна чернодробна болест
- Ползите от упражнения при безалкохолни мастни чернодробни заболявания поради повишената автофагия
- Може ли ограничаването на приема на фруктоза да намали мастната чернодробна болест при деца Blog AGA Journals