Резюме
Заден план
Въздействието на диетата с ниско съдържание на протеини върху храненето при диабетици с ХБН е несигурно.
Методи
Метаболитните и хранителни ефекти на диета с ниско съдържание на протеини (0,5–0,6 g/kg/d), нормално-висока енергия (30–35 kcal/kg/d), допълнена с кетокиселини (LPD-KA), са оценени проспективно при пациенти с ХБН. с (DM) и без (non-DM) захарен диабет.
Резултати
Записани са 197 пациенти на стадии 3–5 с ХБН. DM (н = 81) и не-DM (н = 116) са сравними за пол (мъже 58 срещу 55%), възраст (66 ± 9 срещу 63 ± 18 години), бъбречна функция (eGFR 23 ± 13 срещу 24 ± 13 ml/min). След 6 месеца серумна урея (DM: 131 ± 58 до 105 ± 49 mg/dl, стр 2) и албумин (
Заден план
През последните десетилетия разпространението на хроничните бъбречни заболявания (ХБН) се увеличи в световен мащаб, крайният стадий на бъбречно заболяване (ESRD) се превърна в една от основните причини за смъртност в света и се очаква използването на бъбречна заместителна терапия да се удвои до 2030 г. [12]. Освен това се оказа, че диализата не е в състояние да удължи живота, докато за разлика от това намалява качеството на живот и индивидуалния функционален капацитет при повечето пациенти [3]. Следователно, в допълнение към популационни стратегии за предотвратяване на ESRD, ефикасно консервативно лечение за пациенти, страдащи от ХБН, които не са на диализа. Хранителното лечение е основна част от консервативното лечение на недиализната ХБН, целяща да намали метаболитните нарушения на ХБН, признаците и симптомите на уремия и прогресията на бъбречното заболяване и може да забави диализата [4]. Следователно диетата с ниско съдържание на протеини, която е крайъгълният камък на хранителното лечение на ХБН, играе централна роля в консервативното управление на ХБН [5].
Захарният диабет (СД) бързо се увеличава по целия свят и се очаква да се развие диабетна нефропатия при четири от десет пациенти със СД, представляващи основната причина за ХБН; наистина, около един над трима пациенти с ХБН е засегнат от диабет [14]. Следователно диета с ниско съдържание на протеини, допълнена с кетокиселини, може да бъде ресурс за пациенти с ХБН с диабет, но тези пациенти са по-възпалени, устойчиви на инсулин, коморбидни, хиперкатаболни и, поне на теория, може да се наложи повече протеини и аминокиселини компенсират катаболния статус [15]. Следователно, ограничена диета, като диетата с ниско съдържание на протеини - LPD, може да не осигурява достатъчно количество хранителни вещества и енергия и в резултат на това може да увеличи риска от PEW. Освен това, поради намаленото количество енергия в резултат на по-ниския прием на протеини, LPD съдържа повече въглехидрати, за да достигне енергийната заявка, а високите въглехидрати могат да влошат контрола на диабета. Данните за безопасност относно връзката между продължителната употреба на протеиново ограничение и PEW при диабетична ХБН са оскъдни. Това наблюдателно, проспективно проучване, насочено към оценка на ефектите на LPD, допълнена с кетокиселини върху дългосрочния хранителен резултат при пациенти с ХБН с диабет.
Методи
Пациенти и групи
Това е наблюдателно, проспективно проучване, проведено в бъбречната клиника на Centro de Atención Nutricional Fresenius Kabi в град Мексико, Мексико. Последователни амбулаторни пациенти с недиализно хронично бъбречно заболяване (ХБН) на редовна нефрология и хранително проследяване са включени в периода между 1 януари 2010 г. и 1 август 2013 г .; краят на проследяването беше на 31 август 2015 г. Протоколът за изследване, включващ тези пациенти, беше одобрен от местния етичен комитет, „Comité Local de Investigación y Ética del Hospital de Especialidades Centro Médico Nacional la Raza del Instituto Mexicano del Seguro Social“ и всички участници, включени в проучването, дадоха своето информирано съгласие за участие в изследването.
Критериите за подбор бяха: а) възраст ≥ 18 години; б) CKD етап 3 или по-висок според прогнозната GFR; в) проследяване от най-малко 6 месеца в клиника за ХБН; д); стабилна бъбречна функция (вариация на eGFR 2 и серумен албумин 2, независимо от стойността на албумина или неволно телесно тегло - намаляване на телесното тегло> 7,5% през последните 3 месеца); з) невъзможност за спонтанно хранене; и) всяко остро заболяване през предходните 3 месеца.
Дизайн на изследването и хранително лечение
Избраните пациенти са били наблюдавани за период на включване преди окончателното записване. Ако критериите за включване бяха потвърдени, пациентите бяха подложени на диетологична оценка и им беше предписана диета с ниско съдържание на протеини, допълнена с кетокиселини (LPD-KA), съдържаща 0,5–0,6 g протеини/kg iBW/ден, малко количество пурини, натрий (2 ( kg/m 2) Измерва се също обиколката на талията и ханша и се изчислява съотношението W/H.
Съставът на тялото се изчислява чрез анализ на биоимпеданса - BIA, като се използва многочестотен анализатор на състава на тялото (PLUSAVIS 333; честотен диапазон: 5–50-250 kHz; Jawon Medical Co. Ltd; Корея). Мерките са взети с пациент, облечен само в рокля. Електродите бяха поставени на краката и двете ръце. Обектът трябваше да бъде в пост-абсорбиращо състояние и беше поставен в стандартизирани условия: тиха среда, околна температура 22–24 ° C [19, 20]. Оценените променливи, получени от BIA, са обща телесна вода (TBW) и маса без мазнини (FFM); маслената маса (FM) се изчислява като разлика между BW и FFM.
Мускулната сила се измерва с цифров динамометър за ръкохватка (T.K.K. 540.1 ГРИП D; Takei Scientific Instruments Co. Ltd.; Ниигата, Япония). Мерките бяха взети от доминиращата страна. Пациентът стоеше изправен; той/тя е бил помолен да задържи устройството с индикатора за захващане, насочен навън, да остави ръката естествено надолу и накрая да захване захвата с пълна сила за 3 s. В рамките на половин минута са взети три мерки и се отчита средната стойност.
Статистика
Статистическите анализи бяха извършени с помощта на статистическия софтуер SPSS версия 22 (IBM SPSS Statistics). Непрекъснатите променливи са изразени като средно ± стандартно отклонение (SD), а категориалните променливи са изразени като процент. По време на анализа пациентите са групирани в диабетици (DM) и без диабет (non-DM). Сравнение на всички параметри на изходно ниво и в края на проследяващите периоди и сравнение на промените в параметрите по време на проучването между групите бяха извършени от несдвоен студент т-тест. Сравнението в групата беше направено от сдвоен студент т-тест, ANOVA или хи-квадрат-тествайте според случая. За да проверим дали диабетът е свързан с промени по време на дългосрочното проучване на основните клинични и хранителни параметри (телесно тегло, кръвно налягане, мускулна сила, серумни нива на урея, пикочна киселина, фосфати и албумин), направихме множество регресионни анализи. За всеки параметър поотделно изградихме мултивариативен модел, включващ вариацията по време на проследяването (окончателно-базална делта), коригирана за същия параметър на изходно ниво, диабет и потенциални смутители, т.е. индивидуалните характеристики, различаващи се между групите на изходно ниво (пол, възраст и eGFR). Двуопашка P стойност
Резултати
Пациенти
Сред изследваните пациенти бяха изключени тези, които отказаха хранителното лечение или декларираха, че не могат да се придържат към LPD или не отговарят на критериите за включване; тези пациенти не са подложени на по-нататъшна оценка.
Двеста и девет пациенти бяха избрани въз основа на първоначалните критерии за включване; след периода на включване, 197 пациенти (DM = 81; non-DM = 116) са включени в проучването, започвайки диета с ниско съдържание на протеини, допълнена с кетокиселини - LPD-KA. Всички пациенти са завършили 6-месечния диетичен период (краткосрочно наблюдение). След това 86 пациенти не продължиха LPD-KA; сред останалите 111 пациенти, продължили диетата, 47 не са достигнали минимално проследяване от 24 месеца в края на проучването. В обобщение, 64 пациенти (DM = 29; non-DM = 35) са останали на LPD-KA в продължение на 2 години или повече, със средно проследяване от 38 месеца (дългосрочно наблюдение).
Краткосрочно наблюдение
При включените пациенти средната възраст е била 64 години, а мъжете - 57%. Бъбречните заболявания са тип-1 = 6% и тип-2 = 94% при захарен диабет (DM) и хипертония = 59%, гломерулен нефрит = 3%, интерстициален нефрит = 8%, други/неизвестни = 31% при не-DM групи. Средната бъбречна функция, измерена чрез eGFR, е 23,5 ml/min при 25, 43 и 32% от пациентите в стадии на ХБН 3, 4 и 5, съответно. С изключение на бъбречното заболяване, няма разлика между групите (Таблица 1). Пациентите, изключени от проучването след периода на въвеждане, имат подобни характеристики.
Диетичното лечение води до няколко значителни метаболитни промени при всички пациенти (Таблица 2). Както се очаква, серумната урея, която беше малко по-различна сред групите на изходно ниво (стр Таблица 2 Клинично и лабораторно проследяване на пациенти с ХБН на диета с ниско съдържание на протеини и кетокиселини, последвано в краткосрочен план (6 месеца)
Хранителният статус и телесният състав, оценени чрез комбинацията от няколко параметри на обща клинична употреба, са сходни сред групите в началото и не са по-лоши след интервенцията (Таблица 3). Серумен албумин, който е бил намален при пациенти със СД спрямо не-СД в началото (стр Таблица 3 Хранително проследяване на пациенти с ХБН на диета с ниско съдържание на протеини и кетокиселини, последвано в краткосрочен план (6 месеца)
Промени в телесното тегло при пациенти с ХБН на диета с ниско съдържание на протеини и кетокиселини през краткосрочен период (6 месеца); −---- = Захарен диабет; _____ = не захарен диабет
Според справките за ръкохватка (долен праг: съответно 30 и 20 кг за мъже и жени [21]), мускулната форма е лоша при всички пациенти и дори по-намалена при диабетици; разликите между диабетиците и не-СД са сходни за половите подгрупи (Таблица 3). По време на диета с ниско съдържание на протеини, мускулната сила се е увеличила в DM, но не и в групата, която не е DM; по-конкретно, наблюдава се лека клинична тенденция за спад при мъжете без диабет (около 5%) и увеличаване при всички жени (около 5%) и мъжете с диабет (около 8%), със сходни крайни нива или за цялата СД и NON-DM групи или мъжките подгрупи (Таблица 3).
Дългосрочно наблюдение
64 пациенти (DM = 29; non-DM = 35) на LPD-KA са проучени за период по-дълъг от 2 години (38 ± 13 месеца). Диабетичната група беше малко по-възрастна и имаше леко по-ниска бъбречна функция с повече пациенти в стадий 5 на ХБН; тези разлики обаче не бяха значителни (Таблица 4).
По време на дългосрочното проследяване LPD-KA имаше сходни метаболитни ефекти, отколкото в краткосрочен план (Таблица 5). От значение е намаляването на серумната урея и фосфатите (стр Таблица 5 Клинично и лабораторно проследяване на пациенти с ХБН на диета с ниско съдържание на протеини и кетокиселини, последвано в дългосрочен план (най-малко 2 години)
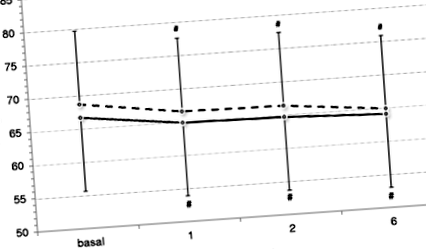
Същите ефекти върху хранителния статус се запазват и по време на дългосрочния LPD-KA. Албумините са почти нормални и стабилни (Таблица 6). Телесно тегло (фиг. 2) значително (стр Таблица 6 Хранително проследяване на пациенти с ХБН на диета с ниско съдържание на протеини и кетокиселини, последвано в дългосрочен план (най-малко 2 години)
Промени в телесното тегло при пациенти с ХБН на диета с ниско съдържание на протеини и кетокиселини в дългосрочен период (3 години); −---- = Захарен диабет; _____ = не захарен диабет
По време на дългосрочната диета LPD-KA, мускулната сила беше подобна на краткосрочното наблюдение, с по-ниски стойности при диабетици и сравними разлики между групите и подгрупите; по време на дългосрочното последващо сцепление с ръце остана по същество непроменено (Таблица 6). Като цяло мускулната сила на изходно ниво е под прага за саркопения [21], съответно при 83 и 69% пациенти със СД и не-СД; по време на проучването той леко се подобри, като съответно 79 и 54% при последното наблюдение.
Процентът на промените спрямо изходното ниво на клиничните и хранителни параметри по време на дългосрочното проследяване не се различава между групите: телесно тегло: - 3,9 ± 7,6 срещу -4,4 ± 8,5%; кръвно налягане: - 2,1 ± 15,3 срещу - 0,2 ± 12,2; мускулна сила: 4,8 ± 20,0 срещу 3,9 ± 18,5; урея: - 2,8 ± 58,5 срещу -1,8 ± 40,0; пикочна киселина: - 11,0 ± 35,7 срещу -6,1 ± 55,8; фосфати: - 7,7 ± 18,5 срещу -3,3 ± 19,8; албумин: 1,9 ± 13,4 срещу -2,0 ± 10,7; съответно за DM и non-DM (всички p = NS).
Многобройните регресионни анализи разкриват, че пол, възраст eGFR и диабет не са предсказвали промените в хранителните и клиничните параметри по време на проучването. Всъщност състоянието на диабет не е свързано значително с промени в телесното тегло (P = 0,636), кръвно налягане (P = 0,291), мускулна сила (P = 0,416) и серумни нива на урея (P = 0,273), пикочна киселина (P = 0,229), фосфати (P = 0,568) и албумин (P = 0,243).
Разхищение на протеинова енергия
Спазването на предписанията за диета обикновено е ниско в клиничната практика [22]. Косвените данни категорично предполагат, че в това проучване приемът на диети е бил достатъчен и по-специално приемът на протеини е намален, както се доказва от намалените нива на серумната урея, а енергийният прием остава постоянен, тъй като телесното тегло е непроменено в дългосрочен план нагоре.
За да получим цялостна оценка на загубата на протеинова енергия, ние приложихме интегрирания алгоритъм, предложен от Международното дружество за бъбречно хранене и метаболизъм, който включва четири различни категории хранителни критерии с цел ранното идентифициране на хранителния риск и навременното диагностициране на PEW в ХБН (Таблица 7) [6]. Преобладаването както на нисък ИТМ (2), така и на намален серумен албумин (Таблица 7 Цялостно загуба на протеинова енергия - PEW, посредством разпространението на основните хранителни параметри, по време на проследяването при пациенти с ХБН на нискобелтъчна диета и кетокиселини
Дискусия
Това проучване предоставя доказателства, че диетата с ниско съдържание на протеини, допълнена с кетокиселини при пациенти с ХБН с диабет, е хранително безопасна. В кохорта от добре подхранени, възрастни амбулаторни пациенти с умерена до напреднала ХБН на редовна нефрологична помощ, диета с ниско съдържание на протеини подобри метаболитния контрол на уремия и диабет. Телесното тегло намалява скоро след започване на диетична интервенция с ниско съдържание на протеини, но впоследствие остава стабилно във времето и, което е важно, мускулната годност е стабилна или дори се подобрява с течение на времето; не са наблюдавани допълнителни хранителни отклонения или промени в телесния състав и не са настъпили разлики между диабетици и недиабетици. Като цяло при пациенти с диабет с ХБН диета с ниско съдържание на протеини, допълнена с кетокиселини, подобрява широкия метаболитен профил и не влошава хранителния статус и телесния състав.
Диетата с ниско съдържание на протеини има по-високо съдържание на въглехидрати, за да компенсира по-ниското енергийно количество, произтичащо от намаленото съдържание на протеини в храната и да достигне адекватен енергиен прием [4]. Освен това метаболизмът на глюкозата при ХБН е нарушен поради намалена инсулинова чувствителност [27]. Следователно, по-високите диетични въглехидрати и дефицитът на глюкозна хомеостаза заедно могат да доведат до влошаване на контрола на диабета при ХБН. От друга страна, приемът на ниско съдържание на протеини увеличава медиираното от инсулина отстраняване на глюкоза; наистина, при пациенти с ХБН пост-абсорбционните плазмени нива както на глюкозата, така и на инсулина намаляват след диета с много ниско съдържание на протеини (с високо съдържание на въглехидрати), допълнена с кетокиселини, което показва възстановяване на инсулиновата чувствителност и подобряване на глюкозния толеранс [28]. Възможен механизъм е предложен от скорошно експериментално проучване, показващо, че дефектната секреция на инсулин при ХБН е свързана с плазменото ниво на урея, демонстрирайки, че циркулиращата урея директно уврежда секрецията на инсулин от панкреатичните островчета [29].
Допълнителна промяна в телесния състав, открита по време на проучването, е малък спад на мастната маса. Масата без мазнини намалява със същата степен и в двете групи, но такъв спад може да се дължи на загубата на вода в тялото; наистина, частичното FFM не намалява по време на диетата. Обратно, мускулната функционалност, оценена по силата на ръкохватката, се подобри в DM, но не и в DM по време на проследяването на LPD-KA. Интересното е, че саркопенията, определена от силата на ръкохватката и скелетната мускулна маса, оценена от BIA, е показана като независим предиктор за смъртността при ХБН [42]; според прага за сила на ръкохватка, в това проучване саркопенията, оценена чрез мускулна сила, е била широко разпространена на изходно ниво и леко подобрена по време на проучването [21].
Като се има предвид наблюдателният дизайн на проучването и малките разлики между групите на изходно ниво, не можем да изключим, че неизмерените смутители и състоянието на диабетици биха могли да повлияят на хранителния ефект на диетата LPD-KA. Въпреки това, няколко мултивариативни анализа категорично предполагат, че диабетът изглежда не играе роля върху хранителните ефекти, наблюдавани по време на дългосрочното наблюдателно проучване.
Заключение
- Нова инжекция помага за загуба на тегло при пациенти със затлъстяване и диабет, разкрива проучване UK News Sky News
- Безопасност и ефективност на амоксицилин при лечението на възпалително акне
- RIBOFLAVIN Потребителски оценки за ефективност, странични ефекти, безопасност и взаимодействия - WebMD
- Безопасност на лечението с чревния гел с Levodopa-Carbidopa при пациенти с напреднала болест на Паркинсон
- PHENIBUT Потребителски оценки за ефективност, странични ефекти, безопасност и взаимодействия - WebMD