Резюме
Програмирането е процес, при който стимул или стрес в критичен или чувствителен период на развитие има трайно или за цял живот значение. Последните проучвания при хора и животни предоставят убедителни доказателства, че вътреутробната среда може да окаже влияние върху процесите на развитие на плода и може да промени хомеостатичните регулаторни механизми сред потомството. Един от принципите на гестационното програмиране е наблюдението, че физиологичните ефекти на вътреутробната пермутация могат да варират в зависимост от периода на развитие на плода или новороденото и от вида. Програмирането може да доведе до промяна на броя на клетките, структурата на органите, хормоналните зададени точки и генната експресия, наред с други. Ефектите могат да бъдат постоянни или изразени само в избрани възрасти (напр. Новородено, възрастно) и могат да зависят от вътреутробната среда (напр. Хранене, глюкокортикоиди). Освен това, изразяването на физиологични аномалии може да присъства по време на базални условия или да се ограничава до стрес от околната среда или болестни състояния при потомството.
Добре известно е, че генетичните мутации в популациите на видовете могат да осигурят предимство за оцеляване, било за насърчаване на растежа на популацията при статични условия на околната среда, или за осигуряване на оцеляване при дългосрочни промени в околната среда. Генетичните мутации обикновено изискват продължителни еволюционни периоди от време, за да повлияят на популацията на вида. Освен това е вероятно мутациите да бъдат обратими или бързо приспособими към променящите се условия на околната среда. И обратно, перинаталното програмиране може да осигури полза за оцеляването на видовете, улесняващо различни фенотипове на потомството, които са приспособими към промените в състоянието на околната среда, които могат да решават или обръщат често.
По време на еволюцията и развитието хората и животните са били изложени на стрес на околната среда, като сушата и гладът са две от най-честите условия. Ако по време на гестационния период настъпи суша или глад, програмирането на развитието на специфични фенотипове на потомството може да бъде от полза при адаптирането на потомството към оцеляване в тази среда. Например, хранителни ограничения по време на живота на плода, които могат да доведат до вътрематочно забавяне на растежа (IUGR) и ниско тегло при раждане, са свързани с развитието на потомство с „пестелив фенотип“ (3, 4). Тези потомци са по-способни да придобиват и използват хранителни вещества, фенотип, който служи за предимство за оцеляване в продължителна среда на относителен глад.
Докато гестационното програмиране може да се е развило в полза на оцеляването на видовете, етиологията на избраните фенотипове на потомството се е променила драстично през последните епохи. Например, в съвременното общество потомството на IUGR обикновено е резултат от фактори, различни от хранителни ограничения, включително болестни състояния, които може да не са разрешавали плодовитостта на майката преди медицинско лечение от 20-ти век (напр. Автоимунно заболяване) или са уникални за настоящата епоха [напр. недостатъчност, свързана с предварително цезарово сечение (68); или многобройни бременности от по-висок ред, свързани с ин витро оплождане]. Тъй като етиологиите се променят и условията на околната среда на предците вече не съществуват, механизмите за програмиране могат да създадат потомство с неадаптивни фенотипове в съвременното общество. Например, потомството с ограничен растеж („пестелив фенотип“), изложено на западни диети с високо съдържание на мазнини, показва повишен риск от затлъстяване, хипертония и диабет като възрастни (3).
Понастоящем в САЩ и западните общества има големи здравни епидемии от затлъстяване, хипертония и диабет. В Съединените щати приблизително 65% от възрастните са с наднормено тегло и 31% са с наднормено тегло. Детското затлъстяване представлява голяма криза в общественото здраве, като 20% от децата са класифицирани като затлъстели. Във връзка със степента на затлъстяване честотата на хипертонията се увеличава. Сред възрастните в САЩ близо 30% от населението е с хипертония. По същия начин диабетът тип II се е увеличил драстично в западното общество. Световната здравна организация прогнозира нарастване на разпространението на диабет тип II от 1995 до 2025 г. от 170% (84–228 милиона) в индустриализиращия се свят.
Нараства интересът към свързването на развитието на „метаболитния синдром“ с ефектите от гестационното програмиране. Парадоксално повишеният риск от затлъстяване при възрастни, хипертония и диабет сред новородените с малка гестационна възраст е убедително демонстриран в епидемиологични проучвания при хора и проучвания върху животни при видове, включително плъхове, овце и други. Както беше обсъдено по-горе, екологичните стресове, които застрашават оцеляването на населението, включват глад, който създава хранителен стрес, и суша, която създава осмотичен стрес. По-специално, причиненото от суша лишаване от вода и придружаващата плазмена хипернатриемия са свързани с дехидратация-анорексия и по този начин съпътстващ потенциален хранителен стрес. В проучванията, проведени в нашата лаборатория, ние предположихме, че както хранителният, така и осмотичният стрес допринасят независимо за новородените с малка гестационна възраст и програмирането на фенотипите на потомството, които могат да демонстрират адаптивност към последващи условия на глад или суша. Въпреки това, когато са изложени на западни диети, тези фенотипове могат да допринесат за програмиране на затлъстяване и/или хипертония на потомството.
За да могат гестационните стресове да програмират реакциите на потомството, засегнатите физиологични системи трябва да бъдат изложени през периода на функционално развитие. Нашата лаборатория и други потвърдиха, че осморегулаторната и орексигенната системи стават функционални, макар и не напълно зрели, през последната половина на бременността и/или периода на новороденото.
Въпреки че феталната плазмена осмолалност се поддържа успоредно на майчините нива (чрез плацентарно уравновесяване), функционалните осморегулаторни механизми се развиват вътреутробно при овце и хора и може би по време на феталния и новородения период при алтрициални видове (напр. Плъхове) (76). Wirth и Epstein (76) предполагат, че реакциите на жажда се развиват през неонаталния период при сравнително високите видове плъхове. Наскоро обаче демонстрирахме централна осмотична реакция при краткосрочен фетален плъх (80). В по-прекоциалния плод на овцете системните и централните осмотично-дипсогенни механизми са функционални в близко бъдеще, тъй като гълтателната активност и секрецията на аргинин вазопресин (AVP) се предизвикват в отговор на предполагаемите дипсогени (61, 64). Развитието на осморегулацията също се показва от метаболитната активност в избрани новородени мозъчни региони, включително супраоптичните и паравентрикуларните (PVN) части на антеровентралната трета камера (33). Въпреки че феталните осмотично-дипсогенни отговори са непокътнати в близко бъдеще, нивото на осмотична чувствителност предполага функционална незрялост, тъй като плодът изисква значително по-голямо увеличение на плазмената осмолалност в сравнение с възрастния, за да стимулира поглъщането (13, 79).
Нашата лаборатория е извършила проучвания сред бременни животни, в които симулираме условия на суша чрез обезводняване на майката и условия на глад чрез относително ограничаване на хранителните вещества. Изследвахме отговорите на потомството както при плъхове, висок вид, така и при овце, предкоциални видове с модели на развитие, по-близки до човешките.
Симулирана суша: обезводняване на майката.
За да се изследва ефектът от ограничаването на водата при бременни плъхове, майките на майките бяха ограничени с вода, за да увеличат плазмения натрий с ~ 6 meq/l от 10 дни на бременността до термина (18). Ограничаването на водата се запазва през целия период на лактация до отбиването на новороденото на 21-дневна възраст. Новородените се отбиват от храна и вода ad libitum и се изучават както на 1 ден, така и на 12 седмици. Приемът на храна при майките беше значително намален (40%) както по време на бременност, така и при кърмене в отговор на ограничаването на водата при майките. По същия начин наддаването на телесно тегло при майката е намалено в по-голяма степен по време на бременност (64%), отколкото при лактация (24%), в съответствие с ефектите от дехидратационната анорексия. Както се очакваше, натриевият плазмен майчин се увеличи значително през двата периода на бременност и кърмене в сравнение с контролните язовири, така че относителното намаляване на плазмения натрий и осмолалитета, наблюдавано при бременност при плъхове, беше предотвратено при ограничените от вода язовири. Както се очаква, потомството на плъхове с ограничени от вода язовири тежи със 17% по-малко при раждането. В допълнение, 1-дневно потомство е имало повишена плазмена натриева осмолалност и хематокрит, отчасти резултат от раждането от вътреутробната хипернатриемия (18).
Като възрастни на 12 седмици, тези потомци продължават да показват значително намалено телесно тегло, като мъжете показват 11%, а жените 19% намаление от контролите. По-важното е, че въпреки 9 седмици храна и вода ad libitum, мъжкото потомство демонстрира устойчиви и значително повишени плазмени нива на натрий, осмолалитет и хематокрит. За разлика от тях, женското потомство има сходни плазмени нива на натрий и осмолалитет, въпреки че постоянно повишен хематокрит (15).
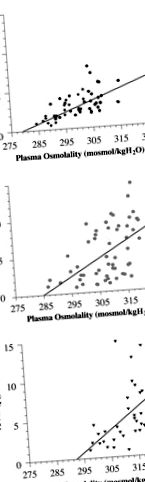
Фиг. 2.Линейна регресионна връзка между плазмената осмолалност (POsm) и плазмените нива на AVP (PAVP) в контролния единичен (A), контролни близнаци (Б.) и дехидратиран единичен (° С) новородени. Уравненията на линейната регресия бяха изчислени за всички набори от данни на 3-те групи и решени за праговата стойност, като се използва нулевото пресичане. Прагът за AVP секреция: дехидратиран единичен [PAVP = 0,27 (POsm - 290); r = 0,79; P
По този начин изглежда, че гестационната хипертоничност както при плъхове, така и при овце води до потомство с повишен натрий в плазмата и осмолалитет и хематокрит. Изследванията на потомци на плъхове допълнително показват постоянство на тези специфични за пола промени в зряла възраст, докато проучвания върху овце показват, че пренатално дехидратираните агнета едноплоди свидетелстват и за повишено артериално кръвно налягане. Освен това тези агнета показват променен праг на осмоларност за AVP секреция. Заедно, проучвания от двата вида показват, че хормоналните механизми за осморегулация могат да бъдат програмирани вътреутробно.
Симулиран глад: ограничаване на хранителните вещества при майките.
Вътреутробната среда отдавна е призната като допринасяща за поведението на потомството, въпреки че едва в края на 80-те години Barker et al. (4) разшири концепцията за вътреутробно програмиране до асоциация с ниско тегло при раждане с рискове от сърдечно-съдови заболявания при възрастни, захарен диабет и дислипидемия (57). Кръвното налягане при възрастни при хора е повишено сред фетусите със забавен растеж (46). Проучвания при плъхове, овце, прасенца и бабуини, при различни гестационни периоди, степени и видове дефицит на хранителни вещества (17, 40, 67, 73, 77), потвърдиха връзка, макар и понякога несъвместима, между IUGR и хипертония за възрастни или метаболитно заболяване. По подобен начин е доказано повишено кръвно налягане при възрастни потомци на плъхове след ограничаване на гестационния протеин (42, 51, 53, 67). Въпреки че рядко е измерван плазмен осмоларитет или натрий, няма промяна в натрия в майчината плазма на майки, лишени от хранене (45).
Изследванията на овце за недохранване показват различни фенотипове на потомството в зависимост от периода на бременност. В началото на бременността до средното хранене недохранването обикновено увеличава растежа на плацентата, докато недохранването в края на бременността намалява растежа на плода. В отговор на 15% намаляване на майчиното хранене между бременността дни 0 и 70, кръвното налягане е намалено при краткосрочни плодове, но се увеличава при новородено потомство (36, 39). По този начин механизмите на програмиране, които произвеждат постнатална хипертония, могат да доведат до по-ниско кръвно налягане във феталния живот чрез необясними досега механизми. За разлика от това, 15% ограничение на храната през последните 30 дни от бременността повишава средното фетално кръвно налягане (25). Противно на проучванията за недохранване в началото на бременността, 50% намаление на хранителните вещества при майките от 115 дни до срока повишава кръвното налягане на плода. Освен това, фетусите на 115 до 125 дни демонстрират повишен пресорен отговор на ANG II, въпреки че това не е демонстрирано навреме. В сравнение с проучванията при плъхове, има значително по-малко последващи проучвания върху потомство на недохранени овце.
маса 1. Базални стойности на урина при контролни единични, контролни близнаци и пренатално дехидратирани единични
Стойностите са средни стойности ± SE. GFR, скорост на гломерулна филтрация. Значителна разлика, контрол единичен срещу контролен близнак:
* P † P
Фиг. 3.Телесна маса и процент телесни мазнини при 3-седмично потомство (мъжки и женски комбинирани; Горна част) и при 9-месечни мъжки (плътни решетки) и женски (отворени решетки) потомство (отдолу) от контролни [пренатални/постнатални: ad libitum хранени (AdLib)/AdLib], незабавен ръст на догонване [ограничена храна (FR)/AdLib] и забавен растеж на догонващия растеж (FR/FR)). Стойностите са средни ± SE. *P
Фиг. 4.Плазмени нива на лептин при 3-седмично потомство (мъжки и женски комбинирани; A) и на 9 месеца (Б.) при мъжки (плътни решетки) и женски (отворени решетки) потомци от контрола (AdLib/AdLib), незабавен ръст на догонване (FR/AdLib) и забавен растеж на догонване (FR/FR). Стойностите са средни ± SE. *P
За да се предотврати бързият растеж на настигането сред малките плъхове с ниско тегло, новородените са кърмени от язовири, на които е осигурена 50% диета с ограничена храна през 21-те дни на кърмене. Тези потомци показват по-нататъшно забавяне на растежа по време на лактация, тежаща значително по-малко (55%) от контролите, с намален процент телесни мазнини, на 3 седмици на възраст (14). Въпреки това, на възраст от 9 месеца тези потомци са достигнали телесно тегло и телесни мазнини, еквивалентни на контролите (фиг. 3). Освен това плазмените нива на лептин са еквивалентни на контролите при 3 седмици и 9 месеца (фиг. 4).
Тези резултати потвърждават, че ограничаването на хранителните вещества по време на бременност може да доведе до намалено тегло при раждане. Бързият растеж на догонването, осигурен от нормалното хранене и лактация, води до нарастване на догонването извън контрола с 9 месеца при плъхове, като потомството демонстрира повишени телесни мазнини и повишен плазмен лептин. Повишеният плазмен лептин е очевиден преди увеличаване на процента телесни мазнини и по този начин предполага програмиране на развитие на лептинова резистентност. Забавеният растеж на догонване, предизвикан от ограничаване на храната по време на лактация, води до растеж на догонване до стойности, подобни на контролите, но с нормални телесни мазнини и плазмен лептин. Тези резултати предполагат, че програмирането на затлъстяването на потомството може да зависи от времето на намаляване на хранителните вещества и/или наличността на хранителни вещества. Може да се предположи, че предотвратяването на незабавен бърз растеж на новороденото може да намали риска от затлъстяване при възрастни при хората.
Сред допълнителните системи активирането на симпатиковата нервна система (SNS) може да бъде от решаващо значение за програмираната хипертония, свързана с хронична хипертоничност, по начин, подобен на хипертонията, свързана с повишен прием на натрий (8). В покой симпатиковите нерви проявяват тонизираща активност, което допринася за поддържане на артериалното кръвно налягане. Както хипертоничността, така и ANG II действат като симпато-възбуждащи фактори чрез осмо- или ANG II AT1 рецептори в OVLT и/или SFO. Невронните пътища от средното преоптично ядро и PVN до ростралния вентролатерален мозък и гръбначния междинно-страничен клетъчен стълб и накрая симпатиковите преганглионарни неврони (2, 52, 72) увеличават активността на SNS. Значителни доказателства сочат, че абсолютното ниво на симпатиковия тонус се променя при условия на повишен прием на сол или плазмена хипертоничност (8). При нормални индивиди повишеният прием на сол намалява плазмения ANG II, въпреки че артериалното кръвно налягане се поддържа чрез баланс на намалена медиирана от ANG II и повишена активност на SNS на осмо- или натриев рецептор. Въпреки това, при чувствителни към солта индивиди или животни доминират симпато-възбуждащи действия, предизвикани от хипертоничност, вероятно поради намаляване на нивата или действията на ANG II.
Фиг. 5.Ограничение на водата или хранителните вещества при майката по време на бременност и/или кърмене и неговите ефекти върху потомството. Фигурата обобщава нашите резултати от проучвания както при модели на овце, така и при плъхове. АН, кръвно налягане; Osm, осмоларност; Dif, разлика; Thresh, праг.
В обобщение изглежда, че гестационното програмиране е допринесло за адаптацията на видовете и оцеляването на популацията. Тези реакции на развитие и процеси все още функционират при хората и вероятно са допринесли за настоящата епидемия от хипертония, затлъстяване и диабет. Необходими са съгласувани научни усилия, за да се разберат механизмите и регулирането на гестационното програмиране. Съществува потенциал за промяна на бременността и/или средата на новороденото, така че да се оптимизират ползите и да се избегнат вредните ефекти от гестационното програмиране.
Тази работа беше подкрепена от безвъзмездни средства от March of Dimes (MG Ross), Американската асоциация за сърдечни заболявания (MG Ross) и Националните здравни институти [5-R01-DK-4331112 (MG Ross), 1-R03-HD-3967102 ( MG Ross), 5-R01-HL-4089912 (MG Ross), 1-R03-HD-044482 (MG Ross) и K01-DK-06399401 (M. Desai)].
- Гестационен диабет Американска асоциация по бременност
- Ранни ефекти на диетата с високо съдържание на мазнини върху нервно-съдовата функция и фокалната исхемична мозъчна травма американец
- Плач по време на бременност Причини; То; s Ефекти върху бебето
- Цефтриаксон - странични ефекти, употреби, дозировка, предозиране, бременност, алкохол RxWiki
- Ядене на лист от бетел (Paan) по време на предимства за бременност; Вредни ефекти