Магнезиевият фосфат е нова кисела киселина, която е бавнодействаща и се активира от топлина (40 ° C).
Свързани термини:
- Глюкоза
- Витамин D
- Ейкозаноиден рецептор
- Антиациди
- Паратиреоиден хормон
- Калциев фосфат
- Урея
- Креатинин
- Протеин
- Уреаза
Изтеглете като PDF
За тази страница
Нарушения, свързани с метаболизма на калция
Кристофър Саймъндс, д-р Джошуа Бусе, в ендокринните биомаркери, 2017 г.
Фосфат, магнезий и витамин D
Измерването на фосфат, магнезий и витамин D е полезно за диагностика на ендокринни нарушения, които влияят на калция. Въпреки това, обсъждането на тези аналитични измервания и преаналитичните, аналитичните и постаналитичните променливи ще бъде обхванато в лабораторни съображения и интерпретационни въпроси за оценка на анормално състояние на фосфат/магнезий/витамин D.
Специфичната за пациента история е от решаващо значение за оценка на влиянието на интер- и интраиндивидуалната променлива върху резултата от теста •
Дискусията с лабораторията относно оптималните техники за събиране, транспортиране и съхранение на проби ще поддържа оптимална цялост на пробата.
Използването на златните стандартни методи за анализ ще осигури превъзходен резултат; разбирането на неговите ограничения обаче ще осигури правилна клинична интерпретация.
Неадекватните лабораторни показатели и липсата на подходящ референтен диапазон за всеки аналит могат да доведат до неправилно тълкуване и решение от страна на клиницистите със сериозни последици за клиничната практика, здравеопазването и в крайна сметка за пациента.
Наследствени тръбни нарушения при боравене с минерали
Даниела Маген, Израел Зеликович, в Pediatric Bone (Второ издание), 2012
Тази глава обобщава нормалното бъбречно боравене с фосфати, калций и магнезий, както и бъбречно киселинно-алкално болни, прави преглед на молекулярната патофизиология и генетичните аспекти на наследствените тубуларни заболявания, засягащи боравенето с минерали, и описва клиничните и лабораторни характеристики на тези тубулопатии, включително свързаните с тях кости болест. Наследствените нарушения на тръбния транспорт включват група заболявания, които водят до дълбоки нарушения в хомеостазата на електролити, минерали или органични разтворени вещества в тялото и са свързани със значителна заболеваемост. Молекулярното изследване на наследствените тубулопатии е много важно за изясняване на генетичната основа на нарушенията, както и за предоставяне на нов и важен поглед върху функцията на специфични транспортни протеини и във физиологията на бъбречната тубуларна регенерация на разтворените вещества. Неорганичният фосфат (Pi) е един от най-разпространените аниони в човешкото тяло и играе решаваща роля в скелетната минерализация и клетъчния метаболизъм. Сред органните системи и тъкани, участващи в Pi хомеостазата, бозайникът на бозайниците служи като основен регулатор на Pi баланса и е способен да модулира своя реабсорбиращ капацитет Pi в съответствие с нуждите на организма.
Хранене при критично болни пациенти
Lee-lynn Chen MD, Annette Stralovich-Romani RD, CNSD, в Critical Care Secrets (Четвърто издание), 2007
21 Как трябва да се наблюдава критично болен пациент, който получава парентерално хранене?
Изходни стойности на електролити (напр. Натрий, калий, бикарбонат, магнезий, фосфат и калций), азот в уреята в кръвта, креатинин, глюкоза, албумин, триглицериди, пълна кръвна картина и тестове за чернодробна функция (например трансаминази, алкална фосфатаза и билирубин) трябва да се провери преди започване на терапията. След започване на терапията, проследяването на кръвната захар трябва да се извършва на всеки 4–6 часа, докато инфузията се стабилизира. Серумните триглицериди трябва да се проверяват 6 часа след завършване на инфузията на IV мазнина, за да се гарантира, че пациентът е в състояние да изчисти адекватно липидите. Трябва да бъдат серумни триглицериди
Физиология и патофизиология на диуретичното действие
Екскреция на електролит в урината и вода
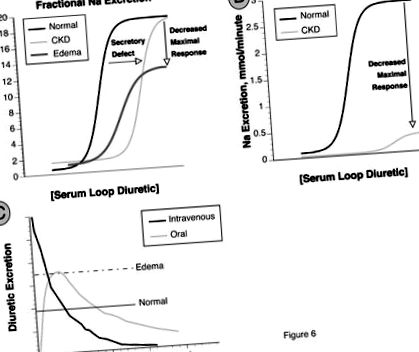
ФИГУРА 6. Крива на реакцията на дозата за бримкови диуретици. а: Фракционната екскреция на Na (FENa) като функция от контурната диуретична концентрация. В сравнение със здравите пациенти, пациентите с хронично бъбречно заболяване (ХБН) показват промяна в кривата надясно поради нарушена диуретична секреция. Максималният отговор се запазва, когато се изразява като FENa, но когато се изразява като абсолютна екскреция на Na (Б.), максималната натриуреза е намалена при пациенти с ХБН. Пациентите с оток демонстрират изместване надясно и надолу, дори когато са изразени като FENa (а). ° С: Сравнение на отговора на интравенозните и пероралните дози бримкови диуретици. При нормален индивид (Нормален) пероралната доза може да бъде толкова ефективна, колкото интравенозната доза, тъй като времето над натриуретичния праг (обозначено с "нормалната" линия) е приблизително равно. Ако натриуретичният праг се повиши (както е показано с пунктирана линия, от оточен пациент), пероралната доза може да не осигури достатъчно високо ниво на серума, за да предизвика натриуреза.
Наследствено недегенеративно невромускулно заболяване
Периодична парализа
По време на епизод на слабост трябва да се вземат серийни кръвни тестове за калий, калций, магнезий, фосфат и CK, за да се изключат другите споменати по-рано причини за слабост. Тъй като нивото на калий може да е нормално по време на хиперкалиемична периодична парализа и от време на време при хипокалиемична периодична парализа, нивото на калий трябва да се проверява последователно на всеки 15 до 30 минути, за да се определи посоката на промяна в момент, когато мускулната сила или се влошава или подобрява . ЕКГ може да покаже промени, съответстващи на хипо- или хиперкалиемия и може също да предупреди за сърдечни усложнения. EMG показва намален CMAP, пропорционален на степента на слабост. Изследванията на нервната проводимост са нормални. Неврофизиологията също така служи за изключване на други причини за парализа, като синдром на Guillain-Barré или миастения гравис (Видео 86, Тест с леден пакет в Myasthenia Gravis).
Пациентите, които се наблюдават между пристъпите, се нуждаят от изследване, за да се изключат причините за вторична хипокалиемия. ЕМГ може да бъде полезен при показване на доказателства за миотония, което би благоприятствало хиперкалиемичната периодична парализа. При тези пациенти, при които се е развила фиксирана слабост, ЕМГ може да бъде миопатична. Дори при тези с първоначално нормална ЕМГ може да има преувеличено увеличение, последвано от спад на CMAP с високочестотна 30-Hz стимулация или след повтаряща се мускулна контракция. 21 Мускулната биопсия често е необичайна между пристъпите на хипокалиемична периодична парализа, с патогномонични промени на големи централни вакуоли и от време на време некротични влакна. При хиперкалиемична периодична парализа могат да присъстват по-малки вакуоли и да се наблюдават тръбни агрегати. За потвърждаване на диагнозата може да се наложи провокативно тестване. Това трябва да се извършва с внимателен надзор, включително мониторинг на калия и ЕКГ. Хипокалиемично предизвикателство може да се извърши чрез даване на интравенозна глюкоза с или без инсулин. 22 Хиперкалиемично предизвикателство може да се извърши чрез даване на многократни дози перорален калий. 22 Когато е възможно, генетичното изследване може да бъде предпочитаното изследване, но ефективността му зависи от използваната скринингова стратегия.
Хиперекплексия на говедата
ДЖУЛИ А. ДЕНИС,. PETER J. HEALY, в Животински модели на нарушения на движението, 2005
V. БИОХИМИЯ
А. Клинична химия
Биохимичните находки са незабележими при телета, засегнати с ICM. Концентрациите на калций, магнезий, фосфат, глюкоза, урея, протеини и албумин в плазмата и CSF (само плазма) са подобни на концентрациите при клинично нормални телета. В допълнение, изследователите не наблюдават разлики между нормалните и засегнатите телета в плазмената активност на алкална фосфатаза, креатин киназа, аспартат аминотрансфераза, гама глутамил трансфераза или орнитин карбамоилтрансфераза. Креатин киназата и аспартат аминотрансферазата в CSF също не са забележителни (Dennis, 1987).
Б. Невротрансмитери
Очевидният неуспех на ICM-засегнатите телета до умерени двигателни отговори и някои клинични прилики с отравяне с тетанус и стрихнин, накараха изследователите да предположат, че заболяването може да бъде причинено от аномалия в механизма на инхибиторна обратна връзка в мозъчния ствол или гръбначния мозък, най-вероятно включващ отказ на инхибиране на долния двигателен неврон Тази хипотеза предизвика подробно разследване на концентрациите на аминокиселини, органични киселини и катехоламин в различни тъкани и телесни течности, с особен акцент върху инхибиторните невротрансмитери, глицин, таурин и гама-аминомаслена киселина (GABA) (Dennis, 1987).
Въпреки че глицинът има инхибиращ ефект върху гръбначния мозък, когато се прилага йонофоретично и е най-мощният от известните инхибиторни невротрансмитери (Curtis et al., 1968), изследователите не наблюдават разлики между нормалните и засегнатите телета в концентрациите на свободен глицин в плазмата, серума, CSF, гръбначен мозък и тринадесет физиоанатомично различни области в малкия мозък и мозъчната кора. Другите невротрансмитери на свободни аминокиселини, анализирани в плазмата и ликвора - GABA, таурин, аспартат, глутамат и норадреналин - също са сходни между двата фенотипа. Концентрациите на таурин са значително по-високи в някои региони на мозъка на телета, засегнати от ICM (продълговатия мозък, pons, бялото вещество на малкия мозък и substantia nigra), но значението, ако има такова, на това наблюдение остава неизвестно. Концентрациите на GABA не се различават значително между фенотиповете за нито един от анализираните тринадесет мозъчни сайта (Dennis, 1987).
В. Изследвания на рецептори за стрихнин
Говедата ICM споделя известно сходство с клиничните признаци на субконвулсивно отравяне със стрихнин. Стрихнинът блокира инхибиторния аминокиселинен предавател, глицин (Curtis и Johnston, 1974), като взаимодейства с постсинаптичния глицинов рецептор (Young and Snyder, 1973). Изследователите проведоха поредица от експерименти за изследване на усвояването и освобождаването на глицин в екстракти на гръбначния мозък от телета, засегнати от ICM, с помощта на радиоактивно маркиран стрихнин. Изследванията на функцията на рецепторното място в препарати за синаптозома показват, че само 5% свързване на стрихнин се наблюдава при телета, засегнати от ICM, в сравнение с контролите, което показва тежък дефицит на функционални места на глициновия рецептор. ГАМКA местата за свързване на рецепторите не се различават значително между ICM телета и контролите, потвърждавайки, че резултатите са селективни за глициновия рецептор. Изследователите също демонстрират 240% увеличение на скоростта на усвояване на глицин от синаптозомите на гръбначния мозък при засегнатите телета и те постулират, че това увеличение може да бъде компенсаторен механизъм за липсата на функционални постсинаптични рецептори (Gundlach et al., 1988).
Диария
Осмотичен
Осмотичната диария възниква, когато неабсорбираните, разтворими във вода разтвори остават в лумена на червата и така задържат вода. Полученото високо осмотично натоварване задължително изтегля разтворителя, вода, от тялото в лумена на червата в опит да се поддържа хомеостазата. Често срещан пример е „диетични бонбони“ или диария „дъвка“, при която захарен заместител, като сорбитол, не се абсорбира. Като осмотично активен, сорбитолът изтегля вода от тялото в лумена на червата, което води до диария.
Осмотичната диария обикновено се проявява в две ситуации:
Поглъщане на слабо абсорбиращи се материали: йони като магнезий, сулфати и фосфати, които обикновено се използват в лаксативи, или слабо абсорбирани захари и захарни алкохоли като сорбитол, лактулоза или манитол. Тези абсорбирани малки молекули остават в лумена на червата. Водата трябва да се задържа задължително, тъй като тялото не може да издигне осмотичен градиент през червата, което е условие за хомеостаза. Получената интралуминална осмоларност е около 290 mOsm kg -1, равна на тази на течностите в тялото като плазмата.
Осмотично натоварване: Такива разтворени вещества включват полиетилен гликол, магнезиеви соли (хидроксид и сулфат) и натриев фосфат, които се използват като лаксативи. Осмотичната диария се появява и при непоносимост към въглехидрати (напр. Непоносимост към лактоза, причинена от дефицит на лактаза). Поглъщането на големи количества хекситоли (напр. Сорбитол, манитол, ксилитол) или високофруктозни царевични сиропи, които се използват като заместители на захарта в бонбони, дъвки и плодови сокове, причинява осмотична диария, тъй като хекситолите се абсорбират слабо. Лактулозата, която се използва като слабително, причинява диария по подобен механизъм. Този дизахарид съдържа два монозахарида: фруктоза плюс галактоза. Несмилаема захар, лактулоза достига до дебелото черво, където пребиваващите бактерии разделят лактулозата до съставните й захари, които след това задържат вода.
Друга захар, фруктоза (плодова захар), е прост монозахарид, който не се нуждае от храносмилане, но може да се абсорбира слабо при някои хора, чиито тънки чревни епителни клетки притежават оскъдни рецептори за транспорт и абсорбция. Избягвайки в дебелото черво, фруктозата се ферментира, давайки късоверижни мастни киселини и газове. При тези със синдром на раздразнените черва диетата с високо съдържание на фруктоза може да допринесе за диарията и подуването на корема. Тъй като абсорбцията на фруктоза се възползва от наличието на глюкоза, храните с високо съдържание на фруктоза и с високо съдържание на глюкоза са по-малко склонни да причинят диария.
- Хиповитаминоза А - общ преглед на ScienceDirect теми
- Хипотрофия - общ преглед на ScienceDirect теми
- Goitrogens - общ преглед на ScienceDirect теми
- Липидният метаболизъм - общ преглед на ScienceDirect теми
- Течна диета - общ преглед на ScienceDirect теми