Свързани термини:
- Липиди
- Протеин
- Сърдечно-съдови заболявания
- Холестерол
- Дислипидемия
- Миоглобинурия
- Заболяване на коронарната артерия
- Липопротеинов холестерол с ниска плътност
- Атеросклероза
Изтеглете като PDF
За тази страница
Липопротеин и липиден метаболизъм
Резюме
Нарушенията на липопротеиновия и липидния метаболизъм - дислипидемии - могат да бъдат класифицирани въз основа на първичното биохимично нарушение, като високи или ниски плазмени нива на липопротеинов холестерол с ниска плътност, липопротеинов холестерол с висока плътност, триглицериди или някаква комбинация от тях. Няколко моногенни дислипидемии, като хетерозиготна фамилна хиперхолестеролемия, сега са дефинирани на молекулярно генетично ниво. За да се предотвратят сериозни усложнения, особено преждевременни сърдечно-съдови заболявания, при моногенни дислипидемии е важно да се изследват субекти в риск. Диагнозата може да изисква клинична, биохимична и геномна ДНК оценка. Лечението включва диета, упражнения и лекарства за понижаване на липидите.
Диабетна дислипидемия
Резюме
Затлъстяването, метаболитният синдром и диабетът често се свързват с нарушения на метаболизма на липидите и липопротеините. Тези нарушения обикновено се наричат метаболитна или диабетна дислипидемия, състояща се предимно от хипертриглицеридемия, увеличени малки плътни частици липопротеини с ниска плътност и нива на холестерол на липопротеини с ниска плътност. Основните механизми, залегнали в основата на диабетната дислипидемия, изглежда са свръхпроизводството на липопротеини с много ниска плътност в гладно и производството на чревен хиломикрон в постпрандиалното състояние, което води както до гладно, така и до постпрандиална дислипидемия. Настоящата глава разглежда основните характеристики на диабетната дислипидемия и патофизиологичните механизми, участващи в развитието на тази все по-често срещана форма на дислипидемия при метаболитно заболяване.
Метаболомика при дислипидемия
Хуа Чен,. Rui-Chao Lin, в Advances in Clinical Chemistry, 2014
5 Хиперлипидемия
Хиперлипидемията, като основен рисков фактор за коронарна болест на сърцето, е един от най-важните проблеми на общественото здраве [26]. Това нарушение на липидния метаболизъм се характеризира с необичайно повишен триглицерид (TG), общ холестерол (TC), липопротеинов холестерол с ниска плътност (LDL-C) и холестерол с много ниска плътност (VLDL-C) и намален холестерол на липопротеините с висока плътност (HDL-C) [27]. Голямото свръхпроизводство на VLDL-C е основен дефект в този процес, предизвиквайки множество липопротеинови промени, които водят до увеличени остатъчни частици, по-малки LDL-C и намален HDL-C [28]. LDL-C е основната цел за понижаваща липидите терапия и профилактика на сърдечно-съдови заболявания. Интересното е, че хиперлипидемията може да участва и в други патологични състояния, включително увреждане на паметта и потенциално може да влоши острия хеморагичен некротичен панкреатит [29, 30] .
Циркулиращи TC, TG, HDL-C, LDL-C и липопротеин (а) са добре установени биомаркери за хиперлипидемия [31]. Metabolomics предоставя алтернативен подход за разширяване на този традиционен репертоар и потенциално идентифицира нови показатели преди началото на клиничното заболяване.
Хиперлипидемията се класифицира в пет типа (I, II, III, IV и V) [32]. Друг тип хиперлипидемия, т.е. фамилна дислипидемия, е наследствена. Това разстройство се състои от фамилна комбинирана хиперлипидемия, фамилна хиперхолестеролемия, фамилна дисбеталипопротеинемия, фамилен дефицит на липопротеинова липаза и други генетични нарушения на метаболизма на липопротеините въз основа на различни модели на наследяване [33]. За опростяване хиперлипидемията може да бъде класифицирана като хиперхолестеролемия, комбинирана хиперлипидемия, хипертриглицеридемия и HDL хиперлипидемия въз основа на вида и концентрацията на липидите в кръвта.
Първични смесени дислипидемии
Определение
FDBL е известен също като широко бета заболяване, xanthoma tuberosum, заболяване за отстраняване на остатъци или хиперлипопротеинемия тип III в класическата класификация на Fredickson (Fredrickson et al., 1967). Това е рядко автозомно-рецесивно наследствено нарушение на липидния метаболизъм, характеризиращо се с повишени плазмени концентрации на холестерол и триглицериди, причинени от натрупването на остатъчни липопротеинови частици (остатъци от хиломикрон и остатъци от VLDL или липопротеини с междинна плътност (IDL), наричани още β-VLDL). Болестта става напълно изразена в зряла възраст и е по-често при мъжете. FDBL е свързан с повишен риск от преждевременна коронарна, периферна съдова (интермитентна клаудикация) и мозъчно-съдова болест (Carmena et al., 2000; Durrington, 2007b; Stalenhoef, 2011).
Класификация на хиперлипидемии и дислипидемии
Jesús E. Millán Núñez-Cortes, Joaquín J. Millán Pérez, в Encyclopedia of Endocrine Diseases (Second Edition), 2019
Нефротичен синдром
Въпреки че има глобална дислипидемия, най-характерната промяна е повишаването на общия холестерол и LDL-C. Това е представено главно за увеличения чернодробен синтез и намаленото сливане на плазмен клирънс (Vaziri, 2003). Някои от участващите механизми в разстройството на липидния метаболизъм при нефротичен синдром са:
Придобит дефицит на LDL рецептор с последващо увеличаване на вътреклетъчния синтез на холестерола поради увеличаване на ензимната активност на HMGCoAR.
Увеличение на ензима PCSK9 с последващ катаболизъм на LDL рецептор, което води до увеличаване.
Повишената чернодробна активност на ацил-КоА-холестерол ацил-трансфераза (ACAT-2) катализира образуването на естери на холестерола от свободен холестерол, като по този начин увеличава LDL липопротеините, богати на холестерол.
Загуба на урина в придружаващата протеинурия лецитин-холестерол ацил-трансфераза (LCAT).
Намаляване на активността на липопротеин липазата (LPL).
Намаляване на ензима 7-алфа-хидроксилаза и производството на жлъчни киселини, натрупвайки вторични отлагания на холестерол.
Увеличение на синтеза на Lp (a).
Следователно плазматичният профил на дислипидемия при нефротичен синдром е много разнообразен (de Sain-van der Velden et al., 1998):
Хиперхолестеролемия с повишен LDL-C.
Хипертриглицеридемия с повишена VLDL.
Увеличение на остатъчните липопротеини с повишена IDL.
Повишаване на липопротеина (а).
Често спадане на HDL-C с намаляване на обратния поток на холестерола.
Сърдечно-съдова токсикология
6.16.11 Проблеми и подводни камъни с работната хипотеза
Една проблемна част от „ДНК pol-γ хипотезата“ (Lewis and Dalakas 1995) се основава на полезността на изобилието на mtDNA в сурогатни тъкани за удостоверяване на митохондриалната токсичност в прицелните тъкани (Cote et al. 2002). Съществуват данни относно токсикогеномиката и антиретровирусната терапия и са изложени някои теории - особено по отношение на липодистрофия и нарушения на липидния метаболизъм (Arnedo et al. 2007; Tarr и Telenti 2007) и нарушения на репликацията на mtDNA; прегледано в (Tarr and Telenti 2007). Като цяло има някои доказателства за делеции на mtDNA в различни тъкани на пациенти, получаващи NRTIs (White 2001), например скелетни мускули (Vittecoq et al. 2002), но липсващи в други тъкани, докато някои проучвания, използващи периферна кръв като сурогатен маркер не открива никакви разлики, свързани с мутация на mtDNA (Walker et al. 2002). Като цяло хипотезата за изчерпване на mtDNA, свързана с инхибирането на ДНК pol-γ, е разумна; все пак са необходими допълнителни доказателства, за да се определят клиничните събития.
Основни атрибути на приемлив in vitro диагностичен тест
5.1.1.3 Връзка между двете регулаторни класификации
Преглеждайки базата данни на FDA за медицински изделия, изглежда, че FDA класификацията на изделията и определянето на нива на сложност не са свързани, освен, може би, за IVD на клас III, които се считат за тестове с висока сложност. Например, системите за тестване на LDL-C за същата индикация, както са изброени в заповедта или етикета за одобрение (измерване, което подпомага диагностиката и лечението на нарушения на метаболизма на липидите и липопротеините), бяха одобрени от FDA за трима доставчици на IVD под клас I, но междувременно, класифицирани като отказани [15], умерени [16] или с висока сложност [17]. Струва си да се спомене, че първите две устройства използваха един и същ предикат, Roche DL Cholesterol Plus, за 510K значителни заявления за еквивалентност. Друг пример, тестът за протромбиново време е определен като клас II, но също така устройствата са определени като отказани [18], умерени [19] или с висока сложност [20]. Последните два теста бяха одобрени за една и съща компания, Siemens, използвайки един и същ реагент, при едно и също подаване на 510K, но умерената сложност беше автоматичен анализ, а високата сложност беше ръчен анализ.
Мускулни заболявания
Миоглобинурия
Лечението е насочено към обръщане на мускулното разрушаване (в много случаи почивка) и поддържане на адекватно отделяне на урина. Ранната енергична реанимация с течности намалява честотата на бъбречна недостатъчност по време на миоглобинурия. Манитолът трябва да се прилага за насърчаване на осмотична диуреза и за отстраняване на свободните кислородни радикали, произведени след реперфузия на исхемичния бъбрек. Алкализирането на урината с натриев бикарбонат може да предотврати утаяването на хематин на миоглобинова киселина в бъбречните тубули и също така да намали риска от бъбречна недостатъчност.
Геномика за прогнозиране на риск от коронарна артериална болест
Торстен Кеслер,. Heribert Schunkert, в Геномна и прецизна медицина (трето издание), 2018
Въведение
Исхемичната болест на сърцето е водещата причина за смърт в западните страни. Като се има предвид, че остър миокарден инфаркт и застойна сърдечна недостатъчност са почти отзад, значението на коронарната атеросклероза става още по-очевидно.
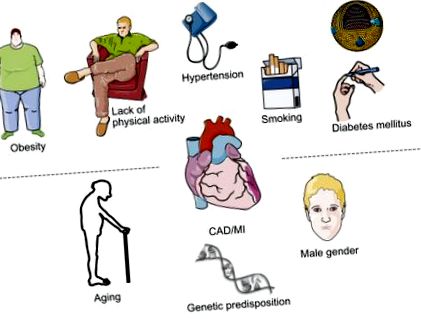
Модифицируемите рискови фактори на атеросклероза могат да бъдат разграничени от немодифицируемите рискови фактори, докато рисковите фактори като тютюнопушене, артериална хипертония и диабет могат да бъдат благоприятно повлияни от модификация на начина на живот или фармакологични интервенции [1], възрастта и полът не могат да бъдат модифицирани (фиг. 8.1). Нарушенията на липидния метаболизъм представляват някакви идиосинкразии, тъй като те са модифицируеми от една страна чрез фармакологични терапии, но от друга страна, често причинени от принципно немодифицируема генетична основа, например фамилна хиперхолестеролемия.
Фигура 8.1. Модифицируеми и немодифицируеми рискови фактори, увеличаващи риска от коронарна артериална болест.
Положителната фамилна анамнеза, която също е израз на генетичното бреме, което носи човек, е друг немодифицируем рисков фактор. Хората с близък роднина, страдащи от миокарден инфаркт в млада възраст, имат повишен риск от коронарна артериална болест (ИБС), който зависи от степента на родство (фиг. 8.2). През последните години резултатите от проучвания за асоцииране в целия геном (GWAS) показват, че тази генетична основа далеч надхвърля само положителната фамилна анамнеза и не може да бъде сведена до само един засегнат ген. Всъщност всеки индивид, независимо от положителната фамилна анамнеза, носи голям брой алели на генетичен риск. Сумата (или интерактивните ефекти) от тези рискови алели по-скоро представлява генетичния риск на човек.
Фигура 8.2. Влияние на различни степени на родство по отношение на фамилната анамнеза за коронарна артериална болест върху индивидуалния риск.
Модифициран след Mayer B, Erdmann J, Schunkert H. Генетика и наследственост на коронарна артериална болест и миокарден инфаркт. Clin Res Cardiol. 2007; 96 (1): 1–7 [2] .
Търсенето на генетични варианти, причиняващи CAD, започва с ограничен брой кандидат-гени и след това преминава към търсене в целия геном, тъй като технологията се подобрява. Първоначално гените, кодиращи протеини, за които е известно, че модулират традиционните рискови фактори, са основните цели на търсенето на генетични рискови фактори, което се дължи на ограничените технически възможности. Причинното участие в болестния процес наистина може да бъде показано за гените, кодиращи съответно холестеролния рецептор с ниска плътност (LDL) и липопротеин (a), LDLR и LPA. В много случаи обаче не е открита връзка между генетичните полиморфизми и проявата на CAD. Подход без хипотези, който разглежда варианти в целия геном, се оказа по-ефективен. С дешифрирането на човешкия геном и анотирането на еднонуклеотидни полиморфизми (SNP), търсенето на варианти, свързани с риска от коронарна болест в целия геном, стана възможно от GWAS.
Хранене и храна при пациенти със СПИН
Беата Калунюк,. Małgorzata Muc-Wierzgoń, в „Здраве на хората, заразени с ХИВ“, 2015 г.
9.2 Хранене и АРТ
През последното десетилетие се наблюдава значителен напредък в разработването на лекарства за АРТ, използвани в комбинация за намаляване на репликацията на ХИВ вируса и за лечение на заразени с ХИВ лица. Поради тези лекарства, много хора, заразени с ХИВ, могат да намалят нивата на вируса в кръвта до неоткриваеми нива. Антиретровирусното лечение е важно в живота на пациентите със СПИН, тъй като трябва да продължи до края на живота им, дори няколко десетилетия.
Комбинираната антиретровирусна терапия (cART), която в момента се препоръчва, се основава на шест групи антиретровирусни лекарства. Има риск от различни неблагоприятни ефекти. Следните ефекти се наблюдават при заразени пациенти: промени в метаболизма като повишени нива на триглицериди, общ холестерол и LDL; Спад на концентрацията на HDL; инсулинова резистентност на тъканите и нарушения на глюкозния толеранс; повишено ниво на лактат; остеопения и остеопороза; сърдечно-съдови заболявания; хематологични аномалии; стомашни симптоми; нефропатии; и кожни лезии. Нарушения на липодистрофията или липидния метаболизъм се наблюдават в рамките на 3–12 месеца от терапията при приблизително 40% от пациентите. Нарушенията на метаболизма на въглехидратите засягат приблизително 60% от пациентите [80]. Нефропатиите са свързани както с HIV инфекция, така и с нефротоксичните ефекти на антиретровирусните лекарства [81]. Развитието на такива нарушения може да се забави чрез подходяща диета.
Поради лекарствени взаимодействия, употребата на хиполипидемични средства - статини - е ограничена поради повишената вероятност от миопатия. В този контекст диетата с контролиран прием на мазнини става важна за поддържащото управление [80,82] .
Неблагоприятните взаимодействия на протеазни инхибитори с протонната помпа и Н2 рецепторните инхибитори (намалена абсорбция на, например, атазанавир) ограничават тяхната употреба при лечение на стомашни разстройства [81,82]. Диетата, която намалява киселинността на стомашния сок, е клинично значима. Освен това се препоръчва да се елиминира алкохолът по време на АРТ. Редовната консумация на дори леки количества алкохол води до пристрастяване и реагира с лекарства [80]. Освен това цитрусовите плодове, особено грейпфрутите и всички продукти, съдържащи грейпфрут, са противопоказани, тъй като нарушават механизма на действие на антиретровирусните лекарства, като блокират ензима цитохром P450 3A4.
Преди започване на терапията интервюираме всеки пациент, извършваме пълен физически преглед, провеждаме задълбочена хранителна оценка, оценяваме чревната функция и изчисляваме дневните калорични и протеинови нужди. Изборът на подходящи орални, ентерални и парентерални диети е от решаващо значение за успешното лечение на тези пациенти. Тъй като всички пациенти със СПИН, използващи ART, се различават по своите хранителни нужди, толерантност към диетата и степен на чревна дисфункция, няма единна схема на хранителна терапия, която може да се използва при лечението на всички тези пациенти. Поради това препоръчваме специални индивидуални диети за устно комбиниране с хранителни добавки и ентерални и парентерални диети при лечението на пациенти със СПИН, използващи ART [78] .
Във всеки случай хората трябва да следват диетичните препоръки, свързани с терапията, и да консумират рационална, здравословна диета без излишни калории, захари и животински мазнини и богата на зеленчуци и протеини. Диетата трябва да се консумира под формата на четири до шест хранения на ден.
- Дъвка - общ преглед на ScienceDirect теми
- Функционална напитка - общ преглед на ScienceDirect теми
- Кожен васкулит - общ преглед на ScienceDirect теми
- Диетичен прием - преглед на ScienceDirect теми
- Функционално стомашно-чревно разстройство - общ преглед на ScienceDirect теми