Изветряне на бурята - Буря - Пароксизмална симпатикова хиперактивност
От: Хайди Рейст, Доктор, CBIST
Центрове за рехабилитация на дъга
Штурм, какво има в името?
Обикновено наричан „щурм“, пароксизмалната симпатикова хиперактивност (PSH) е разстройство на нервната система, което засяга 15 до 33 процента от хората, претърпели тежка черепно-мозъчна травма (TBI). Появата на симптомите може да настъпи в рамките на часове или месеци след нараняването, а за членове на семейството с малко медицинско минало признаците могат да бъдат тревожни: учестено дишане, изпотяване, възбуда и необичайна поза (Lemke, 2007).
Какво е PSH, какво го причинява и как може да се лекува? Преди да започнем, нека се обърнем накратко към името, пароксизмална симпатикова хиперактивност. През годините той е известен с различни имена, много от които са еволюирали чрез опити за описване на неговата симптомология или етиология. Например, Baguley (1999) отбелязва, че отделните случаи на разстройството са имали различни имена като „пароксизмални симпатикови бури“, „синдром на вегетативната дисфункция“, „треска от централен произход“ и „остро разстройство на средния мозък“. Тук се използва терминът PSH, защото той най-добре описва настоящите познания. Бърз преглед на самото име ще илюстрира няколко основни концепции за PSH.
Първо, а пароксизъм е внезапно повторение или пристъп на заболяване или внезапно влошаване на състоянието. Второ, симпатичен се отнася до частта „борба или бягство“ на нашата автономна нервна система. И накрая, хиперактивност описва състоянието на симпатиковата система, когато настъпи „щурм“.
Определение и диагностика
Сега, когато разбираме разнообразните конвенции за именуване, би трябвало да е по-лесно да се определи какво е PSH, но и това не е толкова лесно. Всъщност PSH е конгломерат от симптоми, с диагноза по изключение. Нека започнем със симптоми:
Хипертония—Повишено кръвно налягане
Тахикардия- абнормно бърз сърдечен ритъм
Тахипнея- анормално учестено дишане Дистония - състояние на анормален мускулен тонус
Хипертермия- анормално висока телесна температура, от централен произход
Позиране- анормална мускулна скованост/позициониране на тялото
Диафореза- анормална/прекомерна степен на изпотяване
Различни медицински специалисти са приложили изисквания за диференциална симптоматика за окончателна диагноза PSH. Например, една дефиниция изисква поне един пароксизъм (внезапна поява на симптоми), който включва тахикардия, хипертония, хипертермия, тахипнея, дистония, поза или диафореза, да се проявява със скорост най-малко един цикъл на ден (отбелязано в Liu, Jolly, Pokala, 2010). Друго определение (Baguley, Nicholls, Felmingham, Crooks, Gurka и Wade; 1999) го дефинира като „едновременно, пароксизмално увеличаване на поне пет от седем докладвани функции“ ... „с епизоди, продължаващи поне две седмици след нараняване“. Perkes, Baguley, Nott и Menon (2010) отбелязват, че от 1993 г. насам са публикувани девет набора диагностични критерии за PSH, като в областта не е постигнато нито едно съгласувано определение.
Тъй като в PSH няма един тест, който да се прави при много други заболявания или състояния (напр. Кръвен тест за разстройство на щитовидната жлеза), клиницистите трябва да изключат метаболитни или инфекциозни причини за симптомите. След като могат да бъдат изключени други причини за симптомите, определение като горното може да се използва за положителна диагностика на PSH. Въпреки че няма напълно съгласувана диагноза
се използва постоянно, ключовата характеристика при диагностицирането на PSH е, че трябва да има ясно клинично представяне на симптомите, заедно с последователност на тяхното внезапно начало с течение на времето.
Ретроспективно проучване на Baguley, Nicholls, Felmingham, Crooks and Wade (1999) установи значителни статистически разлики между клиничните симптоми между индивидите, диагностицирани с PSH, в сравнение с контролните групи, които PSH изключват. За седем от осемте клинични характеристики данните показват, че пациентите с PSH са имали значително по-високи честоти на изпотяване, тонус, поза, хипертония, дифузно аксонално увреждане, нараняване на мозъчния ствол и хипоксия преди приемане (вж. Таблица 1). Това подкрепя диагностичните критерии, посочени по-горе за PSH. Докато първите клинични характеристики представляват симптомология (изпотяване, тонус и т.н.), последните две в таблица 1 представляват потенциална етиология на PSH. С други думи, възниква въпросът „кой получава PSH?“ 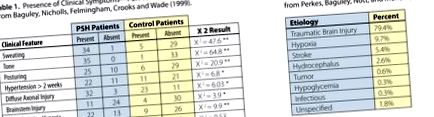
Причините за PSH
PSH рядко се съобщава без идентифицирана етиология (причина) и е свързан предимно с TBI. Perkes, Baguley, Nott и Menon (2010) установяват, че от 349 случая, идентифицирани в медицинската литература, 277 (79%) са предшествани от появата на TBI. Останалите 21 процента са подкатегории на придобити мозъчни наранявания (ABI), както е показано в таблица 2. Kishner, Augustin и Strum (2013) отбелязват, че дифузните аксонални наранявания и мозъчните стволови увреждания са идентифицирани като причини за PSH при по-високи нива. Рабинщайн (2007) установява, че 33% от пациентите с TBI отговарят на диагностичните изисквания на PSH, спрямо само 6% от пациентите с други остри неврологични диагнози.
Някои автори отбелязват, че PSH е значително по-вероятно да се появи при пациенти с тежка TBI с оценки на Glascow Coma от 3 до 8 (Lemke; 2004) или нива на Ranchos I до IV (Kishner; 2013). Това дава по-ясна картина на заболеваемостта на пациентите - това са индивиди, които обикновено са на ниско ниво неврологично и може да са във вегетативно или минимално съзнателно състояние. Колективно обаче информацията досега не идентифицира ясно етиологичните фактори точно на това, което причинява PSH, а само идентифицира, че неврологичната травма е предшественик. За да идентифицират правилното лечение на PSH, лекарите и клиницистите трябва да разберат патофизиологията, причиняваща безбройните симптоми на хората с опит с PSH.
Предполага се, че има много различни основни причини, включително мозъчни места с дисфункция, вариращи от мозъчния ствол до диенцефалона до орбиталната фронтална кора. Предполага се, че има и други основни причини, включително епилепсия и гърчове, въпреки че ЕЕГ тестовете изключват гърчовете като източник (Do, Sheen and Bromfield, 2000). Каква е тогава преобладаващата мъдрост по отношение на патофизиологията на PSH? За да отговорим на този въпрос, трябва отново да се обърнем към заглавието, като се съсредоточим върху аспекта на Симпатиковата хиперактивност, защото той ни казва, че „щурмът“ вероятно е резултат от свръхактивна симпатикова нервна система.
Автономна нервна система
За да говорим със симпатиковата нервна система, първо трябва да се обърнем към автономната нервна система, в която симпатиковата система е разположена. Автономната нервна система (ANS) е система за контрол, която работи до голяма степен извън нашия съзнателен контрол. Той контролира (чрез инервация) такива области като сърдечни и гладки мускули, ендокринни и екзокринни (хормонални) функции и както McCorry (2007) посочва, че „влияе върху дейността на повечето тъкани и системи от органи в тялото“. Съществуват различни мозъчни области, които допринасят за функциите на АНС, включително мозъчния ствол, диенцефалона (особено хипоталамуса) и дори области от мозъчната кора и лимбичната система (по-специално амигдалата).
Жизнените функции се контролират от ANS, включително сърдечната честота, кръвното налягане, стомашно-чревната перисталтика, температурата, глада, жаждата, плазмения обем и плазмената осмоларност (McCorry, 2007).
Има две анатомично и функционално различни подсистеми на ANS, които работят паралелно, но в допълнение и играят жизненоважна роля в поддържането на хомеостазата. Единият е парасимпатикова система който е отговорен за вегетативните функции, възникващи, когато тялото е в покой (напр. стимулиране на слюноотделянето и храносмилането, свиване на пикочния мехур, инхибиране на сърцето и обикновено се нарича „почивка и храносмилане“ функции. Другото е симпатикова система който контролира дейности, които са от съществено значение за подготовката ни за физическа активност, позволявайки на тялото да функционира при стрес (напр. разширяване на зеницата, ускорено сърце, инхибирано храносмилане), и обикновено се нарича реакция „борба или бягство“. По отношение на PSH, въпреки че точният механизъм все още е неизвестен, се предполага, че той е пряк резултат от загуба на баланс между парасимпатиковата и симпатиковата нервна система на нашата ANS.
Ключов аспект на двете системи е, че те осигуряват с думите на McCorry’s (2007), „някаква степен на нервно постъпване на тъкан по всяко време“. Това означава, че във всеки момент парасимпатиковата система или симпатиковата система могат да повлияят на тъканите, като инхибират или подобряват чрез невронално изстрелване. Обикновено двете подсистеми имат диаметрално противоположни ефекти върху тъканта, при което едната система би инхибирала (напр. Симпатиковата система инхибира свиването на пикочния мехур), а другата би усилила (напр. Парасимпатиковата система свива пикочния мехур). Вижте фигури 1 и 2.
По отношение на PSH се смята, че дисбалансът между парасимпатиковата и симпатиковата система води до неефективност на парасимпатиковата система при уравновесяване на симпатиковата система. Това прави индивида в неконтролиран симпатиков отговор (готов за физическа активност), където зениците се разширяват, слюноотделянето се задържа и сърцето се ускорява, за да назовем само няколко. Baguley, Nicholls, Felmingham, Crooks, Gurka и Wade (1999) излагат хипотезата за тристепенен процес след нараняване, за да обяснят щурма:
Етап 1
Пациентите получават паралитици или са успокоявани за предотвратяване на отоци и няма идентифицируема разлика между тези, които ще получат PSH и тези, които не.
Етап 2
Настъпва PSH и прекратяването се сигнализира от спирането на диафорезата. Средното прекратяване е 74 дни след нараняване.
Етап 3
Пароксизмите са спрели, но пациентът вероятно има остатъчна дистония и спастичност, като количествата варират в зависимост от пациента. Малко известно е какво причинява симпатиковата система да стане хиперактивна, но са предложени редица теории. Perkes, Baguley, Nott и Menon (2010) отбелязват по-специално три. Първият е свързан с предположенията, че възбудителните центрове на мозъчния ствол вече нямат кортикален контрол над тях, което води до хиперсимпатиково състояние. Вторият се отнася до модел, наречен Excitatory/Inhibory Ratio модел, където хиперактивността произхожда от нивото на гръбначния мозък. Третата теория се отнася до връзката между аферентните стимули (информация от тялото към мозъка) и симпатиковата хиперактивност. Някои доказателства показват, че теорията за аферентните стимули има най-голямо сцепление. Baguley, Hersineau, Gurka, Nordenbo and Cameron (2007) и Lemke (2007) отбелязват, че „вредните“, но „тривиални“ стимули, като засмукване, аларми на оборудването, преместване и т.н., могат да доведат до пароксизми. Perkes, Baguley, Nott и Menon (2010) призоваха за по-нататъшно проучване на патофизиологията на PSH и отбелязаха, че „свръхреактивността към аферентни стимули може да бъде отличителен белег на PSH“.
Значение на лечението
Независимо дали механизмите са известни или неизвестни днес, има достатъчно причини да се съсредоточи върху лечението на PSH. Основната причина е, че без лечение има потенциал за повишена заболеваемост в резултат на PSH. Хипертермията, която може да доведе до вторично мозъчно увреждане, е едно от тези притеснения. В Baguley, Nicholls, Felmingham, Crooks, Gurka and Wade (1999) 73% от пациентите с PSH са имали ядра с температури над 38 ° C (100,4 ° F) до две седмици след нараняване, като 24% продължават в продължение на четири седмици след травма. Друго притеснение е забавянето или отслабването на позата. Това значително увеличава енергийните разходи на пациентите (вариращи от 100 до 250 процента), което води до загуба на тегло и трайно увреждане на сърдечните и скелетните мускули.
Lemke (2007) отбелязва различни вторични проблеми, които могат да доведат до повишена заболеваемост. Може да се увеличи вторично мозъчно увреждане поради намаляване на оксигенацията на мозъчната тъкан. Хипертонията може също да повлияе на вторично нараняване поради риск от кървене, както и сърдечни аритмии в резултат на буря, която може да доведе до дългосрочна сърдечна дисфункция. Повишената метаболитна активност може да доведе до повишени нива на кръвната захар и основните температури, което може да доведе до загуба на мускули и загуба на тегло и бъбречна дисфункция. Лемке също така отбеляза, че „крайната цел е бърз контрол на признаците и симптомите на излишната активност на симпатиковата нервна система, за да се предотвратят вторични усложнения при продължителен стрес и да се улесни рехабилитацията“. Какви са тогава възможностите за лечение на PSH?
Лечение
Лечението и управлението на PSH до момента е фармакологично основано, като най-често срещаните лекарства са тези, които потискат централната нервна система и следователно потискат симпатиковата нервна система (Lemke, 2007). Общите лекарства включват морфин, фентанил и мидазолам. Интратекалният баклофен е успешен, като същевременно ограничава седативните ефекти на някои други лекарства (докладвано в Lemke, 2007). В голяма степен протоколите за лечение се различават в зависимост от практикуващия и могат да бъдат описани като „проби и грешки“ въз основа на отговора на пациента към лекарствените протоколи. В допълнение, други лекарства се използват за насочване на специфични симптоми и Lemke (2007) има отличен преглед на употребата на лекарства и техните действия за лечение на PSH. Лечението и по-доброто разбиране на патофизиологията са две области, които се нуждаят от допълнителни изследвания. По-доброто разбиране на механизмите на PSH ще помогне да се насочи по-доброто лечение, ако не и превенцията. По-прецизните протоколи за лечение също ще спомогнат за предотвратяване на дългосрочните съпътстващи заболявания.
Образование
Както гласи поговорката, мозъчна травма често се случва на цялото семейство, а не само на индивида с нараняването, поради често трайните и за цял живот промени, които се случват както на индивида, така и на неговото семейство и социална мрежа. За тази цел образованието на семейството по отношение на PSH е изключително важно. Първо и най-важно, те може да са първите, които ще видят признаците и симптомите, когато се появят, и могат да бъдат решаваща част за поддържането на комфорта на любимия човек. Както отбелязва Лемке (2007), това може да бъде от полза и за семейството, тъй като активното участие може да намали чувството на безпомощност при справяне с нараняванията на близките си.
Препратки
Baguley, IJ. Номенклатура на „пароксизмални симпатикови бури“ (1999). Изследвания на клиника Майо; 74-105.
Baguley, IJ, Heriseanu, RE, Gurka, JA, Nordenbo, A и Cameron, ID (2007). Габапентин при лечението на дизавтономия след тежка черепно-мозъчна травма: серия от случаи. Вестник по неврология неврохирургия и психиатрия; 78; 539-541.
Baguley, IJ, Nicholls, JL, Felmingham, KL, Crooks, J, Gurka, JA и Wade, LD (1999). Дизавтономия след мозъчна травма: забравен синдром? Вестник по неврология неврохирургия и психиатрия; 67; 39-43.
Do, D, Sheen, VL, Bromfield, E (2000). Вестник по неврология неврохирургия и психиатрия; 69; 832-838.
Kishner, S и Lorenzo, CT. Автономни усложнения след нараняване на главата. От www: //emedicine.medscape. com/article/325994-преглед. Отпечатано 13.06.2103.
Лемке (2004). Избягване на бурята: симпатична буря след черепно-мозъчна травма. Вестник за сестрински грижи; 36 (1).
Лемке (2007). Симпатикова буря след тежка черепно-мозъчна травма. Критична медицинска сестра; 27; 30-37.
Liu, Y, Jolly, S и Pokala, K (2013). Продължително пароксизмално симпатиково буря, свързано със спонтанен субарахноидален кръвоизлив. Доклади за случаи в медицината; артикул ID 358182.
McCorry, LK (2007). Физиология на вегетативната нервна система. Американски вестник за фармацевтично образование (2007); 71; 1-11.
Perkes, I, Baguley, IJ, Nott, MT и Menon, DK (2010). Преглед на пароксизмалната симпатикова хиперактивност след придобита мозъчна травма. Неврологични анали; 68; 126-135.
Рабинщайн, АА (2007). Пароксизмална симпатикова хиперактивност в неврологичното интензивно отделение. Неврологични изследвания; 29; 680-682.
- Форум за отслабване Phentermine Holistic Bliss Keto Какво хапче мога да взема, за да загубя корема мазнини буря
- Какви природни методи могат да помогнат за потискане на апетита ми Зелено настроение Кето ли Hydroxy Cut работи - буря
- Какви природни методи могат да помогнат за потискане на апетита ми Vexgen Keto Glucagon Отслабване - Буря
- Vexgen Keto Leptiburn At Walmart - Storm Ventures Group
- Vital Max Keto Термални хапчета за отслабване - Storm Ventures Group
