- Цитат: Zullo A, Hassan C, Romiti A, Giusto M, Guerriero C, Lorenzetti R, Campo SM, Tomao S. Проследяване на чревната метаплазия в стомаха: Кога, как и защо. World J Gastrointest Oncol 2012; 4 (3): 30-36
- URL:https://www.wjgnet.com/1948-5204/full/v4/i3/30.htm
- DOI:https://dx.doi.org/10.4251/wjgo.v4.i3.30
В японско проучване с последователни пациенти [19] ИМ е открит при 37% от 1426 H. pylori положителни пациенти (средна възраст: 52,3 години) в сравнение само с 2% от 280 неинфектирани пациенти (средна възраст: 52,7 години). В провинция на северозападен Иран, където и двете H. pylori разпространението и честотата на рак на стомаха са високи, IM е открит при 13% от антралната лигавица и 8,3% от стомашната лигавица на 1011 пациенти (средна възраст: 53,3 години) [20]. От друга страна, в Малайзия, където и двете H. pylori процент на инфекция (4,8%) и честота на рак на стомаха (4,3/100 000) са ниски сред общата популация, IM е открит само при 7,7% от 234 пациенти (средна възраст: 53,4 години), които са претърпели горна ендоскопия, което предполага тясна връзка с инфекцията [21] .
Всички тези данни предполагат, че ИМ е резултат от хронично, възпалително увреждане на стомашната лигавица. Дълготрайният активен гастрит, свързан с H. pylori инфекцията изглежда е основният етиологичен фактор, увеличавайки риска от ИМ в стомаха с 4,5-9 пъти [22 - 24]. Проучване установи, че инфекцията с cagA-позитивна H. pylori щамове е свързано със значително повишено разпространение на IM в сравнение с тези щамове без него [25]. Освен това в H. pylori инфектирани пациенти, настоящ пушач над 20 цигари дневно и висока консумация на масло са свързани с по-нататъшно увеличаване на риска от IM от 4,75 пъти (95% CI: 1,33-16,99) и 2,17 пъти (95% CI: 1,14-4,11 ), съответно [26] .
Доказано е, че степента на разпространение на IM е по-висока при роднини от първа степен на пациенти с рак на стомаха в сравнение с контролите. Всъщност степента на разпространение на ИМ при роднини от първа степен в сравнение със съответстващите контроли е 28,4% срещу 12,2% в Германия [27], 26,1% срещу 12,9% в Корея [28] и 19% срещу 11,7% във Великобритания [29], но не и в Бразилия [30]. Всъщност, неотдавнашен мета-анализ изчислява коефициент на шанс от 1,982 (95% CI: 1,363-2,881) за IM на 1500 субекти от първа степен в сравнение с 2638 контроли [31]. Неотдавнашно иранско проучване върху 808 роднини от първа степен установи подобно разпространение на ИМ между субектите с 1 и тези с> 1 случая в семейството, без разлика, когато индексът е мъж или жена [32] .
По отношение на възможно взаимодействие между H. pylori и фамилна анамнеза, ние наблюдавахме общо разпространение на ИМ от 35,8% при 39 последователни роднини от първа степен, с честота на разпространение до 52,6% при тези с H. pylori инфекция в сравнение с 20% при неинфектираните [33]. Следователно, възможен синергичен ефект между H. pylori инфекция и фамилна анамнеза в развитието на ИМ може да се предположи. Всъщност е подчертана възможна генетична предразположеност към развитие на ИМ в стомаха и наличните данни са анализирани изчерпателно в две скорошни прегледи [34, 35] .
В обобщение: (1) IM се открива при почти 1 от всеки 4 пациенти, подложени на горна ендоскопия; (2) H. pylori инфекцията значително повишава разпространението на ИМ; (3) Степента на разпространение на IM нараства с възрастта на пациента; (4) Разпространението на ИМ е по-високо при роднини от първа степен на пациенти с рак на стомаха; и (5) пушенето (> 20 цигари/дневно) допълнително увеличава разпространението на ИМ.
H. pylori инфекцията, чрез хроничен възпалителен процес на стомашната лигавица, се признава като основен фактор, водещ до развитие на ИМ в стомаха [36]. Следователно, има няколко опита, насочени към индуциране на IM регресия с бактериална ерадикация. Мета-анализ на 7 проучвания обаче установява, че, различно от атрофията, не следва значителна регресия на ИМ H. pylori ерадикация настъпила или в антралната лигавица (OR: 0.795, 95% CI: 0.587-1.078) или в стомашната лигавица на тялото (OR: 0.891, 95% CI: 0.633-1.253) [37]. Тези констатации са потвърдени от по-скорошен мета-анализ на 12 проучвания, включително данни за 2582 пациенти с ИМ в антрума и 2460 в стомашната лигавица на тялото [38]. В подробности само 1 проучване показа, че IM в антрума е обърнат след H. pylori ерадикация и нито едно проучване не показва, че IM в корпуса е подобрен след бактериална ликвидация.
В обобщение: (1) Изглежда, че IM не регресира след H. pylori изкореняване; (2) H. pylori ерадикацията може да забави прогресията на IM; и (3) потенциална химиопрофилактика с добавки на аскорбинова киселина и потенциалната роля на целекоксиб заслужават допълнителни изследвания.
Ролята на IM в стомашната канцерогенеза е единодушно призната. Най-вероятно в последователността на Correa [45] IM е „точката на прекъсване“ на канцерогенезата между хроничния активен гастрит, т.е. доброкачествената, напълно обратима стъпка на последователността и дисплазията, т.е. неинвазивната неоплазия, според класификацията в Падуа [46]. Някои данни биха подкрепили такова предположение. Всъщност проспективно, рандомизирано, 7-годишно последващо китайско проучване установи това H. pylori ерадикацията не е успяла значително да предотврати развитието на рак на стомаха при пациенти, прикриващи ИМ при влизане, докато ракът не се е развил при изкоренените пациенти без ИМ [9] .
Честотата на рак на стомаха при пациенти с ИМ варира от 0% до 10% в скорошен систематичен преглед [46]. Въпреки това, такъв широк диапазон от рак на стомаха може да зависи от огромните разлики между включените проучвания по отношение на размера на пробата (от 14 до 2628 пациенти) или периода на проследяване (от 2 до 23 години) [6] .
В японско проучване на 1246 пациенти и с двамата H. pylori инфекция и IM следват за средно проследяване от 7,8 години, рак на стомаха се развива при 36 пациенти, с относителен риск за наличие на IM от 6,4 (2.6-16.1) [19]. В скорошно проспективно корейско проучване на 541 пациенти с рак на стомаха, наличието на умерено-тежък IM в антралната кост и по-малка кривина на телесната лигавица е свързано със 7,52 (95% CI: 3,06-18,5) и 9,25 (95% CI: 2.39-35.8) съответно повишен риск от рак на стомаха [47] .
Наскоро проведено в цялата страна хистологично холандско проучване, оценило ролята на ИМ в развитието на рак на стомаха [48]. В кохорта от 61 707 пациенти с ИМ ракът на стомаха се развива в 874 случая, което съответства на кумулативна 10-годишна честота от 1,8%, с прогнозна годишна честота от 0,18%. Този анализ обаче е критикуван; до 0.7% от рака е диагностициран в рамките на 10.8 месеца след проследяването [49]. В действителност, като се изключат тези преобладаващи случаи, е изчислена най-вероятната 10-годишна честота от 1,1% (0,11% годишно) на рак на стомаха при пациенти с ИМ [49] .
В обобщение: (1) IM най-вероятно представлява „точката на пречупване“ на канцерогенезата на стомаха; (2) 6-кратно повишен риск от рак на стомаха има при пациенти с ИМ; и (3) действителната честота на рак на стомаха при пациенти с ИМ все още трябва да бъде определена поради широкия интервал, докладван от наличните проучвания.
Доказано е също, че моделът на присъствие на IM в стомаха играе роля при риска от рак на стомаха. В проучване в Колумбия, в сравнение с фокално или антрално преобладаващо IM разпределение (произволно определено като 1), неговото удължаване през цялата по-малка крива повишава риска от рак на стомаха с 5,7 пъти (95% CI: 1,3-26), докато дифузният модел (антрал плюс стомашно тяло) показва 12,2-кратен (95% ДИ: 2,0-72,9) повишен риск [54]. За отбелязване е, че това проучване също така показва, че непълният IM се представя като дифузен по-често от фокалния модел. Връзката между удължаването на IM в стомаха и риска от рак на стомаха е потвърдена в Италия [8]. В това проучване процентът на рак на стомаха изглежда се увеличава с увеличаване на удължаването на IM. По-специално, при първото изследване се предлага удължаване на> 20% IM за идентифициране на пациенти с повишен риск от рак.
В обобщение: (1) наличието на IM от непълен тип е свързано с по-висок риск от рак на стомаха в сравнение с IM от пълен тип; (2) рискът от рак на стомаха е свързан с разпространението на IM в стомаха; и (3) удължаването на IM над 20% изглежда ценна граница.
Съзнанието, че IM представлява определена предракова лезия за рак на стомаха, съчетано с мрачната прогноза за такава неоплазия, когато се диагностицира в напреднал стадий, поражда етични опасения относно оставянето на тези пациенти без планирано проследяване. Подходящото използване на ендоскопски процедури обаче е от съществено значение за рационалното използване на ограничените ресурси. Всъщност разсейването на икономически ресурси при извършване на серийни ендоскопски контроли при всички пациенти с ИМ, повечето от които никога не биха развили рак на стомаха, също би било неетично.
За да се обърне внимание на този проблем, някои параметри могат да се считат за критични: (1) годишната честота на рак на стомаха при ИМ, за да се оцени загубата на продължителността на живота; (2) етапа на рак на стомаха при диагностициране, за да се оцени увеличаването на процента на оцеляване на пациента; (3) ролята на ендоскопското отстраняване на дисплазионните лезии чрез мукосектомия/дисекция за оценка на реалното намаляване на честотата на рак на стомаха; и (4) интервала между две ендоскопии, за да се оцени цената на ендоскопското проследяване.
Рентабилността на наблюдението на ИМ с евентуално развити диспластични и ракови лезии, отстранени чрез ендоскопска резекция на лигавицата, е оценена в друго проучване, моделиращо стратегията върху кохорта от 50-годишни мъже [5]. Според тази симулация наблюдението на ИМ с 5-10 години горна ендоскопия не е било рентабилно, като коефициентът на допълнителна рентабилност е> 500 000 щатски долара за спестена година на живот. Очевидното несъответствие между този модел и предишния [55] вероятно е различната оценка на риска от рак при пациенти с ИМ. В действителност, при последното проучване [5], рискът от рак на стомаха през целия живот при пациенти с ИМ е бил само 1%, много по-нисък от този, наблюдаван при клинични проучвания [8, 49]. Когато авторите симулират по-висок риск от рак на стомаха (т.е. при имигранти от високорисков регион на Китай), е установено, че 5-годишната ендоскопска стратегия за наблюдение е потенциално привлекателна (ICER = 80 600 $ за QALY) [55] .
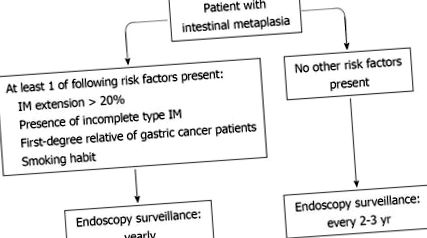
В обобщение: (1) планираният ендоскопски контрол може да бъде рентабилен при пациенти с ИМ; и (2) годишният и двугодишният контрол изглеждат еднакво ефективни, но са необходими специфични проучвания в тази обстановка.
Общата 5-годишна преживяемост при рак на стомаха остава разочароващо ниска, като неоплазията често се открива, когато ендоскопският или хирургичният терапевтичен подход са по-малко ефективни [61]. Следователно, за да се намали смъртността от рак на стомаха, неоплазията трябва да бъде диагностицирана в ранен стадий. IM е определена предракова лезия за стомашен аденокарцином. Често се открива в ендоскопски серии, особено в H. pylori инфектирани пациенти и при роднини от първа степен на пациенти с рак на стомаха, разпространението се увеличава с възрастта. Пациентите с незавършен тип ИМ крият по-висок риск от рак на стомаха в сравнение с тези с пълен тип ИМ. Въпреки това, непълният тип ИМ е много по-рядък от пълен тип (Тип III: 21,5% от 1281 случая на ИМ) [60], така че и двата типа УМ по подобен начин представляват цялостното развитие на рак на стомаха. Освен IM тип, разпределението му в стомаха играе важна роля; ангажирането на антралната и стомашната лигавица на тялото представлява по-висок риск. Стратегията за наблюдение може да бъде рентабилна, поне при тези пациенти с допълнителни рискови фактори за рак на стомаха. Необходимо е голямо проспективно, рандомизирано, многоцентрово проучване, за да се даде точна информация за това кога, как и защо трябва да се грижим за нашите пациенти с ИМ.
Рецензенти: Джиан-Кун Ху, доктор по медицина, доцент, катедра по стомашно-чревна хирургия, Западнокитайска болница, Университет Съчуан, Ченгду 610041, провинция Съчуан, Китай; Джон Гриняцос, д-р, асистент, катедра по хирургия, Университет в Атина, Медицинско училище, 1-ва болница LAIKO, ул. Агиоу Тома 17, GR 115-27, Атина, Гърция
S- редактор Wang JL L- редактор Roemmele A E- редактор Zheng XM
- Целиакия - Рефлукс, Болки в стомаха, Язви - Стомашно-чревна група в Западен Честър
- Храни, които трябва да избягвате, ако се борите с язва на стомаха
- Храни, които трябва да избягвате на празен стомах
- Упражнения за намаляване на стомаха, дупе; Бедра жена - гнездото
- БЪРЗА ПЛОСКА СТОМАШНА ДИЕТА за Android - Изтегляне на APK